Melanie A. McNally
1 Școala de Medicină a Universității Johns Hopkins, Baltimore, MD 21205, SUA
Adam L. Hartman
2 Departamentul de Neurologie, Școala de Medicină a Universității Johns Hopkins, Baltimore, MD 21205, SUA
Abstract
Convulsiile care sunt rezistente la medicamentele standard rămân o problemă clinică majoră. O opțiune subutilizată pentru pacienții cu convulsii rezistente la medicație este dieta cetogenică bogată în grăsimi și cu conținut scăzut de carbohidrați. Dieta și-a primit numele pe baza observației că pacienții care consumă această dietă produc corpuri cetonice (de exemplu, acetoacetat, β-hidroxibutirat și acetonă). Deși mecanismele exacte ale dietei sunt necunoscute, corpurile cetonice au fost presupuse să contribuie la efectele anticonvulsivante și antiepileptice. În această revizuire, sunt discutate proprietățile anticonvulsivante ale corpurilor cetonice și dieta ketogenică (inclusiv efectele GABAergice și glutamatergice). Datorită importanței metabolismului corpului cetonic în primele etape ale vieții, sunt discutate și efectele corpurilor cetonice asupra dezvoltării neuronilor in vitro. Înțelegerea modului în care corpurile cetonice își exercită efectele vor ajuta la optimizarea utilizării lor în tratarea epilepsiei și a altor tulburări neurologice.
Introducere
Epilepsia este o boală devastatoare și răspândită care afectează aproximativ 1% din S.U.A. populație și cel puțin 50 de milioane de oameni în întreaga lume (Hauser & Kurland 1975, Hirtz și colab. 2007, Kobau și colab. 2008). În timp ce a fost dezvoltată o serie de medicamente antiepileptice, acestea rămân incapabile să controleze convulsiile la aproximativ 30% dintre pacienții cu epilepsie (Kwan și Brodie 2000). Unii dintre acești pacienți sunt candidați la rezecția chirurgicală a țesutului anormal (de exemplu, scleroza temporală mezială), dar opțiunile sunt limitate pentru cei fără astfel de leziuni. Pentru a ajuta acești pacienți cu epilepsie intracurabilă nechirurgicală, în anii 1920 a fost dezvoltată o dietă bogată în grăsimi, cu conținut scăzut de carbohidrați, cunoscută sub numele de dietă ketogenică, pentru a imita efectele benefice ale postului asupra controlului convulsiilor (Hartman & Vining 2007). Multe studii clinice au confirmat efectele sale benefice, cu un studiu randomizat care a arătat o scădere cu 75% a convulsiilor la copii pe o dietă ketogenică timp de trei luni (Neal et al. 2008). Cu toate acestea, în timp ce s-au investigat multe posibilități, mecanismele prin care o dietă ketogenică conferă efectele sale anticonvulsivante rămân necunoscute. Dezvăluirea acestor mecanisme va permite perfecționarea utilizării sale clinice, precum și identificarea de noi ținte pentru dezvoltarea viitoare a terapiei.
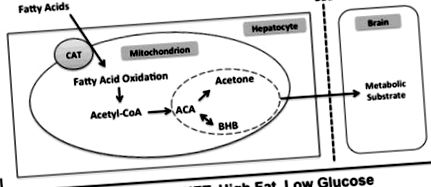
O dietă ketogenică bogată în grăsimi și cu conținut scăzut de carbohidrați determină o schimbare a activității metabolice a hepatocitelor. În aceste condiții, ciclul Krebs nu poate utiliza nivelurile ridicate de acetil-CoA generate din grăsimi. Acetil-CoA rămas este transformat în acetoacetat de corp cetonic. Cele două corpuri cetonice suplimentare, acetonă și β-hidroxibutirat, sunt derivate din acetoacetat prin degradare spontană și conversie enzimatică cu β-hidroxibutirat dehidrogenază. Cele trei corpuri cetonice sunt apoi eliberate din hepatocite, traversează bariera hematoencefalică și își pot exercita efectele în creier. Abrevieri: CAT, carnitină-acilcarnitină translocază; ACA, acetoacetat; BHB, β-hidroxibutirat; BBB, barieră hematoencefalică.
Corpuri cetonice: proprietăți anticonvulsivante
Corpuri cetonice: Posibile mecanisme de acțiune
Studiile in vivo discutate anterior sugerează că corpurile cetonice au proprietăți anticonvulsivante. Au apărut o serie de teorii pentru a explica pragul scăzut al convulsiilor în aceste modele. Glutamatul și respectiv acidul γ-aminobutiric (GABA) sunt principalii neurotransmițători excitatori și inhibitori din creier. A fost dezbătut modul în care corpurile cetonice afectează nivelurile acestor neurotransmițători și receptorii lor, activitatea receptorilor și modul de manipulare a acestora. Apar noi teorii în jurul efectelor corpurilor cetonice asupra potențialului membranei neuronale, excitabilității neuronale și speciilor reactive de oxigen. Aici este prezentată o prezentare generală a datelor actuale care evaluează aceste ipoteze în evoluție.
VGLUT-uri
Alți neurotransmițători, transportori și receptori
Alte sisteme de neurotransmițători care nu sunt de obicei luate în considerare în epilepsie par, de asemenea, necesare pentru efectele anticonvulsivante ale dietei ketogene. Datele privind efectul norepinefrinei includ lipsa efectelor protectoare ale dietei ketogene împotriva fluorotilului convulsiv la șoarecii knockout dopaminici beta-hidroxilazici care nu pot sintetiza norepinefrina (Szot și colab. 2001). Dovezi ale necesității neurotransmisiei adenozinei au fost prezentate atunci când șoarecii cu mutații ale receptorilor adenozinei A1 nu au fost protejați împotriva convulsiilor recurente după tratamentul dietei ketogene (Masino și colab. 2011). O dietă ketogenică a scăzut, de asemenea, enzima metabolizantă a adenozinei, adenozin kinaza. Alți neurotransmițători nu au fost investigați la fel de amănunțit.
Canale KATP
Ciclul Krebs și lanțul de transport al electronilor
O teorie a efectelor polifacetice ale dietei ketogene este că aceasta poate optimiza funcția ciclului Krebs, cu un efect ulterior asupra funcției neuronale. Punctul logic de plecare pentru această teorie este că acetil CoA (un produs din aval al cetogenezei) este un substrat primar pentru ciclul Krebs (Fig. 1). În avalul ciclului Krebs, β-hidroxibutiratul a îmbunătățit activitatea redox și a scăzut moartea celulară în celulele SH-SY5Y dopaminergice după expunerea la toxina I complexă rotenonă (Imamura și colab. 2006). β-hidroxibutiratul pare să necesite un complex II intact pentru a-și conferi efectele benefice în două modele diferite de neurodegenerare, inclusiv un model complex de toxină II (acid 3-nitropropionic) și modelul SOD1-G93A de șoarece de scleroză laterală amiotrofică (boala Lou Gehrig) (Tieu și colab. 2003; Zhao și colab. 2006). Mai recent, Kim și colab. a arătat în felii de hipocamp că un cocktail de β-hidroxibutirat și acetoacetat a păstrat activitatea sinaptică după expunerea la rotenonă sau acid 3-nitropropionic, deși au existat unele disparități regionale (de exemplu, răspunsuri diferite chiar și în aceeași felie) observate în timpul expunerii la cetonă (Kim do și colab. 2010). Motivul diferențelor dintre cele două studii privind acidul 3-nitropropionic este neclar.
S-a demonstrat, de asemenea, că o dietă ketogenică induce transcrierea unor mARN-uri ale subunității lanțului de transport al electronilor (Bough et al. 2006). Un număr crescut de subunități ale lanțului de transport de electroni ar putea crește „rezervele de energie” neuronale și, de fapt, dietele ketogenice cresc nivelul ATP creierului în unele (dar nu toate) studiile de rozătoare (DeVivo și colab. 1978; Bough și colab. 2006, Nylen și colab al. al. 2009, Kim do și colab. 2010). O ipoteză finală este că nivelurile crescute de ATP pot stabiliza potențialul membranei neuronale prin îmbunătățirea funcției Na + -K + -ATPazelor (Bough & Rho 2007). Deși satisfăcătoare din punct de vedere teleologic, evenimentele prezentate aici nu au fost complet legate în mod experimental nici în modelele animale normale, nici în cele de epilepsie. Cu toate acestea, experimentele individuale indică importanța potențială a ciclului Krebs și a funcției lanțului de transport al electronilor în efectele corpurilor cetonice.
Neuroni imaturi și în curs de dezvoltare
Efecte antioxidante
Corpurile cetonice pot avea, de asemenea, efecte antioxidante. Producția de specii reactive de oxigen care rezultă din expunerea la glutamat este inhibată de corpurile cetonice în culturile primare de neuroni neocorticali de șobolan (Maalouf și colab. 2007). Mecanismul pare să implice oxidarea NADH, mai degrabă decât un efect antioxidant mediat de glutation. Dimpotrivă, dieta cetogenă (mai degrabă decât corpurile cetonice) poate modifica metabolismul glutationului prin factorul de transcripție Nrf2 (Milder și colab. 2010). Corpurile cetonice protejează și împotriva morții celulare după ce feliile neocorticale sunt expuse la peroxid de hidrogen (Kim do și colab. 2007). În plus, corpurile cetonice previn afectarea indusă de peroxidul de hidrogen a potențării pe termen lung a hipocampului (Maalouf & Rho 2008). Prin urmare, pe lângă efectele asupra neurotransmisiei, aceste date sugerează că corpurile cetonice pot fi neuroprotectoare împotriva speciilor reactive de oxigen produse în stări neuropatologice.
Concluzii
Posibile efecte anticonvulsivante ale corpurilor cetonice asupra creierului. (1) Sinteza crescută a GABA prin modificarea ciclului de glutamat în ciclul glutamat-glutamină sau modificarea reacției neuronale la GABA la receptorii GABAA. (2) Scăderea eliberării de glutamat prin inhibarea competitivă a transportorilor de glutamat vezicular. (3) Alți neurotransmițători, inclusiv norepinefrină și adenozină. (4) Creșterea hiperpolarizării potențiale a membranei prin canalele KATP posibil mediate de semnalizarea receptorului GABAB. (5) Scăderea producției de specii reactive de oxigen din expunerea la glutamat. (6) Transcrierea subunității lanțului de transport al electronilor. Abrevieri: A1R, receptor de adenozină; Cl, clorură; GLN, glutamină; GLU, glutamat; GABA, acid γ-aminobutiric; GABABR, receptor beta al acidului γ-aminobutiric; GABAAR, receptor alfa al acidului γ-aminobutiric; VGLUT, transportor de glutamat vezicular; ROS, specii reactive de oxigen.
Mulțumiri
Sprijinit de Howard Hughes Medical Institute Medical Research Fellows Program (MAM), K12NS001696, K08NS070931 și un premiu Clinician Scientist (Johns Hopkins University School of Medicine) (ALH). Autorii nu au conflicte de interese de dezvăluit.
- Cum rezistă corpurile noastre să slăbească
- Dieta Keto pentru epilepsie Ce să știți WTOP
- TRATAMENT MODERN AL EPILEPSIEI REZISTENTE LA MEDICAMENTE, DISPONIBILĂ ÎN RUSIA Epilepsie ayvaziană și paroxistică
- Modul în care dansatorii de balet de elită își alimentează corpul între spectacole - Business Live
- Intervenții dietetice importante pentru medicina epilepsiei FX