Yirong Zhu
⁎ Programul de biologie celulară și moleculară, Universitatea de Stat din Michigan, East Lansing, MI
† Programul de cercetare a cancerului de sân și a mediului, Universitatea de Stat din Michigan, East Lansing, MI
Mark D. Aupperlee
† Programul de cercetare a cancerului de sân și a mediului, Universitatea de Stat din Michigan, East Lansing, MI
‡ Departamentul de fiziologie, Universitatea de Stat din Michigan, East Lansing, MI
Sandra Z. Haslam
† Programul de cercetare a cancerului de sân și a mediului, Universitatea de Stat din Michigan, East Lansing, MI
‡ Departamentul de fiziologie, Universitatea de Stat din Michigan, East Lansing, MI
Richard C. Schwartz
† Programul de cercetare a cancerului de sân și a mediului, Universitatea de Stat din Michigan, East Lansing, MI
§ Departamentul de Microbiologie și Genetică Moleculară, Michigan State University, East Lansing, MI
Abstract
Introducere
Material si metode
Șoareci și diete
tabelul 1
| Gras | Ulei de porumb | 2.369 e cel mai frecvent | 16.1498 |
| Untură | 1,8957 | 31.6537 | |
| Carbohidrați | Amidon de porumb | 54.407 e cel mai frecvent | 8.888 este cel mai frecvent |
| Maltodextrină | Cel mai frecvent 11.848 | 16.1498 | |
| Proteină | Cazeină | 18.987 cel mai frecvent | 25,8397 |
| L-cisteina | 0,2843 | 0,3876 | |
| Fibră | Celuloză | 4.7393 | 6.4599 |
| Vitamine | Mix de vitamine V10001 | 0,9479 | 1.2919 |
| Bitartrat de colină | 0,1889 | 0,2584 | |
| Minerale | Amestec de minerale> S10026 | 0,9479 | 0,1286 |
| Fosfat dicalcic | 1.2322 | 1,6795 | |
| Carbonat de calciu | 0,5213 | 0,7106 | |
| Citrat de potasiu, 1 H20 | 1,5639 | 2.1318 | |
| Energie | |||
| densitate kcal/g | 3.8 | 5.2 | |
| % kcal | Gras | 10 | 60 |
| Carbohidrați | 70 | 20 | |
| Proteină | 20 | 20 | |
Tumorigeneză
Șoarecii în vârstă de 3 săptămâni au fost repartizați aleatoriu în grupurile LFD și HFD (LFD, n = 60; HFD, n = 80). Începând cu vârsta de 5 săptămâni, șoarecii din ambele grupuri au fost tratați prin gavaj oral o dată pe săptămână timp de patru săptămâni cu 7,12-dimetilbenz [a] antracen (DMBA) dizolvat în ulei vegetal (50 mg/kg greutate corporală/șoarece). La vârsta de 13 săptămâni (10 săptămâni pe dietă) și la 19 săptămâni (16 săptămâni pe dietă), 3 până la 5 șoareci din fiecare grup au fost selectați aleatoriu și sacrificați la estrus pentru a examina efectele timpurii ale HFD înainte de dezvoltarea tumori palpabile. Șoarecii rămași au fost palpați de două ori pe săptămână pentru dezvoltarea tumorii până la sfârșitul experimentului la vârsta de 52 de săptămâni. Tumorile au fost recoltate la 1 cm în diametru. La terminare, porțiuni de tumori și țesuturi mamare au fost fie fixate în formalină și prelucrate ca monturi întregi [11], fie încorporate în parafină pentru colorarea hematoxilinei și eozinei și imunohistochimie [12]. Preparatele de glandă și secțiuni de hematoxilină și eozină au fost evaluate pentru morfologia generală, prezența hiperplaziei și neoplazia [13]. Toate leziunile și tumorile au fost revizuite și clasificate, după cum sa descris anterior [14].
Analiza întregului montaj
Glandele mamare inghinale fixate pe formalin au fost evaluate pentru creșterea ductală longitudinală măsurată de distanța dintre cel mai distal canal terminal și ganglionul limfatic. Mugurii terminali terminali (TEB) au fost definiți ca vârfuri ductale multistratificate mărite, cu un diametru mai mare de 100 μm, care au fost înconjurate de adipocite și situate în periferia glandei.
Imunohistochimie
Parametrii metabolici
Șoarecii au fost posti timp de 4 ore înainte de recoltarea și sacrificarea sângelui. Nivelurile de glucoză și insulină plasmatică au fost prelevate prin puncție cardiacă și coagulare prevenită cu EDTA. Nivelurile de glucoză plasmatică au fost determinate de OneTouch UltraMini (Lifescan, Milpitas, CA), iar nivelurile de insulină au fost determinate cu setul ELISA de insulină pentru șobolani/șoareci (Millipore, Billerica, MA), conform instrucțiunilor producătorului.
Analize statistice
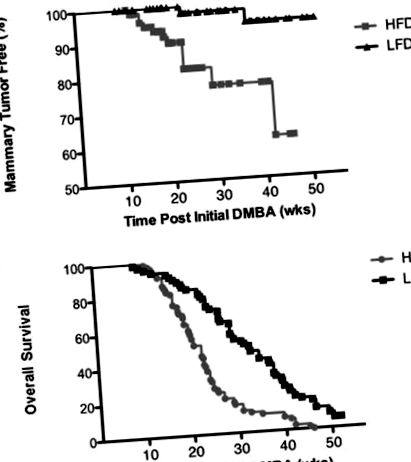
Rezultatele sunt prezentate ca medie ± deviație standard (SD) pentru greutatea corporală și medie ± eroare standard a mediei (SEM) pentru analize imunohistochimice. Diferențele au fost considerate semnificative la P Figura 1 A). Majoritatea tumorilor au fost ER și PR negative (2/2 tumori LFD; 11/12 tumori HFD) (Tabelul 2). Dintre cele două tumori care s-au dezvoltat la șoareci hrăniți cu LFD, una a fost de adenosquamous și una a fost de histopatologie epitelială. Jumătate din tumorile HFD au fost de histopatologie epitelială (6/12; glandulare, papilare, cribriforme, solide), în timp ce restul au fost de histopatologii adenoschamoase (4/12) și cu celule fusiforme (2/12) (Tabelul 2). HFD a promovat, de asemenea, dezvoltarea tumorilor în alte sisteme de organe, producând tumori ale pielii și ficatului și limfoame care au dus la o supraviețuire globală semnificativ mai slabă (Figura 1 B).
Dieta bogată în grăsimi promovează tumorogeneza mamară indusă de DMBA. (A) Un complot Kaplan-Meier a indicat faptul că numărul glandelor mamare fără tumori a scăzut în timp într-o măsură mai mare la o dietă bogată în grăsimi (n = 70) decât la o dietă săracă în grăsimi (n = 50). (B) Un complot Kaplan-Meier a indicat faptul că dieta bogată în grăsimi a scăzut supraviețuirea generală.
masa 2
Proprietățile tumorilor.
| M11 | HFD | 17 | Epitelial | ER−/PR- |
| M21 | HFD | 19 | Adenosquamous | ER−/PR- |
| M45 | HFD | 19 | Adenosquamous | ER−/PR- |
| M20 | HFD | 20 | Adenosquamous | ER−/PR- |
| M27 | HFD | 22 | Epitelial | ER−/PR- |
| M72 | HFD | 24 | Epitelial | ER−/PR- |
| M26 | HFD | 25 | Adenosquamous | ER−/PR- |
| M37 | HFD | 28 | Celula fusului | ER−/PR- |
| M37 | HFD | 28 | Epitelial | ER−/PR- |
| M47 | HFD | 28 | Celula fusului | ER +/PR+ |
| M80 | HFD | 34 | Epitelial | ER−/PR- |
| M84 | HFD | 47 | Epitelial | ER−/PR- |
| M46 | LFD | 28 | Adenosquamous | ER−/PR- |
| M34 | LFD | 42 | Epitelial | ER−/PR- |
Tumorile care s-au dezvoltat la șoarecii hrăniți cu HFD au avut o latență medie de 25,9 ± 2,4 săptămâni, comparativ cu 35 de săptămâni pentru tumorile LFD. În plus, a existat un subset de tumori HFD care s-au dezvoltat înainte de cea mai timpurie tumoare la șoareci hrăniți cu LFD (vârsta de 28 de săptămâni) (Tabelul 2). Acest subset precoce a avut o predominanță a tumorilor adenozchmoase (4/6). Tumorile timpurii au avut o latență medie de 20,9 ± 1,1 săptămâni și tumorile HFD în curs de dezvoltare tardivă au avut o latență medie de 33 ± 3,7 săptămâni.
Am observat anterior că HFD a promovat dezvoltarea tumorii la șoarecii BALB/c prin proliferare crescută, angiogeneză și recrutarea macrofagelor M2 activate alternativ [7], [8]. Pentru a determina baza pentru promovarea HFD a tumorigenezei în acest studiu, tumorile au fost analizate pentru proliferare, angiogeneză și recrutarea macrofagelor. Tumorile care s-au dezvoltat la șoareci FVB hrăniți cu LFD și HFD au avut niveluri similare de proliferare (HFD = 8,3 ± 1,0%, LFD = 8,7 ± 2,4%), angiogeneză (HFD = 16,2 ± 1,2%, LFD = 19,1 ± 4,6%) și similare niveluri de macrofage totale în cadrul tumorilor (HFD = 31,8 ± 5,7, LFD 31 ± 18,4. Cu toate acestea, a existat o tendință către creșterea numărului de macrofage M2 intra-tumorale în tumorile care s-au dezvoltat pe HFD (5,2 ± 1,5) comparativ cu LFD (1,2 ± 0,4) (P = 0,24) (Figura 2).
Dieta bogată în grăsimi a determinat o tendință către creșterea macrofagelor M2 intra-tumorale, măsurată prin colorare dublă F4/80-Arg1 (P = .24). LFD (n = 2), HFD (n = 8).
HFD promovează dezvoltarea canalului pubertal și proliferarea celulelor epiteliale
După ce am stabilit că HFD promovează dezvoltarea tumorilor induse de cancerigen, am căutat să examinăm efectele precoce ale HFD asupra dezvoltării glandei mamare. După doar o săptămână de dietă, HFD a crescut numărul de TEB, structurile extrem de proliferative găsite la vârfurile canalelor în creștere în timpul pubertății (Figura 3 A). După 2 săptămâni de dietă, șoarecii hrăniți cu HFD au avut o alungire ductală îmbunătățită (Figura 3, B și C). După 3 săptămâni de dietă, creșterea ductală la șoarecii hrăniți cu LFD și HFD nu se distinge, cu niveluri similare de alungire ductală și număr de TEB (Figura 3, A și B). După 4 săptămâni de dietă, alungirea ductală distală a atins limita tamponului de grăsime inghinală atât pentru șoarecii hrăniți cu LFD cât și cu HFD, iar TEB-urile au fost reduse în mod similar în număr în ambele grupuri.
Dieta bogată în grăsimi favorizează dezvoltarea canalelor pubertale și proliferarea celulelor epiteliale. (A) Dieta bogată în grăsimi a crescut numărul mugurilor finali (TEB) (*, P Figura 4). Dezvoltarea accelerată a glandei mamare la șoarecii hrăniți cu HFD nu a fost rezultatul apariției precoce a pubertății, deoarece nu a existat nicio diferență semnificativă în vârsta medie a deschiderii vaginale la șoarecii hranați cu LFD și HFD (29,3 ± 1,8 zile și 29,6 ± 2,3 zile, respectiv).
Șoarecii hrăniți cu o dietă bogată în grăsimi timp de 2 săptămâni au prezentat o proliferare celulară crescută în structuri epiteliale normale, măsurată prin încorporarea 5-bromo-2'-deoxiuridinei (BrdU) (*, P Figura 5 A). Analiza proliferării la 10 săptămâni pe dietă a arătat o proliferare crescută a leziunilor hiperplazice în comparație cu țesutul normal atât la șoarecii hrăniți cu LFD, cât și cu HFD, cu o tendință spre o mai mare proliferare a leziunilor pe HFD (P = .14) (Figura 5 B). Canalele mari au arătat o creștere semnificativă a proliferării în rândul șoarecilor hrăniți cu HFD. Nu au existat diferențe dietetice în proliferare între diferitele structuri ale glandei mamare și hiperplazii la 16 săptămâni de dietă sau densitatea vaselor de sânge la 10 sau 16 săptămâni de dietă (datele nu sunt prezentate).
- Nrf2 reprimă FGF21 în timpul unei diete cu conținut ridicat de grăsimi pe termen lung - obezitate indusă la diabet la șoareci
- Stabilitatea unui model de șobolan de tip 2 diabet indus de alimentația cu conținut ridicat de grăsimi cu doze mici
- Noua dietă FAD promovează postul - Dieta la modă sfătuiește să mănânce orice, apoi postul
- Oamenii de știință descoperă modul în care dieta bogată în grăsimi determină creșterea cancerului colorectal
- Reddit - ketoscience - O dietă periodică care mimează postul promovează regenerarea multi-sistem,