Abstract
Hipoxia crește eritropoieza mediată de factori de transcripție inductibili de hipoxie (HIF), care reglează transcrierea eritropoietinei. Neocitoliza este un mecanism fiziologic care corectează policitemia de la hipoxemia cronică susținută prin distrugerea tranzitorie și preferențială a eritrocitelor tinere după restabilirea normoxiei. Am arătat că neocitoliza este cauzată de specii de oxigen reactiv derivate mitocondriale excesive în reticulocite mediate de reglarea descendentă a mitofagiei reglementate BNIP3L controlate prin HIF și de o scădere a catalazei antioxidante RBC (CAT) în eritrocitele produse de hipoxie. Scăderea CAT rezultă din miR-21 indusă de hipoxie care reglează în jos CAT. Acest lucru se corelează cu o scădere acută tranzitorie a HIF-1 la revenirea normoxică care este asociată cu normalizarea masei eritrocitare.
apneea obstructivă în somn (OSA), caracterizată printr-un model unic de hipoxie cronică intermitentă (CIH), este asociată cu comorbidități cardiovasculare, endocrine și neurocognitive și cu un risc crescut de cancer. Rolul corpului carotidian în fiziopatologiile modulate de OSA a fost bine studiat; aici definim anomalii hematologice și discutăm rolul posibil al modificărilor sanguine OSA asupra sănătății. Am găsit numai asta
1% dintre pacienții cu OSA au dezvoltat policitemie, care nu a fost atribuibilă altor cauze și a fost corectată cu terapia continuă pozitivă a presiunii căilor respiratorii (CPAP). Cu toate acestea, în studiile noastre pilot OSA, am constatat creșterea speciilor reactive de oxigen (ROS) și a masei mitocondriale cu scăderea catalazei (CAT) și BNIP3L în celulele sanguine, alături de creșterea markerilor inflamatori. După corectarea OSA cu utilizarea CPAP pentru> 3 luni, unele, dar nu toate, din aceste anomalii au fost corectate.
Schimbările sanguine observate în OSA contribuie probabil la starea de sănătate afectată; cu toate acestea, rolurile lor fiziopatologice trebuie definite cu atenție.
Hipoxemie cronică susținută
Modelul neocitolizei de șoarece
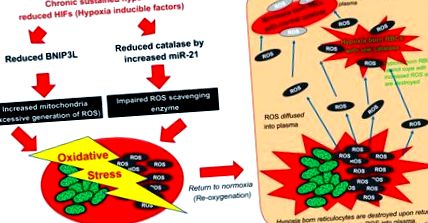
1% dintre globulele eritrocitare, modificările timpului de înjumătățire plasmatică al reticulocitelor nu ar explica o scădere atât de rapidă a hematocritului după revenirea normoxică. Cu toate acestea, administrarea unui agent antioxidant, N-acetil-cisteina sau injecția de polietilen glicol conjugat CAT atenuează rata hemolitică, demonstrând că reticulocitele generate de ROS difuză în plasmă, au contact cu RBC circulante și distrug preferențial acele RBC născute cu hipoxie cu activitate CAT mai scăzută (adică, neocitoliză). Este probabil ca și eritrocitele mai în vârstă să fie afectate de ROS plasmatic, dar probabil într-un grad mai mic decât eritrocitele mai tinere cu CAT scăzut. Pentru a demonstra că aceste constatări sunt modulate de HIF, un model de șoarece cu reglare ascendentă constitutivă a HIF, având o mutație a pierderii funcției VHL, un regulator negativ al HIF-urilor [așa-numitul șoarece de policitemie Chuvash (16)] a atenuat neocitoliza . În mod similar, creșterea activității HIF prin injectarea dimetiloxaloilglicinei, un inhibitor al prolil hidroxilazei 2 (principalul regulator negativ al HIF), a atenuat neocitoliza, indicând faptul că o scădere rapidă a nivelurilor HIF este responsabilă pentru neocitoliză. Mecanismele neocitolizei, constând în producția crescută de ROS și însoțirea scăderii capacității de eliminare a ROS, sunt prezentate în Fig. 1 .
Mecanismul propus de neocitoliză. Neocitoliza este cauzată de creșterea speciilor de oxigen reactiv mitocondrial (ROS). ROS sunt generate de o creștere a masei mitocondriale de către BNIP3L direcționat HIF în reticulocite. ROS este difuzat în plasmă din reticulocitele distruse la revenirea la normoxie. Scăderea catalazei prin miR-21 indusă de hipoxie crește acumularea ROS. Celulele roșii din sânge născute de hipoxie suferă neocitoliză din cauza capacității afectate de a face față stresului oxidativ crescut.
Activitatea HIF în hipoxia acută și cronică
CIH și OSA
Spre deosebire de CSH, CIH constă în cicluri repetitive de normoxie și hipoxie. OSA este un prototip al CIH, caracterizat prin obstrucție respiratorie recurentă din cauza colapsului căilor respiratorii superioare, rezultând desaturări ciclice ale oxigenului (30). Cu toate acestea, în timp ce pacienții cu OSA au cicluri semnificative de hipoxie severă în timpul somnului, majoritatea nu sunt policitemici, așa cum era de așteptat (43). Astfel, am creat experimentele pentru a rezolva acest aparent puzzle fiziopatologic. Am găsit numai asta
- Cum să sprijini un prieten cu o boală cronică SINE
- Modul în care industria suplimentelor alimentare menține reglementarea la distanță • OpenSecrets
- SFC ME cauzat de infecția parazit Health Rising; cu sindromul oboselii cronice (MECFS) și
- Este oboseala cronică sau doar suprasolicitarea și creșterea în greutate
- Reglarea insulinei a mușchilor scheletici PDK4 Expresia mARN-ului este afectată de insulina acută rezistentă