Sukhdip Singh
1 Spitalul Magee-Womens, Pittsburgh, PA 15213, SUA
Keith M. Wirth
1 Spitalul Magee-Womens, Pittsburgh, PA 15213, SUA
Amy L. Phelps
2 Departamentul de Anestezie, Universitatea din Pittsburgh și Școala de Afaceri a Universității Duquesne, Pittsburgh, PA 15282, SUA
Manasi H. Badve
1 Spitalul Magee-Womens, Pittsburgh, PA 15213, SUA
Tanmay H. Shah
1 Spitalul Magee-Womens, Pittsburgh, PA 15213, SUA
Neera Sah
3 Sf. Spitalul Margaret, Pittsburgh, PA 15203, SUA
Manuel C. Vallejo
1 Spitalul Magee-Womens, Pittsburgh, PA 15213, SUA
4 Departamentul de Anestezie, Spitalul Magee-Womens din UPMC, 300 Halket Street, Pittsburgh, PA 15213, SUA
Abstract
1. Introducere
Prevalența obezității a crescut la proporții epidemice în ultimii 20 de ani, cu estimări de cel puțin 1,6 miliarde de supraponderali și 400 de milioane de adulți obezi în întreaga lume [1]. Mulți parturienți câștigă o cantitate semnificativă de greutate în timpul sarcinii și, prin urmare, mulți pacienți satisfac cerința obezității cu un IMC> 30 kg/m2, făcând din managementul adecvat o preocupare importantă pentru clinicienii obstetrici din întreaga lume [2].
În timp ce anestezia regională poate oferi aceste avantaje față de anestezia generală, cantitatea crescută de grăsime subcutanată și epidurală în populația obeză poate reprezenta o provocare semnificativă pentru plasarea cu succes a cateterului epidural. Înainte de vizualizarea SUA, palparea reperelor osoase era singura tehnică disponibilă pentru identificarea spațiilor lombare interspinoase. Stiffler și colab. [11] au raportat dificultăți în palparea reperelor la 5% dintre pacienții cu IMC normal, 33% la cei care erau supraponderali și la 68% dintre pacienții obezi. Procesele spinoase ale unor pacienți obezi pot fi localizate la mai mult de 5 cm de piele, cu ligamentum flavum adânc de până la 8 cm și la extreme de 11-12 cm adâncime [12]. Grau și colab. [13] a stabilit că la termen, zona optimă de puncție pe piele pentru canularea epidurală este mai mică, canalul țesuturilor moi dintre procesele spinale este mai îngust, iar spațiul epidural este, de asemenea, mai îngust. Fiecare dintre aceste modificări ar fi cel mai probabil exagerată la acei pacienți care sunt obezi morbid. Alte motive includ dificultatea în poziționarea pacientului și o probabilitate crescută de falsă pozitivitate la pierderea tehnicii de rezistență la localizarea spațiului epidural [13, 14].
Utilizarea ultrasonografiei (SUA) pentru plasarea cateterelor epidurale a devenit din ce în ce mai populară și s-a demonstrat că reduce ratele de eșec al cateterului epidural și încercările de plasare [15, 16]. SUA pot fi utilizate pentru a identifica spațiul epidural, pentru a localiza linia mediană, pentru a furniza o estimare a adâncimii de la piele la spațiul epidural și pentru a estima punctul de inserție și unghiul de inserare a acului [16-19]. Vizualizarea prepuncturii a spațiului epidural sa dovedit a reduce numărul încercărilor de plasare epidurală și a reduce incidența puncției durale accidentale, în special în rândul noilor stagiari rezidenți [12, 15, 16]. Prezența țesutului adipos crescut face vizualizarea SU a spațiului epidural mai dificilă și o problemă semnificativă atunci când se utilizează SUA la parturienii obezi este că vizualizarea scăzută a spațiului epidural face estimarea distanței de la piele la spațiul epidural mai puțin previzibilă [12 ].
Într-un studiu anterior, am investigat utilizarea SUA pentru plasarea cateterului epidural la parturienții care lucrează, am găsit o corelație ridicată între adâncimea estimată a SUA și adâncimea reală a acului (ND); (Coeficientul de corelație Pearson ≥0,91) [16], și a derivat o ecuație de adâncime epidurală (EDE) utilizând regresie liniară multivariantă în trepte pentru prezicerea distanței de la piele la spațiul epidural în zona intervertebrală lombară inferioară.
Într-un studiu realizat de Balki și colab. [20] pe parturienții cu obezitate morbidă care utilizează SUA, au găsit un coeficient de corelație Pearson de 0,85 între distanța estimată de SUA la spațiul epidural și adâncimea reală a acului (ND). Scopul acestui studiu este de a determina dacă EDE estimează adâncimea spațiului epidural înainte de vizualizarea SUA ar putea îmbunătăți imagistica și ar putea duce la o mai bună corelație clinică la parturienții obezi morbid.
2. Metode
Cu aprobarea comisiei de revizuire a investigației locale și consimțământul verbal și scris informat, au fost recrutați în studiu parturienții cu obezitate morbidă (IMC ≥ 40 kg/m 2) care au solicitat analgezie epidurală de muncă sau au fost programați pentru operația cezariană electivă. Criteriile de excludere au inclus pacienții cu preeclampsie severă, antecedente de intervenții chirurgicale la spate, scolioză semnificativă, IMC ≤ 40 kg/m2 și/sau patologie lombară.
2.1. Determinarea ecuației adâncimii epidurale și scanarea cu ultrasunete
Înainte de introducerea scanerului și a cateterului epidural din SUA, adâncimea epidurală estimată a fost calculată mai întâi folosind ecuația de adâncime epidurală descrisă (EDE) derivată din studiul anterior din SUA la instituția noastră [16]:
Apoi, spațiul intervertebral L3-4 sau L4-5 a fost determinat de palparea creastei iliace, iar pe linia lui Tuffier, interspațiul vertebral a fost identificat și marcat cu un marker de neșters. Această marcă a fost utilizată pentru a vizualiza atât planurile longitudinale mediane și transversale ale SUA, confirmarea liniei medii și determinarea punctului final de inserție în spațiul intervertebral care a dat cea mai bună vedere a ligamentului flavum. Cu cunoștințe prealabile despre adâncimea epidurală calculată, parturientul a avut vizualizare US în planurile longitudinale mediană și transversală cu estimarea distanței de la piele la ligament flavum (dura posterioară) înainte de inserarea cateterului epidural (Figurile 1 1 și 2) 2) prin investigatorul primar (VM). Pentru scanarea SUA a fost utilizat sistemul SonoSite S-Nerve US (SonoSite, Bothell, WA, SUA) cu o sondă cu matrice curbată de 2–5 MHz. Un stagiar rezident care a fost supravegheat de investigatorul primar (MV) a plasat cateterul epidural cu cunoștințe despre adâncimea epidurală calculată, adâncimea epidurală longitudinală SUA și adâncimea epidurală transversală SUA. Odată ce cateterul epidural a fost plasat în spațiul epidural, a fost înregistrată adâncimea efectivă clinică a acului în spațiul epidural (ND).
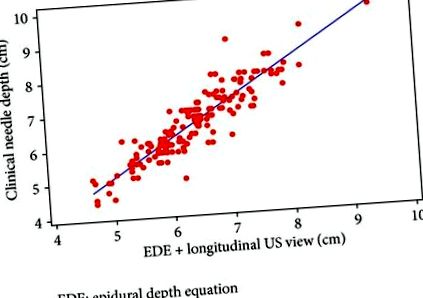
Ecuația adâncimii epidurale plus vizualizarea longitudinală a SUA versus adâncimea clinică a acului.
Ecuația adâncimii epidurale plus vedere transversală SU față de adâncimea clinică a acului.
2.2. Tehnica epidurala
Protocolul de studiu a urmat tehnica standard epidurală a muncii la instituția noastră, cu singura excepție fiind utilizarea EDE pentru a estima inițial adâncimea acului, împreună cu vederi SUA (transversale și longitudinale) pentru a măsura adâncimea până la spațiul epidural, a determina linia mediană, inserarea punct și direcția acului înainte de inserarea cateterului epidural. Poziția șezută a fost menținută pe tot parcursul vizualizării SUA și plasării cateterului epidural.
Folosind o tehnică sterilă, cateterul epidural a fost plasat folosind abordarea liniei medii printr-un ac Tuohy de calibru 17 la interspațiul vertebral L3-4 sau L4-5 folosind o tehnică de pierdere a rezistenței la soluția salină. Cateterul epidural (Arrow FlexTip Plus, Arrow International, Reading, PA, SUA) a fost introdus 5 cm în spațiul epidural și apoi fixat cu pansament adeziv și bandă. Toți pacienții au primit un bolus inițial de 10 ml de 0,0825% bupivacaină și fentanil 100 μg și au fost plasați pe o perfuzie de analgezie epidurală controlată de pacient (PCEA). Parametrii PCEA au inclus perfuzie epidurală continuă de 8 ml/oră, PCEA necesită o doză de bolus de 8 ml, PCEA solicită blocarea dozei de bolus la fiecare 8 minute și PCEA o blocare totală de 1 oră de 24 ml. Pacienților supuși unei operații cezariane elective li s-a pus un ac spinal plasat prin acul epidural și li s-a administrat 12 mg de bupivacaină hiperbară 0,75%, 0,2 mg morfină fără conservanți și 20 μg de fentanil.
O încercare de inserție epidurală a fost definită ca avansarea acului într-un efort de a pătrunde în spațiul epidural; un ac care necesită retragere pentru redirecționare sau reintroducere a fost considerat ca o încercare suplimentară. O epidurală eșuată a fost definită ca un cateter epidural care necesită înlocuire în timpul travaliului. Eșecurile timpurii și tardive au fost definite în funcție de necesitatea înlocuirii cateterului în sau, după primele 90 de minute de la inserare, respectiv. Un anestezist al personalului care a fost orbit dacă au fost obținute puncte de vedere EDE + SUA a luat decizia cu privire la înlocuirea cateterului epidural. Scorul analogic vizual (VAS) (0 = fără durere, 10 = cea mai gravă durere) a fost utilizat pentru a evalua durerea înainte și după activarea epidurală și la evaluarea pacienților pentru analgezie inadecvată. O epidurală eșuată a fost definită ca un bloc care furnizează analgezie inadecvată (VAS ≥ 4/10) în ciuda următoarelor etape secvențiale: (1) un bolus de 10 ml al amestecului de perfuzie epidurală și reevaluare la 15 minute; (2) un al doilea bol de 10 ml al amestecului de perfuzie epidurală și reevaluare la 15 min; și (3) un bolus de lidocaină de 5 ml 1,5%.
Variabilele măsurate au inclus date demografice și obstetricale (vârstă, înălțime și greutate), numărul de sarcini, paritate, dilatare cervicală, rata epidurală eșuată, încercări de inserție epidurală (redirecționări), încercări de plasare epidurală (reinserții), intervenții ale personalului (necesitatea participanților) asistența anestezistului în timpul încercării de plasare), numărul de suplimente epidurale suplimentare (bolusuri) necesare, rata de puncție durală accidentală (ADP) și rezultatul nașterii materne (livrare vaginală, cezariană și cezariană electivă). Adâncimea epidurală calculată de la EDE, adâncimea epidurală longitudinală a SUA (ligamentum flavum/posterior dura), adâncimea epidurală transversală SUA (ligamentum flavum/dura dura posterioară) și adâncimea clinică a acului (ND) până la spațiul epidural, măsurată cu ajutorul unui steril au fost înregistrate, de asemenea, o riglă la cel mai apropiat 0,1 cm.
2.3. Analize statistice
Balki și colab. [20] a constatat că coeficientul de corelație Pearson dintre adâncimea UD și ND a fost de 0,85; IC 95%, 0,75-0,91. Credem că utilizarea EDE + US ar avea ca rezultat un coeficient de corelație de aproximativ 0,91, după cum sa raportat în studiul nostru anterior [16]. Distribuția coeficienților de corelație a eșantionului nu a fost în mod normal dispersată, iar intervalele de încredere pentru coeficienții de corelație nu au fost simetrice. Prin urmare, pentru a menține estimarea limită inferioară în 0,04 dintr-o corelație de 0,91 și pentru a menține un nivel de încredere de 95%, 140 de pacienți ar trebui să fie eșantionați. Pentru a permite pacienților care ar putea să nu finalizeze studiul, au fost înrolați 160 de pacienți.
Datele demografice au fost analizate utilizând statistici descriptive, incluzând media (± SD) pentru datele de interval, procentele pentru datele nominale și mediana (intervalul) pentru datele ordinale. Coeficientul de corelație Pearson a fost calculat pentru măsurătorile distanței epidurale care au inclus adâncimea clinică a acului epidural (ND) și ecuația adâncimii epidurale (EDE), ND și EDE anterioară + vedere mediană a planului longitudinal al SUA și ND și EDE anterioară + vedere transversală a planului SUA.
3. Rezultate
Din august 2010 până în iunie 2011, au fost studiați un total de 160 de părinți. Toate femeile care au fost abordate au participat și au finalizat studiul. Datele demografice materne sunt prezentate în Tabelul 1. Au fost 9 eșecuri ale blocului epidural: două au fost eșecuri timpurii (90 de minute). Niciun pacient nu a avut mai mult de un bloc epidural eșuat. A existat o singură puncție durală accidentală (ADP) recunoscută, care a devenit o durere de cap de puncție posturală (PDPH) și a necesitat un plasture epidural terapeutic de sânge (Tabelul 2). Plasarea acului epidural a fost făcută fără reinserții la 92% dintre pacienți, fără a fi necesară redirecționarea acului la 54% dintre pacienți. Numărul maxim de reinserții la același nivel intervertebral a fost de patru, iar 90% din catetere au fost plasate cu succes în trei sau mai puține încercări de redirecționare prin același loc de puncție.
- Plasarea epidurală dificilă la femeile însărcinate obeze și neobeze o revizuire sistematică și
- Refuzarea intervențiilor chirurgicale la pacienții cu obezitate este o cale ortopedică fără ieșire în această săptămână
- Sicriurile obezilor scoțieni sunt prea mari pentru a fi incinerate The Independent The Independent
- Efectul tratamentului cronic cu beta-blocante asupra cheltuielilor energetice de repaus la hipertensivi obezi
- Efectele postului zilnic alternativ și exercițiile fizice asupra metabolismului colesterolului la supraponderali sau obezi