Termeni asociați:
- Duoden
- Cecum
- Ileum
- Jejunum
- Terminal Ileum
- Anastomoza chirurgicală
- Intestin
- Intestinul subtire
- Rect
Descărcați în format PDF
Despre această pagină
Anatomia și fiziologia intestinului subțire
Valva ileocecală
ICV este o caracteristică distinctă a intestinului subțire și funcționează independent de ileon sau colon. Previne conținutul fecal din colon să pătrundă în intestinul subțire și controlează fluxul de conținut din intestinul subțire în colon. Capacitatea ICV de a controla fluxul conținutului digerat poate ajuta, de asemenea, la prevenirea malabsorbției și a diareei. Valva este declanșată de distensie în intestinul subțire sau colon. Dacă ileonul se distinge, valva se va relaxa și va permite trecerea conținutului din intestinul subțire în colon. Cu toate acestea, dacă colonul se distinge, valva se va închide prin creșterea tonusului pentru a preveni trecerea conținutului din colon în ileon.
Structura și controlul neuronal al ICV sunt încă în curs de investigare. Lucrări recente sugerează că valva se formează dintr-o invaginare a ileonului în cec și că plexurile mienterice și submucoase sunt prezente în valvă împreună cu celulele interstițiale ale Cajalului. Trei straturi musculare, un circular extern, circular interior și un strat muscular longitudinal, sunt continue între ileon și cecum, sugerând mecanismul de propagare a activității motorii din ileon în cecum. 4
Caroserie practică în postpartum
Suzanne Yates BA (Hons) DipHSEC MRSS (T) APNT PGCE (PCET), în Sarcină și naștere, 2010
Beneficii
Valva ileocaecală se găsește în cadranul inferior drept al abdomenului. Formează joncțiunea dintre ileonul intestinului subțire și cecul intestinului gros. Reglează și controlează mișcarea deșeurilor lichide de la intestinul subțire la cel gros și este predispus la blocare, adesea în perioada postnatală din cauza modificărilor și a laxității în țesut.
Este o zonă utilă pentru a lucra dacă există probleme cu excesul de secreție de mucus în tot corpul. Se află în imediata apropiere a psoasului și, prin urmare, merită evaluat dacă psoasul este, de asemenea, contractat și, astfel, blocarea supapei, caz în care ar fi indicată o eliberare aici pentru echilibrare.
Controverse în sindromul intestinului scurt
Controversa 5: Ar trebui să se acorde profilaxia bacteriană a excesului de creștere a intestinului subțire?
Sfincterul ileocecal oferă o barieră mecanică în calea migrației bacteriene în intestinul subțire, dar ajută și la reglarea ieșirii de lichide și substanțe nutritive în colon. Mai mult, pierderea acestei bariere funcționale predispune gazda la sepsis bacterian, chiar dacă probabil nu influențează obiectivul final de a obține hrănirea enterală completă. Așa cum am menționat, pierderea sfincterului ileocecal poate duce la creșterea bacteriană a intestinului subțire, o afecțiune asociată cu diaree și malabsorbție a grăsimilor și vitaminelor (B12), ambele rezultând din deconjugarea sării biliare, împreună cu pierderea de lichide, crampele abdominale și leziunile hepatice. 56 Mai mult, creșterea bacteriană a intestinului subțire la bebelușii umani cu SBS este asociată cu inflamația intestinală proximală. 57 Indiferent dacă este cauza sau efectul, copiii cu SBS au activare nespecifică a sistemului imunitar. Într-un studiu, au existat concentrații crescute de receptor II-factor de necroză tumorală solubilă și interleukină-6 în urină și ser la pacienții cu SBS. 58
La copiii cu SBS, se recomandă întreruperea tratamentului cu agenți antimotilitate, cum ar fi loperamida, deoarece tranzitul mai lent poate exacerba creșterea bacteriană a intestinului subțire (SBBO). După ce creșterea bacteriană a fost confirmată prin analiza microbiotei intestinale (duodenale) sau testarea respirației cu hidrogen, tratamentul trebuie început. Goulet și Ruemmele 59 recomandă utilizarea terapiei antimicrobiene intermitente pe bază de metronidazol oral (10 până la 20 mg/kg pe zi), fie singur, fie în asociere cu trimetoprim-sulfametoxazol. Cu toate acestea, organismele anaerobe sunt epuizate la copiii cu SBS și poate fi preferată acoperirea aerobă gram-negativă a tijei folosind medicamente precum amoxicilină-clavulanat sau ciprofloxacină. Răspunsul poate fi evaluat prin îmbunătățirea clinică și toleranța la hrănire. Antibioticele cu spectru larg ar trebui utilizate cu prudență, având în vedere riscul apariției tulpinilor multiresistente de bacterii și efectele asupra florei bacteriene colonice. Din câte știm, nu există studii prospective care să compare rezultatele sugarilor cu SBS tratați cu antibiotice profilactice versus placebo. Durata și programul optim al profilaxiei ciclice cu antibiotice pentru prevenirea SBBO nu au fost abordate în mod formal.
Probioticele sunt microorganisme care, atunci când sunt administrate oral în cantități adecvate, au proprietăți de promovare a sănătății. S-ar putea întreba dacă profilaxia împotriva SBBO cu probiotice pentru a „concura” flora enterică care tinde să producă SBBO ar fi benefică. Cu toate acestea, din cauza rapoartelor, deși rare, ale organismelor probiotice din sângele circulant al pacienților cu SBS, nu recomandăm tratamentul pacienților cu SBS cu probiotice. În plus, există deja lactobacili și bifidobacili abundenți în scaune.
Controverse în sindromul intestinului scurt
Jacqueline J. Wessel, Med RDN, CNSC, CSP, CLE, LD, în gastroenterologie și nutriție (ediția a treia), 2019
Controversa 4: Ar trebui să se acorde profilaxia bacteriană a excesului de creștere a intestinului subțire?
Sfincterul ileocecal oferă o barieră mecanică în calea migrației bacteriene în intestinul subțire, dar ajută și la reglarea ieșirii de lichide și substanțe nutritive în colon. Pierderea sfincterului ileocecal poate duce la creșterea bacteriană a intestinului subțire, o afecțiune asociată cu diaree și malabsorbție de grăsimi și vitamine (B12), ambele rezultând din deconjugarea sării biliare, împreună cu pierderea de lichide, crampe abdominale și leziuni hepatice. 72.73 Mai mult, creșterea bacteriană a intestinului subțire la bebelușii umani cu SBS este asociată cu inflamația intestinală proximală. 74 Indiferent dacă este cauza sau efectul, copiii cu SBS au activare nespecifică a sistemului imunitar. Într-un studiu, au existat concentrații crescute ale receptorului II al factorului de necroză tumorală solubilă (TNF) și ale interleukinei (IL) -6 în urină și ser la pacienții cu SBS și TNF-α crescut comparativ cu controalele sănătoase. 43 Sugarii cu SBBO prezintă un risc mai mare de infecții în sânge și au niveluri mai ridicate de calprotectină fecală. Cole și colab. a văzut o relație inversă între procentul de calorii de nutriție enterală și nivelurile de citokine proinflamatorii, TNF-α, IL-6, IL-8 și IL-ß. 43
Utilizarea agenților antimotilitate, cum ar fi loperamida, nu este întotdeauna recomandată la copiii cu SBS, deoarece tranzitul mai lent poate exacerba SBBO. 75 După confirmarea supra-creșterii bacteriene prin analiza microbiotei intestinale (duodenale) sau testarea respirației cu hidrogen, ar putea fi luat în considerare tratamentul SBBO. Goulet și Ruemmele au recomandat utilizarea terapiei antimicrobiene intermitente bazate pe metronidazol oral, fie singur, fie în asociere cu trimetoprim-sulfametoxazol. 76 Cu toate acestea, organismele anaerobe sunt epuizate la copiii cu SBS și poate fi preferată acoperirea aerobă gram-negativă a tijei cu medicamente, cum ar fi amoxicilină-clavulanat sau ciprofloxacină. Răspunsul poate fi determinat prin evaluarea îmbunătățirii clinice și a toleranței la hrănire. Antibioticele cu spectru larg ar trebui utilizate cu prudență, având în vedere riscul apariției tulpinilor multiresistente de bacterii și efectele asupra florei bacteriene colonice. Nu există studii prospective care să compare rezultatul la sugari cu SBS tratați cu antibiotice profilactice versus placebo. Durata și programul optim al profilaxiei ciclice cu antibiotice pentru prevenirea SBBO nu este standardizat în toate centrele de reabilitare intestinală.
Contrapunctul de luat în considerare atunci când se tratează SBBO este că rapoartele din literatură au sugerat că tratamentul cu SBBO poate să nu ajute și ar putea chiar să înrăutățească lucrurile. În studiul realizat de Piper și colab., Cinci copii cu SBS tratați pentru SBBO au avut o creștere mai slabă și o cantitate mai mică dintr-un subset de bacterii care produc SCFA, A1C care stimulează intestinul să producă citokine antiinflamatorii, cum ar fi IL-10 și celule T reglatoare ale colonului. 52 Aceste celule pot diminua inflamația intestinală. Deficiențele bacteriilor producătoare de SCFA pot duce la mai multă inflamație, absorbție mai slabă și, cu aceasta, o creștere mai slabă.
Galloway și colab. au evaluat imunoglobulinele anti-flagelină (FLiC) și anti-lipopolizaharidă (LPS) la sugari și copii cu SBS, aproximativ jumătate dintre aceștia primind antibiotice ciclate pentru tratamentul SBBO. 77 Anticorpii împotriva LPS și (FLiC) au fost statistic crescute la momentul inițial la cei care au primit un regim profilactic comparativ cu cei care nu au fost regim. În teorie, în timpul tratamentului profilactic împotriva anaerobilor gram-pozitivi care deconjugează acizii biliari și sunt responsabili de malabsorbție, genurile de bacterii din SBBO sunt suprimate. Există apoi probabilitatea ca aerobii gram-negativi rămași să prolifereze și, prin urmare, să se transloce peste bariera mucoasă în circulația portalului. Această rată crescută de translocație ar putea duce la o mai mare activare a căilor inflamatorii și la un număr mai mare de infecții din sânge.
Probioticele sunt microorganisme care, atunci când sunt administrate oral în cantități adecvate, au proprietăți de promovare a sănătății. S-ar putea întreba dacă profilaxia împotriva SBBO cu probiotice pentru a „concura” flora enterică care tinde să producă SBBO ar fi benefică. Cu toate acestea, din cauza rapoartelor, deși rare, ale organismelor probiotice din sângele circulant al pacienților cu SBS și linii centrale, în prezent tratamentul recomandat pentru pacienții cu SBS este cu probiotice. Cu cercetări ulterioare, putem afla tulpini specifice deficitare la sugari și copii cu SBS și să adunăm mai multe informații despre terapia foarte specifică, țintită și eficientă. 52,78
Polipectomie colonoscopică, rezecție mucoasă și disecție submucoasă
Amplasarea în supapa ileocecală (IC).
Poziția în supapa IC nu este neapărat o contraindicație pentru EMR. Într-o serie de cazuri de 53 de pacienți, LST ar putea fi îndepărtate cu succes și intervenția chirurgicală evitată la 43 de pacienți (81%). 81 Recurența a fost observată la 8 pacienți (20%), care a putut fi gestionată endoscopic în toate cazurile. Infiltrarea ileonului și implicarea ambelor buze ale valvei IC au fost asociate cu eșecul EMR. Trebuie subliniat faptul că datele publicate provin dintr-un grup foarte experimentat și că succesul tehnic poate să nu fie generalizat. Mai mult, aceste rezultate subliniază, de asemenea, că documentația localizării ar trebui să fie detaliată și ar trebui să precizeze dacă sunt implicate buzele superioare și inferioare și unghiurile anterioare și posterioare ale valvei IC.
Polipii intestinului gros
SUPAPĂ ILEOCECALĂ LIPOMATOASĂ
Lipoamele adevărate ale valvei ileocecale sunt leziuni bine circumscrise care afectează doar una dintre buzele valvei ileocecale. 343 Mai frecvent, există o creștere difuză a țesutului adipos submucos care determină valva ileocecală să pară similară cu un set de buze proeminente. Aceasta a fost denumită lipohiperplazie, lipomatoză și hipertrofie lipomatoasă a valvei ileocecale. Histologic, biopsiile forcepsului profund prezintă țesut adipos matur în submucoasă, identic cu histologia unui lipom adevărat. În trecut, examinările clismelor de bariu confundau uneori aceste leziuni cu malignitate. 343 În practica actuală, valvele ileocecale lipomatoase sunt rareori prelevate, deoarece aspectul lor la colonoscopie este caracteristic și rareori sunt confundate cu neoplasme. Majoritatea pacienților nu prezintă simptome, dar, în cazuri rare, hiperplazia lipomatoasă poate duce la invaginare recurentă 344 sau apendicită. 345 Mucoasa ileocolonică care se află deasupra valvei proeminente poate prezenta, de asemenea, ulcerații nespecifice legate de traume mecanice.
Într-un studiu de autopsie, 80,4% dintre pacienți au avut un anumit grad de hipertrofie lipomatoasă a valvei ileocecale și s-a considerat că este marcat la 13,7%. 346 Gradul de lipohiperplazie corelat cu o greutate corporală mai mare și cu infiltrarea grasă în ventriculul drept și pancreasul. 346
Posibile capcane la interpretarea CTC
VALVA ILEOCECALĂ
O capcană suplimentară legată de care trebuie să fim conștienți este ceea ce ne referim la o leziune „pseudovalvă”. Acesta este un mare polip sau masă dreaptă care seamănă cu o supapă ileocecală și ar putea fi interpretat greșit pentru a reprezenta această structură normală. Cheile pentru recunoaștere sunt locația și multiplicitatea; atâta timp cât se face întotdeauna identificarea pozitivă a supapei reale, orice altă constatare nu poate fi supapă și, prin urmare, reprezintă altceva. Asemănarea superficială a unor tipuri de cancer pe partea dreaptă și adenoame mari avansate cu valva ileocecală la CTC poate fi izbitoare (Fig. 20-102 și 20-103).
Sindromul intestinului scurt
Valvele intestinale
Importanța valvei ileocecale a fost bine apreciată de cei care îngrijesc pacienții cu SBS. În 1972, Wilmore a documentat că supraviețuirea la sugari cu valvă ileocecală necesita o lungime minimă a intestinului de 15 cm. 87 Cu toate acestea, la acei sugari fără această supapă, lungimea minimă a intestinului necesară pentru supraviețuire a fost semnificativ mai mare (40 cm). Mai recent, s-a raportat că până la 89% dintre pacienții fără supapă ileocecală și cu mai puțin de 40 cm de intestin subțire vor supraviețui. 16 În același raport, s-a remarcat, de asemenea, că o supapă absentă a fost asociată cu o durată semnificativ mai lungă de TPN. Prin urmare, conservarea valvei ileocecale ar trebui să fie un obiectiv major în timpul oricărei intervenții operatorii.
Pe baza importanței observate a valvei ileocecale, au fost descrise mai multe tehnici pentru construirea unor valve similare. Cele mai simple tehnici includ plasarea de suturi sau un guler de teflon extern în jurul circumferinței intestinului. 64 O procedură mai implicată din punct de vedere tehnic implică transformarea unui segment al intestinului pentru a crea un mic intussusceptum și, astfel, tranzit lent (Fig. 86-3). Aspectele mai variabile și mai puțin înțelese ale acestor proceduri se concentrează în jurul lungimii optime a intestinului care urmează a fi înlăturată, precum și a direcției invaginării. Dacă un segment de intestin prea mare este intususceptat, va rezulta o obstrucție funcțională a intestinului.
Experiența clinică cu valvele intestinale este limitată și limitată la serii mici sau rapoarte de caz. S-a demonstrat că crearea unei valve parțial obstructive induce dilatarea intestinală și adaptarea mucoasei. 18 Profitând de această observație, Georgeson și asociații au raportat o serie de pacienți pediatrici cu SBS la care inițial a fost construită o valvă intususceptantă, urmată de o procedură de alungire intestinală la o dată ulterioară. Mai mulți dintre acești pacienți s-au îmbunătățit ca urmare a capacității de a prelungi intestinul anterior nondilat.
Chimiorecepție și motilitate intestinală și colonică
Intestinul gros sau colonul au mai multe regiuni anatomice
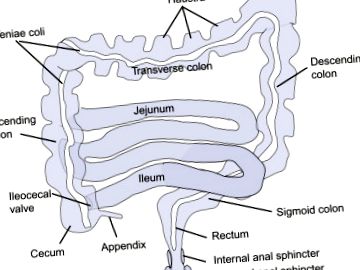
Colonul începe la sfincterul ileocecal și este format din cecum, colon ascendent, colon transvers, si colonul descendent. Acest lucru duce la colon sigmoid si rect (vezi Figura 8.3.9). Ca și în restul sistemului gastro-intestinal, colonul conține un strat interior de mușchi circular care este continuu de la cecum la rect. În rect, acest strat se îngroașă pentru a forma sfincterul anal intern. Contracția mușchiului circular împarte colonul în segmente numite haustra, dând aspectul unui lanț de saci mici. Hustra dispare în timpul contracțiilor unui segment și locațiile lor se schimbă. Straturile musculare longitudinale exterioare nu sunt continue în intestinul gros, ci formează în schimb trei benzi numite teniae coli care parcurg lungimea intestinului gros. Acestea devin continue și devin continue la nivelul rectului. Sfincterul anal extern este format din mușchi striat care se suprapune sfincterului anal intern. Acest mușchi oferă control voluntar asupra defecației.
Figura 8.3.9. Anatomia grosieră a intestinului gros.
- Agricultura insectelor - o prezentare generală Subiecte ScienceDirect
- MacConkey Agar - o prezentare generală a subiectelor ScienceDirect
- Maltodextrina - o prezentare generală a subiectelor ScienceDirect
- Lactobacillus - o prezentare generală Subiecte ScienceDirect
- Stomatita herpetică - o prezentare generală Subiecte ScienceDirect