Jing Huang
un Departament de Radiologie și Științe Imagistice, Școala de Medicină a Universității Emory, Atlanta, Georgia 30322, SUA
Liya Wang
un Departament de Radiologie și Științe Imagistice, Școala de Medicină a Universității Emory, Atlanta, Georgia 30322, SUA
Xiaodong Zhong
b MR R&D Collaborations, Siemens Healthcare, Atlanta, Georgia 30322, SUA
Yuancheng Li
un Departament de Radiologie și Științe Imagistice, Școala de Medicină a Universității Emory, Atlanta, Georgia 30322, SUA
Lily Yang
c Departamentul de Chirurgie, Școala de Medicină a Universității Emory, Atlanta, Georgia 30322, SUA
Hui Mao
un Departament de Radiologie și Științe Imagistice, Școala de Medicină a Universității Emory, Atlanta, Georgia 30322, SUA
Date asociate
Abstract
Nanoparticulele magnetice de oxid de fier ultrafin sub 5 nm acoperite cu oligozaharide (SIO) cu efect dublu de îmbunătățire a contrastului ponderat T1-T2 și clearance-ul rapid au fost dezvoltate ca agent de contrast pentru imagistica prin rezonanță magnetică (RMN). Solubilitatea excelentă în apă, biocompatibilitatea și stabilitatea ridicată a unor astfel de nanoparticule SIO sub-5 nm au fost obținute prin utilizarea metodei de acoperire „in-situ”, care permite oligozaharidelor care formează glucoză direct pe suprafața nanocristalelor de oxid de fier hidrofob. Nanoparticulele SIO ultrafine raportate prezintă o relaxare longitudinală (r1) de 4,1 mM −1 s −1 și un raport r1/r2 de 0,25 la 3 T (intensitatea câmpului clinic), făcând îmbunătățirea T1 îmbunătățită sau contrastul „mai luminos” în RMN ponderat T1 pe lângă contrastul tipic T2 sau „întunecarea” nanoparticulelor convenționale de oxid de fier. Un astfel de efect de contrast dublu poate fi demonstrat în imagistica hepatică cu contrast „întunecat” T2 în parenchimul hepatic, dar contrast „luminos” T1 în vasculatura hepatică. Mai important, această nouă clasă de nanoparticule de oxid de fier sub-nm de 5 nm a prezentat un clearance corporal mult mai rapid decât cele cu dimensiuni mai mari, promițând o siguranță mai bună pentru aplicațiile clinice.
1. Introducere
Până în prezent, s-au dezvoltat diverse forme de IONP pentru aplicații RMN, dintre care doar doi agenți (Feridex®, Resovist®) formulați cu acoperire cu dextran au fost aprobați de FDA pentru utilizări clinice. 12 Ambele au o dimensiune medie a miezului de peste 5 nm și o dimensiune totală de 60-150 nm. 5, 13 Particulele cu o astfel de dimensiune totală sunt prinse rapid în organele sistemului retoculoendotelic (RES) și pot dura câteva săptămâni sau chiar luni pentru a fi degradate și eliminate din corp. 14 Clearance-ul lent nu numai că provoacă îngrijorare cu privire la efectele secundare pe termen lung ale unor astfel de IONP-uri, ci și le limitează să fie utilizate în mod repetat în studiile de imagistică longitudinală. Mai mult, dimensiunea totală mai mare împiedică IONP-urile să mențină proprietățile de îmbunătățire a contrastului T1. 15, 16
Aici raportăm o nouă clasă de nanoparticule de oxid de fier acoperite cu oligozaharidă ultrafină (SIO-3, dimensiunea medie a miezului de 3,5 nm) preparate prin polimerizarea in-situ a glucozei pe suprafața particulelor. SIO-3 sub 5 nm raportat este extrem de stabil în soluția apoasă și prezintă un raport r1/r2 îmbunătățit față de IONP cu dimensiuni globale mai mari, ceea ce duce la îmbunătățirea excelentă a contrastului RMN T1 și efectul de contrast dublu T1-T2 dublu pentru aplicații noi. În plus, SIO-3 a prezentat un timp de eliminare a corpului redus cu secreție renală parțială, comparativ cu IONP cu dimensiuni mai mari, prin urmare, promite să abordeze îngrijorarea durabilă a unei posibile toxicități pe termen lung asociată cu IONP.
2. Secțiunea experimentală
Sinteza nanoparticulelor de oxid de fier hidrofob (IONP)
Nanoparticulele hidrofobe de oxid de fier au fost sintetizate prin termodescompunere. Pe scurt, oleatul de fier (III) a fost preparat mai întâi printr-o metodă publicată modificată. 20 De obicei, 4,04 g nitridură ferică (10 mmol) și 9,13 g oleat de sodiu (30 mmol) au fost dizolvate în solvent amestecat cu 40 ml apă distilată, 50 ml hexan și 10 ml etanol absolut. Amestecul de oleat de fier a fost agitat la temperatura camerei timp de 4 ore și apoi a fost ținut liniștit peste noapte. Stratul de hexan roșu-maroniu rezultat a fost utilizat ca sursă de fier pentru termodescompunere. Într-o reacție tipică, 5 ml de oleat de fier au fost amestecați cu 5 ml de 1-octadecen la temperatura camerei și s-au degazat cu argon ultra-înalt timp de 20 min. După evaporarea hexanului la 70 ° C, amestecul de reacție a fost încălzit la 320 ° C cu o rată de încălzire de 0,6 ° C · s -1. Timpul de reacție a fost ajustat pentru a controla dimensiunea IONP-urilor, care a fost de aproximativ 5 min pentru IONP-uri cu o dimensiune a miezului de 3,5 nm și s-a reîncălzit aproximativ 10, 15, 20, 30 min pentru IONP-uri cu 4,8, 9,9, 15,6, 19,9 nm mărimea. După răcire la temperatura camerei, s-a adăugat etanol pentru a precipita nanoparticulele. Produsele au fost colectate prin centrifugare și spălate cu hexan și etanol de mai multe ori.
Sinteza nanoparticulelor de oxid de fier acoperit cu oligozaharidă (SIO)
Acoperirea cu oligozaharide a fost introdusă pe IONP-uri hidrofobe prin polimerizare in situ. Pe scurt, IONP-urile acoperite cu acid oleic au fost redispersate în cloroform după purificare cu centrifugare și adăugate cu grijă în picătură în soluția de glucoză preîncălzită în dimetilformamidă (DMF). Amestecul a fost încălzit la 120 ° C și menținut la această temperatură timp de 2,5 ore. După răcire la temperatura camerei, produsul a fost precipitat prin adăugarea de etanol. Precipitatul a fost spălat și centrifugat de mai multe ori. Produsul final a fost colectat și redispersat în apă distilată pentru alte caracterizări și aplicații.
Caracterizări ale nanoparticulelor SIO
Morfologia și dimensiunea nanoparticulelor SIO au fost studiate folosind un microscop electronic cu transmisie (TEM, Hitachi H-7500, tensiune de accelerare 75 kV). De obicei, probele TEM sunt preparate prin aruncarea soluțiilor de nanoparticule diluate pe rețeaua de cupru acoperită cu carbon și uscate la aer. Mărimea hidrodinamică și încărcăturile de suprafață ale nanoparticulelor din soluția apoasă au fost evaluate utilizând un instrument de împrăștiere dinamică a luminii (DLS) (Malvern Zeta Sizer Nano S-90) echipat cu un laser He-Ne de 22 mW care funcționează la 632,8 nm. Analiza structurală a nanoparticulelor SIO a fost efectuată prin difracție cu raze X în pulbere (XRD, difractometru în pulbere Bruker D8 DIFFRAC, Co Kα). Pentru studierea acoperirii cu nanoparticule, spectrele de spectroscopie în infraroșu cu transformată Fourier (FTIR) au fost colectate pe un spectrometru PerkinElmer Spectrum 100 FT-IR (Bucks, Marea Britanie). Spectrele de absorbție UV-vis au fost obținute cu un spectrofotometru de scanare (Shimadzu UV-2401PC) cu o lățime a fantei de 1,0 nm.
Măsurarea timpilor de relaxare și calcularea relaxivităților
Pentru a evalua contrastul RMN, îmbunătățirea capacității, soluțiile SIO cu concentrații diferite au fost examinate cu un scaner RMN 3T (Magnetom Tim Trio, Siemens Medical Solutions, Erlangen, Germania) folosind secvențe de ecou de spin rapid ponderate T1 și T2, secvență de ecou de turbo spin recuperare recuperare și secvența de ecou de rotire ponderată T2 cu ecou multiplu. Agentul de contrast pentru îmbunătățirea T1 comercial Multihance® (Gd-BOPTA) a fost folosit pentru a compara efectul de îmbunătățire a contrastului RMN. Fiecare probă a fost preparată cu concentrații de Fe sau Gd variind de la 0,004 la 40 mM. Pentru a măsura timpul de relaxare longitudinal T1, a fost utilizată o secvență de recuperare a inversării turbo spin echo (TSE) cu lungimea trenului de ecou (ETL) de 3, timpul de ecou (TE) de 13 ms și timpul de repetare (TR) de 1500 ms pentru a obține imagini la timpi de inversiune diferiți (TI) de 23, 46, 92, 184, 368, 650, 850, 1100 și, respectiv, 1400 ms. Pentru a măsura timpul de relaxare transversal T2, a fost utilizată o secvență de ecou de spin multi-ecou cu TR de 2400 ms și 15 TE, începând de la 11 ms cu trepte de 11 ms. Intensitatea semnalului (SI) a fiecărei regiuni de interes (ROI) la diferite TI sau TE a fost măsurată pentru eșantioanele fiecărei concentrații.
RMN de șoareci administrat cu nanoparticule SIO
Toate experimentele pe animale au fost efectuate în urma unui protocol aprobat de Comitetul instituțional de îngrijire și utilizare a animalelor (IACUC). Șoarecii BALB/c au fost anesteziați prin injectarea intraperitoneală a unui amestec de ketamină-xilazină (95: 5 mg/kg). Soluția salină SIO-3 diluată a fost administrată intravenos la o doză de 2,5 și 10 mg Fe per kg de greutate corporală a șoarecelui. Pentru comparație, Gd-BOPTA și SIO-20 (dimensiunea miezului de 20 nm) au fost injectate la doza de 2,5 mg/kg și respectiv 0,2 mmol/kg. Au fost obținute imagini de ecou de spin ponderate T1 suprimate cu grăsime pentru a investiga schimbările de contrast din diferite organe și structuri anatomice, cum ar fi ficatul, rinichii și artera iliacă, în diferite momente de timp. Parametrii de imagine au inclus: TR) = 724 ms, TE = 10 ms, matrice = 320 × 134, câmp vizual (FOV) = 120 × 60 mm 2, flip angle = 70 și grosimea feliei = 1,00 mm. Raportul semnal-zgomot (SNR) a fost calculat conform ecuației: SNR = SImean/SDnoise. Îmbunătățirea relativă a contrastului la diferite puncte de timp a fost definită ca scăderea semnalului ΔSNR = (SNRpre - SNRpost)/SNRpre. Raportul contrast-zgomot dintre parenchimul hepatic și vasculatură a fost calculat ca CNR = (SNRpost (vasculatură) −SNRpost (parenchim hepatic))/SNRpre (parenchim hepatic).
Clearance-ul corporal al nanoparticulelor SIO la șoareci
3. Rezultate si discutii
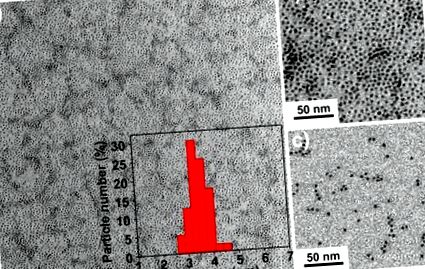
(a) Imagini TEM cu mărire mică și (b) cu mărire mare a IONP-urilor hidrofobe de 3,5 nm (IO-3). Inserția lui (a) este distribuția mărimii după 100 de particule măsurate. (c) imagini TEM ale IONP-urilor hidrofile acoperite cu oligozaharide (SIO-3).
Modelele de difracție cu raze X în pulbere (XRD) ale IO-3 și SIO-3 au fost prezentate în Figura 2a. Au fost observate vârfuri de difracție lărgite pentru ambele probe datorită cristalelor de dimensiuni nano ultrfine. Vârfurile de difracție lărgite au devenit mai clare după aplicarea acoperirii, datorită rearanjării suprafeței înclinate în timpul procesului de încălzire. 31 Cu toate acestea, mărimea bobului s-a schimbat puțin în funcție de jumătatea lățimii vârfurilor de difracție. Ambele vârfuri XRD ale IONP-urilor înainte și după acoperire au fost atribuite structurii magnetitei spinării sau maghemitei. Formarea acoperirii oligozaharidelor pe suprafața IONP-urilor a fost confirmată în continuare prin spectroscopie în infraroșu cu transformată Fourier (FTIR) (Figura 2b). Benzile caracteristice ale acidului oleic, inclusiv întinderea CH (2923, 2852 cm -1), îndoirea CH2 (1457, 1375 cm -1) și întinderea C = O (1540 cm -1), au devenit slăbite după ce au fost înlocuite cu oligozaharide pe suprafaţă. Banda ascuțită C = C apărută la 1653 cm -1 a indicat prezența structurilor aromatice din oligozaharide pe suprafața particulelor. 32, 33
(a) Modelul pulberii XRD și (b) spectrele FTIR ale IO-3 și SIO-3. (c) Monitorizarea stadiului de reacție prin emisie de FL. Inserția din (c) este fotografii ale amestecului de reacție colectat la un timp de reacție diferit sub lumină normală (stânga) și lumină UV de 365 nm (dreapta). (d) Tranziția fazei de solvent a IONP-urilor de la hexanul în fază organică la soluția apoasă în timp.
Trebuie remarcat faptul că temperatura pe care am folosit-o pentru polimerizarea in situ a glucozei pe suprafața nanoparticulelor este mult mai mică (
Efectele de amplificare a contrastului RMN ale SIO au fost investigate la câmpul magnetic relevant clinic (3 T). Figura 3a și b prezintă imagini MR ponderate T1 și T2 ale soluțiilor apoase SIO cu concentrații diferite de Fe. SIO-3 prezintă cea mai mare îmbunătățire a contrastului T1, în timp ce SIO-20 prezintă cea mai mare îmbunătățire a contrastului T2. Această observație este de așteptat, deoarece SIO-3 are cel mai mare raport suprafață-volum datorită dimensiunii ultrafine. Pentru agenții de contrast nanoparticulate, se consideră că îmbunătățirea contrastului T1 este contribuită în principal de relaxarea sferei interioare, care provine din coordonarea directă dintre moleculele de apă și ionii magnetici de pe suprafața particulelor. 5, 27, 39 Raport ridicat suprafață-volum în combinație strat de acoperire hidratat subțire de oligozaharide pentru SIO-3 ar facilita interacțiunea moleculelor de apă cu stratul interior.
(a) Imagini MR ponderate T1 și (b) T2 ale soluțiilor SIO cu concentrații diferite și valoarea (c) r1 și d) r2 corespunzătoare se modifică cu dimensiunea particulelor.
Pentru a evalua în continuare eficiența îmbunătățirii contrastului și comportamentul SIO-urilor, am calculat un profil de intensitate a semnalului unui agent de contrast (Figura 4a, b) folosind ecuația care descrie evoluția intensității semnalului (SI) din secvența de ecou de spin ponderată T1. Având în vedere aceeași concentrație de Fe (adică 1 mM) și parametrii de achiziție a imaginii (adică TR = 500 ms, TE = 12 ms) utilizați în mod obișnuit pentru RMN echo de spin ponderat T1, cel mai mare contrast T1, adică cel mai luminos semnal, pentru un dat r1 poate fi obținut numai când r2 ajunge la zero. Mai mult, SI este mai sensibil la schimbarea în r2 decât în r1 pentru agenții de contrast cu un r1 mai mare de 4,5 mM −1 s −1. De exemplu, deși SIO-3 are o r1 mai mică, are o eficiență de îmbunătățire T1 mult mai mare decât SIO-20 din cauza unei reduceri mai accentuate a r2.
(a) Predicția SI în imaginile MR ponderate T1 determinate de r1 și r2 și (b) imaginea de sus. (c) SI maxim pentru fiecare soluție SIO legată de raportul r1/r2. (d) raportul r1/r2 se modifică cu dimensiunile hidrodinamice.
Studiile timpurii au sugerat că raportul r1/r2 poate dicta proprietățile de îmbunătățire a contrastului T1 ale nanoprobelor magnetice. 5, 16 Un SI maxim crescut în imaginile MR ponderate T1 a fost observat cu un raport r1/r2 crescător, așa cum se arată în Figura 4c. S-a studiat teoretic că rapoartele r1/r2 cresc monoton față de timpul de difuzie translațional τD, 24 care este legat de raza IONP-urilor, permeabilitatea la apă a stratului de acoperire și grosimea stratului de acoperire. În mod surprinzător, SIO-3 are cel mai mare raport r1/r2 de 0,25 în comparație cu omologii în diferite dimensiuni (Figura 4d).
Deoarece majoritatea agenților de contrast nanoparticulati T1 raportați până acum au un r1 mai mare de 4,5 mM -1 -1 s -1, dar și r2 substanțial ridicat, 16 o strategie alternativă pentru dezvoltarea viitoare a agenților de contrast RMN ponderat T1 pe bază de nanoparticule magnetice este atenuarea r2 în timp ce încercând să crească r1. De exemplu, cationii magnetici cu electroni nepereche (de exemplu, Mn 2+, Gd 3+) au fost introduși în nanostructurile de oxid de fier pentru a crește r1, astfel pentru a realiza îmbunătățirea contrastului pozitiv. 6, 42, 44 Indiferent de toxicitatea metalelor, dopajul Gd poate fi considerat un mod mai eficient din cauza creșterii mai ușoare a r2. 6 Mai mult, reducerea r2 poate permite creșterea concentrației IONP pentru îmbunătățirea T1 SI, care este adesea compromisă la concentrațiile mai mari de IONP.
Imagini MR ponderate T1 ponderate ale grăsimilor la șoareci înainte și după administrarea SIO-3 la o doză de 10 mg/kg. Ameliorarea pozitivă a contrastului a fost observată în inimă, splină (cerc punctat roșu), rinichi (cerc punctat verde) și vase hepatice.
- Articol complet Evaluarea termodinamică pentru reducerea particulelor de minereu de oxid de fier într-un nivel ridicat
- Poli (oxid de etilenă) reticulat pentru sisteme de eliberare a medicamentelor - Panayotov - 1996 - Macromolecular
- Căderea părului, cercuri întunecate sub ochi, unghii peeling de care aveți nevoie de fier - Soluții inteligente de Lorna
- China Nou detașabil Hula Hoop de masaj cu terapie magnetică cu cosuri - China Masaj Hula Hoop preț
- Doppelherz fier activ vital - Sănătate - Sănătate; Frumuseţe