Pablo Kizelsztein
1 Centrul de biotehnologie, Universitatea Rutgers, New Brunswick, New Jersey; și 2 Pennington Biomedical Research Center, Baton Rouge, Louisiana
Dmitry Govorko
1 Centrul de biotehnologie, Universitatea Rutgers, New Brunswick, New Jersey; și 2 Pennington Biomedical Research Center, Baton Rouge, Louisiana
Slavko Komarnytsky
1 Centrul de biotehnologie, Universitatea Rutgers, New Brunswick, New Jersey; și 2 Pennington Biomedical Research Center, Baton Rouge, Louisiana
Alysa Evans
1 Centrul de biotehnologie, Universitatea Rutgers, New Brunswick, New Jersey; și 2 Pennington Biomedical Research Center, Baton Rouge, Louisiana
Zhong Wang
1 Centrul de biotehnologie, Universitatea Rutgers, New Brunswick, New Jersey; și 2 Pennington Biomedical Research Center, Baton Rouge, Louisiana
William T. Cefalu
1 Centrul de biotehnologie, Universitatea Rutgers, New Brunswick, New Jersey; și 2 Pennington Biomedical Research Center, Baton Rouge, Louisiana
Ilya Raskin
1 Centrul de biotehnologie, Universitatea Rutgers, New Brunswick, New Jersey; și 2 Pennington Biomedical Research Center, Baton Rouge, Louisiana
Abstract
Hormonul steroid 20-hidroxidecisonă (20HE) este o moleculă de semnalizare esențială care modulează răspunsul de mutare la insecte și poate funcționa ca un factor anabolic putativ la animalele vertebrate, deși nu a fost identificat niciun receptor 20HE de mamifer. Aici arătăm că în cultura celulară H4IIE, tratamentul cu 20HE a scăzut expresia fosfoenolpiruvatului carboxicinazei (PEPCK) și glucozei-6-fosfatazei (G6Pazei), a redus producția de glucoză și a indus fosforilarea Akt2 sensibilă la inhibitorul specific al căii fosfoinositidă-3 kinază LY- 294002. Administrarea zilnică orală de 20HE (10 mg/kg timp de 13 săptămâni) ameliorează obezitatea și rezistența la insulină la șoarecii C57BL/6J hrăniți cu o dietă bogată în grăsimi și a produs o scădere semnificativă a creșterii în greutate corporală și a masei de grăsime corporală în comparație cu animalele netratate, după cum a demonstrat analiza absorptiometriei cu raze X cu energie duala. În plus, nivelurile de insulină plasmatică și toleranța la glucoză au fost semnificativ reduse prin tratamentul cu 20HE. Aceste modificări au fost însoțite de expresia hepatică redusă a PEPCK și G6Pase și creșterea producției de adiponectină de către țesutul de grăsime viscerală. Aceste studii demonstrează efectele anti-obezitate și anti-diabetice ale 20HE și încep să elucideze țintele sale celulare putative atât in vitro, cât și in vivo.
ecdisteroizii sunt steroizi polihidroxilați prezenți în plante și nevertebrate. Până în prezent, aproape 120 de ecdisteroizi au fost caracterizați structural (18). Structura chimică a ecdisteroizilor se bazează pe scheletul colesterolului C-27; cu toate acestea, diferă de steroizii vertebratelor prin polaritatea și volumul lor. Unul dintre cele mai frecvente și mai abundente ecdisteroizi, 20-hidroxidizona (20HE), se găsește în multe plante, inclusiv specii cultivate pe scară largă, cum ar fi Spinacia oleracea (spanac) (29). La insecte, ecdisteroizii sunt implicați preponderent în reglarea năpârlirii și metamorfozei, în timp ce la plante pot contribui la descurajarea prădătorilor de nevertebrate (9).
Puține informații sunt disponibile cu privire la rolurile fiziologice ale ecdisteroizilor la animalele vertebrate. În plus față de efectele lor anabolice (7, 8), s-a raportat că ecdisteroizii au proprietăți imunomodulatoare (7), hepatoprotectoare (30), antiaritmice (21) și de scădere a colesterolului (26). Există, de asemenea, unele dovezi care arată că 20HE afectează metabolismul glucozei in vivo. Pre-tratamentul cu 20HE a redus hiperglicemia asociată cu administrarea fie de glucagon, fie de aloxan (25). Mai mult, extractul bogat în ecdisteroizi din Ajuga turkestanica administrat pe cale orală (5 mg/kg) a fost mai eficient în reducerea hiperglicemiei într-un model de diabet indus de aloxan la șobolani decât medicamentul de referință manilil fără a provoca un efect hipoglicemiant la animalele normale (22).
Un aspect important al ecdisteroizilor este toxicitatea lor scăzută la mamifere. Doza letală mediană (LD50) de 20HE la rozătoare este de 6,4 g/kg corp greutate (pentru injecție intraperitoneală) și este> 9 g/kg corp greutate atunci când este administrată oral (25).
MATERIALE ȘI METODE
Produse chimice.
Ecdysterone a fost achiziționat de la Bosche Scientific (New Brunswick, NJ). Dexametazona, 8- (4-clorfeniltio) -CAMP (AMPc), lactat de sodiu și piruvat de sodiu au fost achiziționate de la Sigma Chemicals (St. Louis, MO). Insulina umană (Humulin) a fost cumpărată de la Eli Lilly (Indianapolis, IN) și compusul C de la EMD Biosciences (San Diego, CA); mAbs de iepure fosfo-Akt2 și Akt2 au fost achiziționate de la Cell Signaling Technology (Danvers, MA). Toate celelalte substanțe chimice, inclusiv mediile de cultură celulară, au fost obținute de la Invitrogen (Carlsbad, CA). Reactivii și enzimele utilizate pentru RT-PCR au fost obținute de la Stratagene (La Jolla, CA) și Applied Biosystems (Foster City, CA). Linia celulară H4IIE (CRL-1548) a fost obținută din colecția American Type Culture Collection (Manassas, VA).
Cultura și tratamentul celular.
Celulele de hepatom H4IIE au fost cultivate în plăci de cultură tisulară cu 24 de godeuri (Greiner Bio One, Monroe, NC) și crescute până aproape de confluență în mediul Eagle modificat al lui Dulbecco conținând 2,5% (vol/vol) ser de vițel nou-născut și 2,5%) ser fetal de vițel . Celulele au fost tratate timp de 8 ore cu 500 nM dexametazonă și 0,1 mM 8-CTP-cAMP (Dex-cAMP) pentru a induce expresia genei fosfoenolpiruvat carboxicinazei (PEPCK) și glucozei-6-fosfatazei (G6Pazei) împreună cu diferite concentrații de 20HE nM insulină. Au fost alocate trei godeuri pentru fiecare tratament, inclusiv controlul negativ (celule netratate). Pentru teste inhibitorii, celulele au fost pretratate timp de 30 de minute cu 20 μM LY-294002 sau 40 μM compus C așa cum este specificat, spălate cu soluție salină tamponată cu fosfat și incubate timp de încă 7 ore cu Dex-cAMP împreună cu concentrații diferite de 20HE, sau 10 nM insulină.
Analiza producției de glucoză.
Celulele de hepatom de șobolan H4IIE au fost înfometate cu ser peste noapte în tampon de producere a glucozei (mediu esențial modificat Dulbecco fără glucoză, pH 7,4, conținând 20 mM lactat de sodiu și 2 mM piruvat de sodiu fără fenol roșu) și tratate timp de 8 ore cu Dex-cAMP în prezență sau absența insulinei 10 nM sau concentrații diferite de 20HE timp de 8 ore. La sfârșitul incubației, s-au luat 0,5 ml mediu pentru a măsura concentrația de glucoză în mediul de cultură folosind kitul de testare a glucozei Amplex Red (Invitrogen). Corecțiile pentru numărul de celule au fost făcute pe baza concentrației de proteine măsurată folosind kitul de testare a proteinelor BCA (Pierce Biotechnology, Rockford, IL).
Extracția totală de ARN, purificarea și sinteza ADNc.
ARN-ul total a fost extras din celule H4IIE sau țesuturi murine conservate cu azot lichid folosind reactivul Trizol (Invitrogen) urmând instrucțiunile producătorului. ARN-ul a fost cuantificat spectrofotometric prin măsurători de absorbanță la 260 și 280 nm utilizând sistemul NanoDrop (NanoDrop Technologies, Wilmington, DE). Calitatea ARN-ului a fost evaluată prin separare în electroforeză pe gel. Pentru a elimina orice urmă de contaminare a ADN-ului, ARN-ul a fost apoi tratat cu DNază I (Invitrogen) urmând liniile directoare ale producătorului. ADNc-urile au fost sintetizate folosind 2,5 μg de ARN pentru fiecare probă, utilizând transcriptaza inversă Stratascript (Stratagene) urmând protocolul producătorului.
Analiza PCR cantitativă a celulelor de hepatom de șobolan H4IIE.
Analiza qPCR a țesuturilor murine.
Testul activității AMPKα1 și -α2.
Activitatea AMPK a fost testată așa cum s-a descris anterior (12). Pe scurt, AMPK a fost imunoprecipitat din 200 μg de lizat celular H4IIE folosind anticorpi anti-AMPKα1 (Upstate Biotechnology, Lake Placid, NY) sau -α2 (Santa Cruz Biotechnology, Santa Cruz, CA) în 500 μl de tampon A (50 mM Tris · HCI, pH 7,4, 150 mM NaCI, 50 mM NaF, 5 mM pirofosfat de sodiu, 1 mM EDTA, 1 mM EGTA, 1 mM DTT, 0,1 mM benzamidină, 1 mM fenilmetilsulfonil fluor, 5 μg/ml aproptin) la 4 ° C pentru 2 ore. Imunocomplexele au fost spălate cu tampon A de trei ori, tampon B conținând 0,5 M NaCI și 62,5 mM NaF o dată, și apoi tampon de reacție (50 mM HEPES, pH 7,4, 1 mM DTT) de trei ori. Activitatea AMPK a imunocomplexelor a fost determinată prin fosforilarea peptidei SAMS în tamponul de reacție conținând SAMS 0,25 mM, 5 mM MgCl2 și 10 μCi de [r- 32 P] ATP timp de 10 min la 30 ° C cu sau fără stimulare AMP 200 μM. Reacția a fost terminată prin depistarea amestecurilor de reacție pe hârtie de filtru P81 și clătire în acid fosforic 1% (vol/vol) cu agitare ușoară pentru a îndepărta ATP-ul liber. Substratul fosforilat a fost măsurat prin numărarea scintilației.
Analiza Western blot.
Celulele H4IIE au fost cultivate așa cum s-a descris mai sus, iar extractele de celule întregi au fost preparate în tampon de liză rece cu gheață [62,5 mM Tris · HCI (pH 6,8), 2% în greutate/vol SDS, 10% glicerol, 50 mM DTT, 0,01% în greutate/vol. albastru de bromofenol] și centrifugat la 12.000 g timp de 20 minute la 4 ° C. Cantități egale de proteine (50 μg) din supernatante au fost separate pe geluri de poliacrilamidă SDS 10% și șterse pe membrana nitrocelulozei. Analiza Western blot a fost efectuată cu anticorpi monoclonali fosfo-Akt (Ser 473) conform instrucțiunilor producătorului (Cell Signaling Technology, Danvers, MA). După ce au fost spălate, petele au fost incubate cu un anticorp secundar marcat cu peroxidază anti-iepure și vizualizate folosind reactivul ECL Western Blotting Detection (GE Healthcare, Piscataway, NJ). După ce au fost dezbrăcate, petele au fost sondate cu anticorpi Akt2 (5B5) pentru a vizualiza Akt-ul total (controlul încărcării).
Experimente pe animale.
Toate experimentele pe animale au fost efectuate conform procedurilor aprobate de Comitetul instituțional de îngrijire și utilizare a animalelor Rutgers. Șoarecii masculi C57BL/6J de șase săptămâni au fost obținuți de la Laboratorul Jackson (Bar Harbor, ME) și au fost menținuți fie pe o dietă cu conținut scăzut de grăsimi (LFD; n = 10) conținând 10% calorii derivate din grăsimi (D12450B; Research Diets, New Brunswick, NJ) sau un HFD (n = 10) conținând 60% calorii derivate din grăsimi (D12492, Research Diets) cu cicluri de lumină și întuneric de 12 ore.
Animalele HFD au fost randomizate în continuare în două grupuri. Grupul de control (n = 10) a fost gavat zilnic cu o soluție vehicul singură (10% DMSO în ulei de porumb), iar un grup de tratament (n = 10) a fost gavat cu 10 mg/kg corp greutate 20HE timp de 13 săptămâni. Pentru a monitoriza creșterea și pierderea greutății corporale, animalele au fost cântărite săptămânal pe durata experimentului. Temperatura intrarectală a șoarecilor a fost măsurată săptămânal folosind un termometru conținând o sondă (Oakton Instruments, Vernon Hills, IL). Concentrațiile de glucoză plasmatică au fost măsurate la săptămânile 4, 9, 10, 11 și 12 în probele de sânge din vena submandibulară folosind un glucometru (Lifescan, Johnson și Johnson, NJ). Concentrațiile plasmatice de insulină și adiponectină au fost determinate în săptămâna 13 prin setul ELISA de insulină de șobolan/șoarece (Millipore, Billerica, MA) și setul ELISA de adiponectină (Otsuka Phamaceuticals, Toyko, Japonia), respectiv.
Pentru a efectua testul de toleranță la glucoză în săptămâna 13 a experimentului, atât șoarecii LFD, cât și șoarecii HFD au fost postiti peste noapte (16 ore) și injectați intraperitoneal cu 1,5 g/kg soluție de glucoză. Nivelurile de glucoză plasmatică au fost măsurate imediat înainte și la 30, 60 și 120 de minute după provocarea glucozei. La sfârșitul studiului, șoarecii au fost uciși și cantități egale de ficat și grăsime viscerală au fost eliminate. Masa de grăsime și țesutul slab au fost determinate utilizând analiza de absorptiometrie cu raze X cu energie duală (DEXA) pe echipamentul PIXImus (Lunar, Madison, WI) așa cum este descris în altă parte (27). Procentul de țesut adipos a fost calculat după cum urmează:% grăsime corporală = (masa grasă/greutatea totală a corpului) × 100, unde greutatea corporală totală a fost suma masei slabe și a grăsimii pentru fiecare animal. Raportul dintre masa adipoasă și masa slabă pentru fiecare animal a fost calculat prin împărțirea masei grase la masa slabă.
REZULTATE
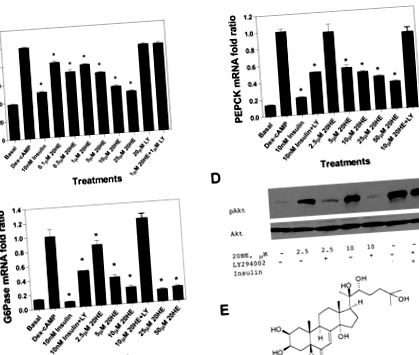
20HE modulează metabolismul glucozei în celulele de hepatom de șobolan.
Producția de glucoză ca răspuns la 20HE a fost testată pe celule de hepatom de șobolan H4IIE incubate în mediu care conține piruvat și lactat ca substraturi pentru gluconeogeneză.
Datele reprezintă media a 2 experimente diferite ± SE. Concentrația de insulină este exprimată ca ng/ml, iar concentrațiile de adiponectină sunt ng · μl -1 -1 g grăsime corporală -1 și ng · μl -1 -1 g corp greutate -1. LFD, dieta saraca in grasimi; HFD, dietă bogată în grăsimi; 20HE, 20-hidroxidizona.
Medicamentele biguanidine de origine vegetală, cum ar fi metformina, exercită o reglare descendentă independentă de PI3K a expresiei genei PEPCK bazale în hepatocite (39) printr-un mecanism dependent de AMPK. Această cale duce la suprimarea insulinei independentă a gluconeogenezei hepatice prin fosforilare și sechestrare citoplasmatică a țintei mamifere a coactivatorului transcripțional al complexului 2 de rapamicină (17). 20HE a fost capabil să crească activitatea bazală a subunității catalitice AMPKα1 exprimate omniprezent, dar nu a avut niciun efect asupra subunității catalitice AMPKα2 hepatice specifice (Fig. 2). Compusul C, un inhibitor ATP-competitiv al AMPK (26), nu a inversat efectele 20HE asupra expresiei genei PEPCK stimulate de Dex-cAMP în celulele H4IIE (datele nu sunt prezentate). Luate împreună, aceste date sugerează că activarea independentă de PI3K a AMPKα1 de către 20HE joacă un rol minor în reglarea enzimelor gluconeogene și a producției de glucoză hepatică.
În concluzie, rezultatele noastre aruncă o nouă lumină asupra efectului hipoglicemiant al 20HE in vitro și in vivo și indică faptul că acest efect poate fi exercitat prin reglarea dependentă de PI3K a activității enzimei gluconeogene. Și mai important, datele sugerează că administrarea zilnică a 20HE poate preveni obezitatea, rezistența la insulină și hiperglicemia asociată la animale prin scăderea depozitelor de grăsime, reglarea în sus a expresiei adiponectinei în țesutul adipos și creșterea nivelurilor circulante de adiponectină ajustate la greutatea corporală sau la masa grasă.
SUBVENȚII
Cercetarea a fost susținută de Centrul Internațional Fogarty al Institutelor Naționale de Sănătate (NIH) în cadrul grantului U01-TW-006674 pentru Grupurile Internaționale Cooperative pentru Biodiversitate; Centrul NIH pentru Cercetarea Suplimentelor Dietetice privind Botanicele și Sindromul Metabolic, grant nr. 1-P50-AT-002776-01; și fitomedică (Jamesburg, NJ).
- Un model de șoarece de obezitate indusă de dietă și rezistență la insulină - PubMed
- Deteriorarea CGI-58 la șoareci provoacă steatoză hepatică, dar previne obezitatea și glucoza induse de dietă
- Semnalizare AR necesară pentru termogeneza indusă de dietă și știința rezistenței la obezitate
- Cele mai bune pastile pe care le-am încercat Obezitate Dieta Pilula Slabire - Global Study UK
- Un extract de afine bogat în polifenoli protejează împotriva obezității induse de dietă, rezistenței la insulină și