Eva M. Vicente-Perez
a School of Pharmacy, Queen’s University Belfast, 97 Lisburn Road, Belfast BT9 7BL, Marea Britanie
Eneko Larrañeta
a School of Pharmacy, Queen’s University Belfast, 97 Lisburn Road, Belfast BT9 7BL, Marea Britanie
Maelíosa T.C. McCrudden
a School of Pharmacy, Queen’s University Belfast, 97 Lisburn Road, Belfast BT9 7BL, Marea Britanie
Adrien Kissenpfennig
b Clădirea Wellcome-Wolfson, Centrul de Medicină Experimentală, Școala de Medicină, Stomatologie și Științe Biomedice, Universitatea Queen's Belfast, 97 Lisburn Road, Belfast BT9 7BL, Marea Britanie
Shauna Hegarty
c Spitalul Royal Victoria, 274 Grosvenor Road, Belfast BT12 6BA, Marea Britanie
Helen O. McCarthy
a School of Pharmacy, Queen’s University Belfast, 97 Lisburn Road, Belfast BT9 7BL, Marea Britanie
Ryan F. Donnelly
a School of Pharmacy, Queen’s University Belfast, 97 Lisburn Road, Belfast BT9 7BL, Marea Britanie
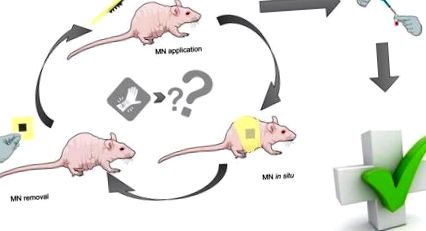
Abstract grafic
Abstract
1. Introducere
Studiile de siguranță efectuate până în prezent au presupus că MN va fi întotdeauna utilizat pentru cea mai frecventă aplicație propusă; ca dispozitive de administrare a vaccinului. În consecință, măsurătorile au fost luate după o singură inserție a matricei MN. Cu toate acestea, munca noastră a arătat că plasturile MN proiectați corespunzător sunt capabili să administreze doze relevante terapeutic de medicamente pe cale transdermică, chiar și atunci când aceste medicamente nu au o potență ridicată [16], [17]. De asemenea, am ilustrat că MN poate avea un rol de jucat în monitorizarea pacientului minim invazivă [18], [19]. În ambele aplicații din urmă, MN va fi cu siguranță introdus în piele în mod regulat, utilizarea zilnică nu fiind exclusă. Într-adevăr, chiar și vaccinurile MN sunt susceptibile de a fi inserate de mai multe ori, având în vedere necesitatea unor regimuri prime și de stimulare pentru a obține o imunizare puternică pentru majoritatea vaccinurilor actuale.
Punctul nostru de vedere este că dizolvarea matricelor MN polimerice își va găsi cea mai adecvată utilizare ca vehicule de administrare a vaccinurilor, datorită capacității lor de încărcare de obicei limitate și a tendinței lor de a depune polimerul în piele. Ca atare, acestea vor fi introduse în piele de un număr relativ mic de ori de-a lungul vieții unui pacient. În schimb, MN-ul nostru care formează hidrogel, care se umflă în piele pentru a permite livrarea controlată a unei substanțe medicamentoase dintr-un rezervor atașat de medicamente de tip plasture sau captează lichidul interstițial al pielii pentru a fi utilizat în monitorizarea pacientului, sunt îndepărtați intacte de pe piele, depunând nicio măsurabilă cantitate de polimer [16], [17], [18], [19]. Deoarece pacienții pot avea nevoie de un medicament administrat zilnic sau de monitorizare de rutină pentru o afecțiune cronică, este posibil ca aceste MN să fie introduse în piele într-o bază mult mai regulată. Deoarece autoritățile de reglementare vor pune, fără îndoială, întrebări cu privire la impactul inserării repetate a MN, am proiectat o serie de experimente preclinice pentru a investiga acest lucru, ale căror rezultate sunt detaliate aici.
2. Materiale și metode
2.1. Produse chimice
Gantrez® S-97 BF, un copolimer de metil-vinil eter-co-maleic-acid (PMVE/MA), Mw = 1.500.000 Da) și poli (vinil pirolidonă) (PVP, Mw = 58.000 Da) au fost furnizate de Ashland, Surrey, Marea Britanie. Polietilen glicol (PEG, Mw = 10.000 Da) a fost obținut de la Sigma-Aldrich, Steinheim, Germania. Isofluranul a fost achiziționat de la Abbott Laboratories, Illinois, SUA. Formaldehida-soluție salină a fost achiziționată de la TCS Biosciences Ltd, Buckingham, Marea Britanie. Toate celelalte substanțe chimice utilizate au avut un grad de reactiv analitic.
2.2. Animale
Crl: Șoarecii SKH1-Hr hr au fost aleși ca animale de testare, deoarece au fost utilizați anterior ca model animal dermatologic din cauza lipsei lor de păr [20]. Această caracteristică a evitat procedura de îndepărtare continuă a părului înainte de inserarea MN care ar putea irita pielea. Important, spre deosebire de alte tulpini de șoareci fără păr, Crl: SKH1-Hr hr este imunocompetent [21].
Toate experimentele pe animale de-a lungul acestui studiu au fost aprobate de Comitetul de Etică al Unității Serviciilor Biologice QUB și efectuate în conformitate cu politica Federației Asociațiilor Europene de Științe a Animalelor de Laborator (FELASA) și a Convenției europene pentru protecția animalelor vertebrate utilizate în scopuri experimentale și Alte scopuri științifice, cu implementarea principiului 3R (înlocuire, reducere, rafinament). Orice animal cu o pierdere în greutate de 20% în timpul studiului urma să fie îndepărtat pentru eutanasie, dar acest lucru nu a avut loc. Nici nu au apărut reacții cutanate la MN. La sfârșitul experimentului, eutanasierea a fost de dioxid de carbon.
2.3. Testele biomarkerului
Kituri de cuantificare ELISA Mouse DuoSet pentru IL-1β, CRP și TNF-α au fost achiziționate de la R&D Systems Inc., Minneapolis, SUA. Mouse IgG Total ELISA Ready-SET-Go! a fost achiziționat de la Affymetrix, California, SUA. În toate cazurile, s-au făcut diluții adecvate ale probelor, astfel încât să se alinieze la intervalele de calibrare relevante.
2.4. Microneedles
Micromulele din silicon proiectate cu laser au fost fabricate folosind o metodă detaliată anterior [32]. Caracteristicile acelor produse au fost forme conice cu: 600 μm înălțimi, 300 μm lățimi de bază și 150 μm ac interspacing pe o zonă de 0,5 cm 2 (19 × 19 design) și 600 μm înălțimi, 300 μm lățimi de bază și 300 μm ace interspacing o suprafață de 0,5 cm 2 (design 11 × 11).
Așa cum se arată în FIG. 1, MN care formează hidrogel a fost preparat din amestecuri apoase de 15% g/g PMVE/MA și 7,5% g/g PEG așa cum s-a descris anterior [16], [17], [18], [19]. MN dizolvarea a fost preparată din amestecuri apoase de 20% g/g PMVE/MA și respectiv 40% g/g PVP. În fiecare caz, formulările au fost mai întâi centrifugate la 3500 rpm timp de 15 minute pentru a asigura un amestec omogen și pentru a îndepărta orice bulă de aer. O alicotă de 0,5 g a fost apoi aruncată în micromould din silicon și centrifugată din nou la 3500 rpm timp de încă 15 min. După uscare în aer, MN care formează hidrogel a fost reticulat prin esterificare. În toate cazurile, pereții laterali formați în timpul micromoldajului au fost îndepărtați folosind un bisturiu încălzit înainte de utilizare.
- Reddit - lostitnarwhals - Hei Narwhals! Pierderea a 6 kg face diferența în ceea ce privește aspectul tău
- Mymi Wonder Patch Recenzii Funcționează Răspunsuri de sănătate de încredere
- Shake Vitamine Proteine Pierdere în Greutate Băuturi Ceai pentru piele; Antrenorul Herba
- Semne de preeclampsie, cauze, factori de risc, complicații, diagnostic și tratament
- Plante medicinale din Africa de Sud utilizate pentru tratarea bolilor de piele - ScienceDirect