Eva Lindauer
1 Departamentul de Neurologie, Universitatea din Ulm, Ulm, Germania,
Luc Dupuis
2 Inserm U1118, Mecanisme centrale și periferice ale neurodegenerării, Strasbourg, Franța,
3 Universitatea din Strasbourg, Facultatea de Medicină, Strasbourg, Franța,
Hans-Peter Müller
1 Departamentul de Neurologie, Universitatea din Ulm, Ulm, Germania,
Heiko Neumann
4 Institutul de procesare a informațiilor neuronale, Universitatea din Ulm, Ulm, Germania (HN),
Albert C. Ludolph
1 Departamentul de Neurologie, Universitatea din Ulm, Ulm, Germania,
Jan Kassubek
1 Departamentul de Neurologie, Universitatea din Ulm, Ulm, Germania,
Conceput și proiectat experimentele: ACL JK. Au efectuat experimentele: EL LD HPM JK. Analiza datelor: EL LD HPM JK. Reactivi/materiale/instrumente de analiză contribuite: LD HPM HN. Am scris lucrarea: EL LD HPM HN ACL JK.
Date asociate
Abstract
fundal
scleroza laterală amiotrofică (SLA) este o boală neurodegenerativă care duce la deces în câțiva ani de la diagnostic. Malnutriția și pierderea în greutate sunt frecvente și sunt indicii de prognostic slab. Nu au fost studiate distribuția totală de grăsimi corporale și grăsimi la pacienții cu SLA.
Obiective
Scopul nostru a fost să descriem conținutul și distribuția țesutului adipos la pacienții cu SLA.
Proiecta
Am efectuat un studiu transversal într-un grup de pacienți cu SLA (n = 62, durata medie a bolii 22 luni) împreună cu controale sănătoase potrivite vârstei și genului (n = 62) folosind o metodă bazată pe RMN pentru a studia cantitativ distribuția grăsimilor.
Rezultate
tabelul 1
| articol | controale | ALS | valoarea p |
| număr inclus | 62 | 62 | |
| M/F | 36/26 | 42/20 | 0,3527 |
| varsta (ani) | 59,9 ± 12,2 | 59,9 ± 12,1 | 1.000 |
| IMC (kg/m 2) | 25,0 ± 6,0 | 23,1 ± 3,6 | 0,0004 |
| locul debutului (bulbar/coloanei vertebrale) | 44 coloanei vertebrale | ||
| 10 bulbar | |||
| 7 necunoscut | |||
| durata bolii (luni) | 22,5 ± 15,3 | ||
| ALS-FRS-R | 36,3 ± 7,5 |
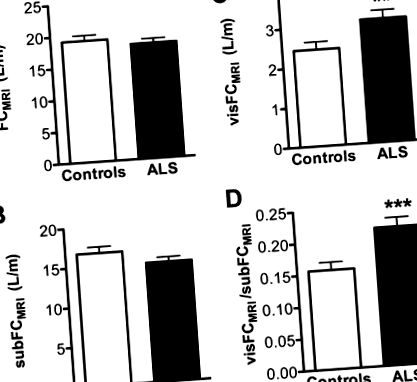
Acumularea de grăsimi viscerale este crescută în SLA
În contrast cu măsurarea impedanței bioelectrice sau cu markeri biochimici, RMN permite studierea topografiei regionale a diferitelor plăci de grăsime. Pacienții cu SLA au prezentat depozite viscerale de grăsime vizibil extinse și țesut adipos subcutanat similar, așa cum se ilustrează în figura 1 . În mod consecvent, analiza cantitativă a arătat că FCMRI și conținutul de grăsime subcutanată (subFCMRI) au fost aproximativ identice între ambele grupuri (p = 0,41 pentru FCMRI și p = 0,09 pentru subFCMRI, Figura 2A - B ), dar volumul de grăsime viscerală a crescut la pacienții cu SLA (visFCMRI, Figura 2C, p = 0,0083). Astfel, raportul dintre tampoanele de grăsime viscerală și subcutanată a fost mai mare la pacienții cu SLA ( Figura 2D, p = 0,001).
Corelații între conținutul total de grăsimi totale (FCMRI, A), subcutanat (subFCMRI, B), visceral (visFCMRI, C) în scanările RMN și scorurile funcționale ale scării de evaluare funcțională a sclerozei laterale amiotrofe (ALS-FRS-R). sunt indicate valorile p și coeficienții de corelație corespunzători (r). Dacă coeficientul de corelație este pozitiv, cele două variabile tind să crească sau să scadă împreună.
Corelații între conținutul total de grăsimi (FCMRI, A), subcutanat (subFCMRI, B), visceral (visFCMRI, C) în scanările RMN și pante ale scorurilor funcționale ale scării de evaluare funcțională a sclerozei laterale amiotrofice (ALS-FRS-R, în puncte pe lună). sunt indicate valorile p și coeficienții de corelație corespunzători (r). Dacă coeficientul de corelație este pozitiv, cele două variabile tind să crească sau să scadă împreună.
Pacienții de sex masculin (A, C, E) și pacienții de sex feminin (B, D, F) au fost stratificați în funcție de totalul lor (FCMRI, A, B), subcutanat (subFCMRI, C, D) și visceral (visFCMRI, E, F ) conținutul de grăsime în scanările RMN. sunt indicate valorile p (log-rank). Linia neagră reprezintă pacienții sub mediana grupului; linia gri reprezintă pacienții peste mediana grupului.
masa 2
| FCMRI | visFCMRI | subFCMRI | ||||
| ßi | valoarea p | ßi | valoarea p | ßi | valoarea p | |
| constantă (ß0) | 10.775 este cel mai frecvent | 0,092 | Cel mai frecvent 1.967 | 0,294 | 8.808 e cel mai frecvent | 0,088 |
| ALS-FRS-R (x1) | 0,198 | 0,042 | 0,012 | 0,668 | 0,186 | 0,019 |
| sex (x2) | Cel mai frecvent 3,117 | 0,049 | -Cea mai frecventă 1.398 | 0,004 | 4.515 e cel mai frecvent | 0,001 |
| varsta (x3) | 0,025 | 0,685 | 0,030 | 0,099 | −0,005 | 0,912 |
| site-ul de debut (x4) | −1.216 | 0,514 | −0,379 | 0,492 | −0,837 | 0,577 |
Discuţie
Prin utilizarea analizei automate a grăsimii RMN, am arătat că distribuția grăsimii este modificată la pacienții cu SLA: grăsimea viscerală a crescut indiferent de severitatea bolii, în timp ce grăsimea subcutanată a fost corelată cu starea funcțională și supraviețuirea pacienților cu SLA.
Primul rezultat important al studiului nostru este că distribuția grăsimilor nu a fost similară între SLA și controalele sănătoase. În timp ce conținutul total de grăsime a apărut aproximativ similar cu martorii, pacienții cu SLA au prezentat țesuturi grase viscerale extinse și o tendință spre scăderea țesuturilor grase subcutanate. În consecință, raportul dintre grăsimea viscerală și cea subcutanată a crescut. Această situație a apărut similar cu ceea ce apare în sindromul metabolic [14], [15], [16], [17] și este în concordanță cu intoleranța la glucoză [9] și hiperlipemie [7], [8] documentată anterior în alte cohorte de pacienți . Această distribuție anormală a grăsimilor care amintește de sindromul metabolic a fost asociată paradoxal cu pierderea în greutate și hipermetabolismul. [1], [2], [3],. Cu toate acestea, este posibil ca hipermetabolismul și pierderea în greutate să reflecte utilizarea crescută a lipidelor în periferie. [23] Astfel, pacienții cu SLA pot prezenta o decuplare între mobilizarea depozitelor de lipide și starea metabolică/nutrițională. [1], [21] De remarcat, distribuția grăsimii observată aici la oameni este deosebit de diferită de modelele animale care, dimpotrivă, pierd grăsime viscerală în cursul bolii. [12].
Am arătat în continuare că depozitele de grăsime ale pacienților cu SLA au prezentat o corelație diferențială cu parametrii clinici. În timp ce cantitatea de grăsime viscerală nu a fost corelată cu starea funcțională, am observat o puternică corelație pozitivă între țesutul subcutanat, starea funcțională și supraviețuirea. Lucrări recente au indicat faptul că IMC a fost un predictor independent al supraviețuirii în SLA, [2], [5] și dislipidemie, asociată și cu supraviețuirea mai lungă, [7] este un marker surogat al IMC crescut. Interesant este faptul că pacienții cu SLA obezi morbid prezintă supraviețuire scăzută paradoxal. Obezitatea morbidă este puternic asociată cu creșterea grăsimii viscerale și, pe baza rezultatelor noastre, s-ar putea specula că dezvoltarea obezității morbide, extinderea grăsimii viscerale în detrimentul grăsimii subcutanate, ar putea avea consecințe dăunătoare asupra stării funcționale și a supraviețuirii pacienților cu SLA. Susținând această din urmă ipoteză, am observat o supraviețuire crescută la pacienții de sex masculin cu grăsime subcutanată mai mare, dar nu viscerală ( Figura 5 ).
Lucrările noastre actuale sunt limitate de designul transversal. La închiderea bazei noastre de date, la 24 de luni de la finalizarea RMN-urilor, 57% dintre pacienții cu SLA au murit. Am observat o supraviețuire îmbunătățită la pacienții de sex masculin cu grăsime subcutanată crescută. Lucrările viitoare, cu un număr crescut de pacienți și o monitorizare mai lungă, ar trebui efectuate pentru a confirma acest prim studiu. Mai mult, designul nostru transversal nu a permis monitorizarea evoluției distribuției grăsimilor cu progresia bolii la un anumit pacient. Astfel de informații ar putea fi, de asemenea, de interes pentru dezvoltarea factorilor de prognostic pe baza distribuției grăsimilor. O altă limitare a studiului nostru actual este progresia omogenă a bolii în cohorta noastră de pacienți, ceea ce slăbește corelația observată între progresia bolii și distribuția grăsimilor. Studiile care investighează distribuția grăsimii la progresorii rapizi față de cei cu progres lent sunt astfel justificate.
Ca o concluzie, am dori să subliniem că creierul este organul cu cea de-a doua cea mai mare concentrație de lipide, după țesutul adipos, și că mai multe boli ale creierului sunt legate de modificări ale metaboliților lipidici. De exemplu, boala Alzheimer este strâns asociată cu metabolismul colesterolului, atât genetic cât și fiziologic. [44], [45] Cu toate acestea, în mod surprinzător, puține studii s-au concentrat asupra țesutului adipos ca sursă și stocare pentru aceste molecule cheie ale creierului. [46] Studiul nostru actual RMN indică faptul că țesutul adipos este afectat și în topografia sa și potențial funcția sa în SLA și solicită studii funcționale ulterioare asupra acestui țesut metabolic cheie.
Subiecte și metode
Pacienți
Șaizeci și doi de pacienți cu SLA și 62 de voluntari sănătoși au fost supuși protocolului de scanare RMN. Pacienții au fost recrutați în ambulatoriu și în spitalele din cadrul Departamentului de Neurologie, Universitatea din Ulm, Germania. Grupul de control în funcție de vârstă și sex, fără nicio boală neurologică/psihiatrică sau altă afecțiune medicală, a fost recrutat printr-un grup de voluntari (Universitatea pentru Bătrâni, expoziție de muncă voluntară) sau soții pacienților. Controalele cu boli neurologice sau psihiatrice sau contraindicațiile pentru scanarea RMN au fost excluse din studiu. Toți pacienții au fost diagnosticați cu SLA definită (23) sau probabilă (39) utilizând criteriile El Escorial și au avut o durată a bolii de 22,55 ± 15,25 luni. Pacienți cu gastrostomie, funcție respiratorie redusă (FVC 3 .
Pregătirea datelor: omogenizarea intensității și îndepărtarea brațelor
În cazurile în care câmpul magnetic sau gradările neomogenități sau distorsiuni ar putea provoca neomogenități ale imaginii pe zona de scanare mare, a fost utilizată o funcționalitate de reparație interactivă pentru a corecta distorsiunile și a pregăti setul de date pentru operațiuni ulterioare de date. Deoarece brațele erau adesea înregistrate doar parțial și nu prezentau interes pentru analize suplimentare, brațele erau șterse manual din seturile de date.
Omogenizarea intensității: filtrare prin difuzie
Pentru a omogeniza intensitatea în seturile de date, s-a aplicat filtrarea prin difuzie. [19].
Analiză
Determinarea grăsimii subcutanate a fost efectuată utilizând algoritmul ARTIS (Redare adaptată pentru segmentarea intensității țesuturilor), care sa dovedit deja că arată o stabilitate ridicată în rezultate. [19] Țesutul adipos visceral abdominal a fost identificat prin selectarea tuturor voxelilor conectați în funcție de intensitatea lor în intervalul predefinit din ARTIS. [19].
Analize statistice
Analiza statistică a fost efectuată folosind Graphpad Prism 5 (GraphPad Software, La Jolla, SUA). Deoarece distribuția grăsimilor atât la pacienți, cât și la voluntari nu a reușit testul de normalitate conform testelor D’Agostino și Pearson, am folosit testul Mann-Whitney pentru comparații de grup. Testul exact al lui Fisher a fost utilizat pentru variabilele dihotomice, iar testul de corelație Spearman pentru corelații. O analiză de regresie multivariată a fost realizată/efectuată folosind SPSS Statistics 19 (IBM, New York, SUA). Testul de rang log (Mantel-Cox) a fost utilizat pentru a evalua efectul diferitelor variabile asupra supraviețuirii. La sfârșitul studiului, 34 de pacienți SLA muriseră și 23 erau încă în viață. Pacienții încă în viață au fost cenzurați pentru analiza supraviețuirii. Semnificația a fost stabilită la p (900K, tif)
Mulțumiri
Mulțumim pacienților și voluntarilor pentru acest studiu. Autorii nu raportează nicio dezvăluire pentru acest studiu.
Declarație de finanțare
Autorii nu au sprijin sau finanțare de raportat.
- Inflamația țesutului adipos contribuie la pierderea în greutate corporală indusă de alimentele cronice experimentale
- Țesutul adipos ca organ imunologic - Grant - 2015 - Obezitate - Biblioteca online Wiley
- Întrebați un expert cum afectează distribuția greutății viteza obiectului de rulare
- Bioinkuri și tehnologii de bioprintare pentru a realiza constructe de țesuturi eterogene și biomimetice -
- 6 strategii pentru a-ți viza capul lateral al tricepsului și a construi brațe mai mari