Homayoon BASHIRI
1 Centrul de cercetare a bolilor infecțioase, Universitatea de Științe Medicale Kermanshah, Kermanshah, Iran,
2 Departamentul de Medicină Internă, Universitatea de Științe Medicale Kermanshah, Kermanshah, Iran,
Arezoo BOZORGOMID
1 Centrul de cercetare a bolilor infecțioase, Universitatea de Științe Medicale Kermanshah, Kermanshah, Iran,
Vahid SHOJAEIMOTLAGH
3 Departamentul de asistență medicală chirurgicală, Universitatea de Științe Medicale Khoy, Khoy, Iran,
Autorii declară că nu au niciun conflict de interese.
Abstract
Context/obiectiv
Boala hepatică grasă nealcoolică (NAFLD) este cunoscută ca fiind cea mai răspândită boală hepatică cronică din întreaga lume. Incidența acestei boli a crescut dramatic în ultimul deceniu. Studiile au arătat o relație puternică între nivelul feritinei și severitatea NAFLD. Obiectivul prezentului studiu a fost de a evalua efectul adăugării Hijamat, ca procedură de reducere a fierului, la modificarea standard a stilului de viață asupra îmbunătățirii rezistenței la insulină și a enzimelor hepatice la pacienții cu NAFLD.
Materiale și metode
O sută douăzeci de pacienți cu NAFLD au participat la un studiu randomizat, controlat, cu o singură orbă. Grupul de control a primit consiliere pentru nutriție și activitate fizică pentru o perioadă de 6 luni. Grupul de tratament a primit articolele de mai sus plus Hijamat de 3 ori pe parcursul unei luni. Imaginile cu ultrasunete ale ficatului, HOMA-IR și datele de laborator, inclusiv ALT, AST, au fost evaluate pre și postintervenție.
Rezultate
La sfârșitul studiului, s-a demonstrat o scădere semnificativă a nivelului seric al HOMA-IR (–1.30 ± 0.88 vs –.02 ± 0.47, P Cuvinte cheie: Boală hepatică grasă nealcoolică, cupare umedă, Hiamat, ALT, AST
1. Introducere
Boala ficatului gras nealcoolic (NAFLD) reprezintă un spectru de boli care variază de la steatoză la steatohepatită, fibroză, ciroză și chiar carcinom hepatocelular care se caracterizează prin acumularea de lipide în hepatocite [1]. Incidența NAFLD a crescut în ultimele 3 decenii, ajungând la 6% -35% în populația adultă din întreaga lume [2]. Unul dintre cele mai importante motive pentru această prevalență ridicată este globalizarea stilului de viață sedentar și a obiceiurilor dietetice moderne, împreună cu prevalența crescută a obezității centrale (abdominale), a diabetului zaharat de tip 2, a dislipidemiei și a sindromului metabolic [3].
Deși mecanismele moleculare implicate în patogeneza NAFLD sunt încă puțin înțelese, rezistența la insulină contribuie la creșterea livrării de acizi grași liberi în ficat și la supraproducția lipidelor în ficat, ducând în cele din urmă la NAFLD [4]. Conform diferitelor studii, nivelurile ridicate de feritină serică, ca marker standard al stocării fierului, sunt asociate cu o creștere a radicalilor liberi și induc rezistența la insulină în miocite, țesut adipos [5].
Terapia cu cupaj umed sau Hijamat este una dintre cele mai vechi tehnici medicale din Asia, Orientul Mijlociu și Europa. Este menționat pe scară largă la documentele de medicină tradițională iraniană pentru prevenirea și tratamentul diferitelor tulburări [6]. În această procedură, substanțele patologice cauzale sunt excretate din identificul interstițial și din sângele din rețeaua capilară a pielii după aspirație și etapele de scarificare [7]. Câteva studii au sugerat că îndepărtarea fierului prin flebotomie duce la îmbunătățirea rezistenței la insulină și a enzimelor hepatice la pacienții cu NAFLD cu niveluri serice normale de feritină și transferină [8,9]. Spre deosebire de Hijamat, una dintre venele superficiale ale corpului este tăiată cu bisturiul și o parte din sânge este îndepărtat din corp în flebotomie [10]. Majoritatea oamenilor preferă de obicei Hijamat în locul flebotomiei, deoarece este mai ușor și provoacă mai puține dureri. În lumina dovezilor cumulative pentru asocierea dintre feritina serică și NAFLD, acest studiu a fost realizat pentru a evalua rolul terapiei Hijamat în îmbunătățirea enzimelor hepatice și a HOMA-IR la pacienții cu NAFLD.
2. Materiale și metode
2.1. Design de studiu
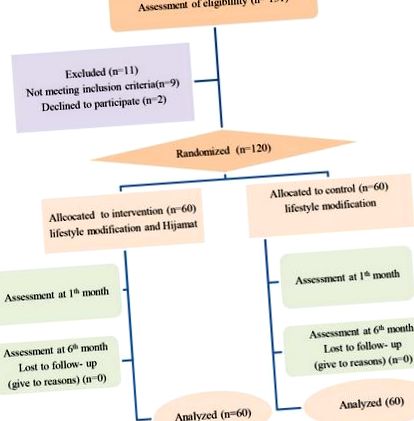
Studiul a fost un studiu randomizat, unic orb (observator-orb), iar durata studiului a fost de 6 luni. Proiectul studiului este descris în Figura. Pacienții au fost împărțiți în mod aleatoriu în grupurile de tratament și control, folosind metoda de randomizare blocată stratificată cu un computer. Toate cazurile NAFLD au primit inițial consiliere pentru a reduce aportul de carbohidrați, carne roșie, alimente prăjite, zaharuri și grăsimi și pentru a crește aportul de fibre și exercițiile fizice (cel puțin 20 de minute, de 3 ori pe săptămână) ca tratament de rutină. După 4 luni, grupul de tratament a primit Hijamat de 3 ori pe parcursul unei luni (0 zile, 14 zile și 28 de zile) [11]. Hijamat a fost efectuat folosind cupe sterile de unică folosință în 5 puncte: ambele scapule, ambele regiuni lombare și vertex. Cupe de unică folosință au fost plasate pe aceste puncte și presiunea negativă a fost aplicată de o pompă de cupare. Cupele au fost îndepărtate după aproximativ 2-3 minute. Apoi, lancete de unică folosință de calibru 26 au fost utilizate pentru scarificare la o adâncime de 2 mm în locurile cupelor. Pomparea cu vid a fost repetată pentru a doua oară și 3-5 cm3 dintr-o excreție sângeroasă au fost îndepărtate pe loc de cupare. Site-urile au fost apoi acoperite cu tampoane sterile.
2.2. Participanții la studiu
Subiecții au fost selectați dintre acei adulți cu vârsta de peste 18 ani, consemnați consecutiv la Clinica de gastroenterologie și hepatologie a spitalului terapeutic educațional Imam Reza (Kermanshah, Iran) cu diagnostic de NAFLD. Acest spital este cel mai mare centru dintre centrele de recomandare din provincia Kermanshah, la vest de Iran. Un diagnostic de NAFLD a fost făcut în conformitate cu dovezile clinice, enzimele hepatice și criteriile de ultrasunografie. Toți subiecții au acordat consimțământul informat în scris pentru studiu. Pacienții cu infecție virală cu hepatită B și/sau C, icter, hepatită autoimună, boala Wilson, deficit de α-1-antitripsină, tip 1 sau forme secundare de diabet, boală celiacă, consum de alcool, consum de corticosteroizi și tulburări renale, precum și gravide sau femeile care alăptează au fost excluse din studiu. Datele demografice, cum ar fi vârsta, sexul și istoricul medical, au fost colectate din interviurile cu pacienții în timpul screeningului.
Organigrama alocării, urmăririi și analizei acestui studiu clinic.
2.3. Marime de mostra
Nu au existat studii similare care să ne ajute cu studiul dimensiunii eșantionului. S-a recomandat ca aproximativ 60 de pacienți să aibă o dimensiune rezonabilă a eșantionului pentru un studiu pilot care să investigheze efectele tratamentului [12]. Astfel, am decis să recrutăm cel puțin 60 de pacienți în fiecare grup ca probă de confort.
2.4. Evaluarea biochimică
Probele de sânge au fost colectate de la participanți după un post de 12 ore peste noapte înainte și după intervenție. După separarea serului, probele au fost etichetate și depozitate la –70 ° C până la analiză. Activitățile enzimatice ale alaninei aminotransferazei (ALT) și ale aspartatului aminotransferazei (AST) au fost măsurate cu autoanalizatorul Hitachi 902 (Japonia) folosind kituri analitice Pars Azmoon (Iran). Intervalele de referință de laborator pentru ALT și AST au fost 5-41 UI/L și respectiv 5-37 UI/L. Rezistența la insulină a fost determinată utilizând evaluarea modelului homeostaziei (HOMA-IR) prin următoarea formulă: insulină de post (µu/ml) × glucoză de post (mmoL/dL)/405.
2.5. Ecografie a ficatului
Imaginile cu ultrasunete ale fiecărui participant au fost, de asemenea, evaluate înainte și după intervenție. Steatoza hepatică a fost clasificată la 0 (fără acumulare de grăsime), 1 (creștere minimă a ecogenității, împreună cu aspectul normal al diafragmei și peretelui venei porte), 2 (creștere moderată a ecogenității, împreună cu vizualizarea ușor afectată a peretelui venei portal și a diafragmei), și 3 (creștere severă a ecogenității, împreună cu vizualizarea slabă sau lipsă a diafragmei, peretelui venei portale și porțiunea posterioară a lobului hepatic drept) [13].
2.6. analize statistice
Software-ul SPSS a fost utilizat pentru analiza statistică versiunea 16 (SPSS Inc., Chicago, IL, SUA). Testul Kolmogorov - Smirnov a fost aplicat pentru a evalua distribuția normală a datelor în fiecare grup. Variabilele continue sunt prezentate ca medie ± deviație standard (SD). Testul t-eșantioane independente sau testul Mann-Whitney U au fost utilizate pentru comparații între grupuri, după caz, și testul t asociat a fost utilizat pentru comparații în cadrul grupului. Variabilele categorice au fost comparate folosind testul chi-pătrat. P 0.05), deci grupurile au fost comparabile. Caracteristicile pacienților sunt descrise în Tabelul 1.
tabelul 1
Caracteristicile de bază și parametrii biochimici ai grupurilor de control și Hijamat.
| Vârstă, ani | 40,53 ± 7,32 | 38,38 ± 9,26 | 0,161 a |
| Genul feminin (%) | 29 (48,33) | 30 (50) | 0,855 b |
| ALT, IU/L | 46,30 ± 4,26 | 45,88 ± 4,39 | 0,883 c |
| AST, IU/L | 45,46 ± 5,25 | 44,33 ± 4,79 | 0,220 a |
| HOMA-IR | 2,23 ± 0,62 | 3,19 ± 0,65 | 0,630 c |
| Sonografie (%) | |||
| Gradul I | 26 (43,3) | 31 (51,7) | 0,364 b |
| Gradul II | 34 (56,7) | 28 (46,7) | |
| Gradul III | - | 1 (1.7) |
Valorile sunt exprimate ca medie ± SD
un test t eșantion independent
b Testul Chi-pătrat
c Testul Mann - Whitney U
- Microbiota intestinală și boala hepatică grasă nealcoolică - ScienceDirect
- Efectul unei diete hipocalorice în transaminaze în boala hepatică grasă nealcoolică și obeză
- Boli hepatice grase un ucigaș tăcut Narayana Health
- Boala ficatului gras în creștere - Divertisment și viață - Stroudsburg, PA
- BOALA FICATULUI GRAS