Abstract
fundal
Glicogenoza hepatică se caracterizează prin acumularea excesivă de glicogen în hepatocite și reprezintă o complicație a diabetului zaharat de tip 1 slab controlat. Poate fi cauzată de doze excesive de insulină sau de episoade recurente de cetoacidoză. Sindromul Mauriac este o boală rară, care include statura scurtă, întârzierea maturării creșterii, dislipidemie, facies lunar, abdomen protuberant, hepatomegalie cu creștere a transaminazelor. A devenit și mai puțin frecventă după apariția progreselor în tratamentul diabetului, dar încă există. Rapoarte recente au descris glicogenoză fără spectrul complet al sindromului Mauriac la adulți și copii cu diabet fragil. Anomaliile clinice, de laborator și histologice sunt reversibile cu un control glicemic adecvat.
Prezentarea cazului
Raportăm prin prezenta un caz de bărbat în vârstă de 11 ani care a prezentat glicogenoză hepatică care imită sindromul Mauriac. Pacientul a fost internat la clinica noastră de diabet pediatric pentru hepatomegalie marcată, statură scurtă și pentru control metabolic slab. Investigațiile de sânge și testele hepatice au exclus majoritatea cauzelor majore ale hepatopatiei. O biopsie hepatică ne-a permis să punem un diagnostic de glicogenoză hepatică. Pentru a controla hiperglicemia, am titrat inițial doza zilnică de insulină, apoi s-a practicat tratamentul cu insulină intravenoasă, cu normalizarea consecutivă a enzimelor hepatice.
Concluzie
Sindromul Mauriac trebuie luat în considerare la subiecții cu diabet de tip 1 fragil și hepatomegalie.
fundal
Prezentarea cazului
Prezentăm cazul clinic al unui băiat de unsprezece ani, născut din părinți români non-consanguini care au aparținut unor straturi socioeconomice scăzute, afectat de T1D de la vârsta de 8 ani.
La debutul diabetului, a fost internat în secția de urgență a unui spital românesc cu antecedente recente de poliurie, polidipsie, slăbire și slăbiciune. La internare, pacientul a prezentat scorul Glasgow Coma Scale de 8. Au fost efectuate următoarele teste de laborator: analiza gazelor din sânge a arătat pH 7,04, bicarbonat seric 6 mmol/l; glucoza serică a fost de 567 mg/dl; hemoglobina glicată a fost de 120 mmol/l, iar nivelurile de ß-hidroxibutirat au fost de 5,6 mmol/l.
El a fost tratat cu terapie cu insulină, înlocuirea apei și a sării, în conformitate cu orientările Societății Internaționale de Diabet Pediatric și Adolescent pentru managementul cetoacidozei diabetice (DKA) timp de 48 de ore [24]. După suspendarea tratamentului cu DKA, au fost prescrise mai multe injecții zilnice de insulină, cu o doză totală inițială de insulină de 1 UI pe kg, insulină lispro la mese și insulină glargină la culcare. Pacientul a fost externat după o săptămână, dar nu a participat la o vizită ulterioară la Centrul pentru diabet.
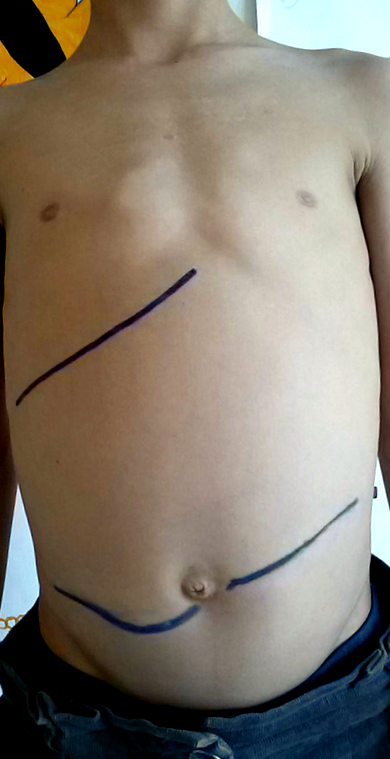
Controlul glicometabolic a fost foarte slab și pacientul a fost internat cu cetoacidoză diabetică moderată în două ocazii. La vârsta de 10 ani, s-a mutat în sudul Italiei împreună cu familia sa. La vârsta de 11 ani, a fost internat din cauza unei DKA severe într-un departament de urgență al unui spital de nivel secundar. După rezolvarea DKA, el a fost transferat la clinica noastră de diabet pediatric pentru investigații ulterioare datorită observării hepatomegaliei marcate (Fig. 1), staturii scurte și a controlului metabolic slab. La admitere, el a prezentat o statură de 127,5 cm și o greutate de 25 Kg (Fig. 1
Limitele hepatice detectate clinic la internarea în centrul nostru de diabet pediatric
Ecografia abdominală a confirmat o hepatomegalie marcată cu textură de ecou regulată și venă portală normală. În timpul spitalizării, a prezentat un control glicemic fragil caracterizat prin fluctuații între hiperglicemie și hipoglicemie. Pentru a obține un control metabolic bun, doza zilnică de insulină a fost titrată, ajungând la o doză zilnică de insulină de 2,3 UI pe kg. Părinții săi au primit un program de educație pentru diabet. SM a fost ipotezată pe baza asocierii hepatomegaliei, staturii scurte, dislipidemiei și istoricului de diabet slab controlat.
S-a efectuat biopsie hepatică, secțiuni de 4 μ grosime colorate în mod obișnuit cu hematoxilină-eozină au fost realizate dintr-un bloc de țesut încorporat în parafină fixat cu formalină 10%, cu tampon neutru. Secțiunile seriale paralele au fost, de asemenea, colorate cu acid periodic Schiff, Sirius Red, Orcein, Perls și tehnicile tricromatice ale lui Masson. Eșantionul a arătat o arhitectură lobulară conservată cu multe hepatocite umflate cu glicogen, pseudo-incluziuni de glicogen nuclear periportal proeminente (Fig. 2a) și steatoză focală macrovesciculară (Fig. 2)
Caracteristici histologice ale reîncărcării glicogenului hepatic. Biopsia hepatică a arătat o arhitectură normală cu modificări hepatocelulare difuze caracterizate prin hepatocite umflate cu citoplasmă palidă, cu colorare clară. Puține nuclee glicogenate sunt prezente în hepatocitele periportale (săgeată)A, Pata de hematoxilină/eozină, X360). O cantitate mare de depozite de glicogen relevate de petele PAS (b, nucleare Mayer’s Haemalum, X360)
La vizita de urmărire de trei luni, el a prezentat un control glico-metabolic slab, hemoglobină glicată 124 mmol/l și variabilitate glicemică extremă. La examenul fizic, a avut o hepatomegalie mai severă. Testele de laborator au arătat colesterolul total 450 mg/dl, trigliceridele 995 mg/dl, ALT 807 UI/L, AST 694 UI/L. Prin urmare, a fost internat în spital și s-a practicat tratament intravenos continuu cu insulină pentru normalizarea aminotransferazelor și realizarea unui control glicemic bun, atins după opt zile. La ultima vizită de urmărire, pacientul a menținut un control glicemic bun, demonstrat de valoarea hemoglobinei glicate (55 mmol/l). Îmbunătățirea controlului glicol-metabolic duce la o remisiune completă a semnelor clinice biochimice și la rezolvarea completă a hepatomegaliei (Fig. 3). În ciuda regresiei bolii hepatice, statura sa a rămas Fig. 3
Reducerea hepatomegaliei după tratament intravenos continuu cu insulină
Diagrama de creștere a pacientului de la admiterea la ultima vizită de urmărire
discutii si concluzii
Până în prezent, SM în timpul copilăriei este mai puțin frecventă, mai ales odată cu apariția de noi analogi de insulină și regimuri intensive de insulină. Cu toate acestea, a existat recent un număr tot mai mare de rapoarte de caz care descriu hepatomegalie indusă de glicogen la pacienții cu T1D fără alte componente ale SM [28, 29]. Mai frecvent, pacienții afectați sunt adolescenți sau tineri [5]. Este bine cunoscut deoarece adolescența este o perioadă critică pentru pacienții cu T1D. Pe lângă faptul că se confruntă cu aceleași provocări ale colegilor săi diabetici, pacientul nostru aparținea unei familii de imigranți cu nivel socioeconomic scăzut, iar părinții săi nu au reușit să-și gestioneze boala. Concomitența tuturor acestor factori a dus la un control glicemic fragil și la reapariția episoadelor de DKA, despre care se crede că sunt principalii factori de risc în dezvoltarea HG.
HG este complet reversibil cu un bun control metabolic [35]. Infuzia continuă de insulină intravenoasă trebuie luată în considerare ca o opțiune atunci când terapia intensivă cu insulină și dieta adecvată hrănitoare nu sunt suficiente pentru a opri progresia bolii hepatice și a preveni complicații ulterioare. O analiză sistematică cea mai recentă a emis ipoteza că HG ar putea fi diagnosticat în mod conservator, pe baza istoricului medical, a examenului fizic, a testelor de laborator, a studiilor imagistice și a răspunsului la tratament. Acești autori determină executarea biopsiei hepatice numai în caz de îndoială cu privire la diagnosticul sau lipsa răspunsului clinic [36].
SM a devenit o afecțiune neobișnuită, deoarece apariția unui tratament intensiv cu insulină a permis realizarea obiectivelor glicemice ideale la diabetici tineri. Raritatea bolii a asigurat că gradul de conștientizare a acestei afecțiuni clinice de către medici, inclusiv specialiști, este scăzut [37]. Dorim să evidențiem recunoașterea semnelor clinice cheie, cum ar fi un control glicemic fragil și hepatomegalie la pacienții T1D, pentru a evita ca HG să rămână diagnosticat greșit. Rapoarte recente au descris că coexistența unor factori de risc, cum ar fi straturile socio-economice scăzute, vârsta adolescenților, doza zilnică ridicată de insulină ar putea determina o inspecție mai atentă. Sunt necesare studii suplimentare pentru a demonstra rolul mecanismului genetic în debutul acestei boli.
- Semnătura metabolică a rezistenței la insulină asociate obezității și a diabetului de tip 2 Journal of
- Vindecarea tipului 1 Diabet Kefir probiotic
- Hipogonadismul hipogonadotrop în diabetul de tip 2 și obezitatea
- Hypouricemia in total parenteral nutrition The American Journal of Clinical Nutrition Oxford
- Sindromul Leriche care se prezintă cu catastrofă vaso-ocluzivă multisistemică - The Western Journal of