Un Franco
1 Departamentul de Științe Biomedice Avansate, Universitatea „Federico II” din Napoli, Italia
M Ciccarelli
2 Departamentul de Medicină și Chirurgie, Universitatea din Salerno, Italia
D Îmi pare rău
3 IBB-CNR, Napoli, Italia
L Napolitano
1 Departamentul de Științe Biomedice Avansate, Universitatea „Federico II” din Napoli, Italia
A Fiordelisi
1 Departamentul de Științe Biomedice Avansate, Universitatea „Federico II” din Napoli, Italia
B Trimarco
1 Departamentul de Științe Biomedice Avansate, Universitatea „Federico II” din Napoli, Italia
M Durante
4 Institutul Trento pentru fizică și aplicații fundamentale, Trento, Italia
G Iaccarino
2 Departamentul de Medicină și Chirurgie, Universitatea din Salerno, Italia
Abstract
I. INTRODUCERE
Mai multe studii au evidențiat efectele radiațiilor asupra celulelor endoteliale vasculare13-15, dar recent s-a observat că radiațiile pot afecta direct cardiomiocitele16 și alte structuri cardiace care duc la cardiomiopatie17, bolile cardiace ale valvelor și anomalii ale conducerii18. Cu toate acestea, cunoștințele despre efectele directe ale radiațiilor asupra miocardului sunt încă slabe, raportate la efectele asupra cardiomiocitului unic și la modificarea moleculară specifică produsă19. Mitocondriile sunt considerate centralele cardiomiocitelor și sunt în același timp sursa majoră a ROS20. Având în vedere relevanța mitocondriilor pentru funcțiile cardiace, este posibil să se speculeze că efectele dăunătoare ale unei iradieri cronice ar putea fi legate de disfuncția acestui organet21. În această revizuire vom discuta cele mai recente dovezi privind toxicitatea cardiacă indusă de radiațiile ionizante (raze X) asupra cardiomiocitelor, cu accent pe rolul jucat de mitocondrii.
II. EFECTE FIZICE ȘI BIOLOGICE ALE RAZELOR X
A. Proprietățile fizice ale razelor X.
O radiație este definită ca transportul de energie în spațiu, care este apoi transferat în materie. Radiația este cuantificată și măsurată în electronVolt (eV). Conform spectrului electromagnetic, o radiație poate fi împărțită în radiații neionizante (10 eV). Când radiația ajunge în corp, excită atomii moleculelor țesuturilor biologice. Legat de doza absorbită, consecințele biologice cauzate de radiațiile ionizante se pot schimba în funcție de natura radiației implicate22: particula α, particula β și raza X-Y, unde α și β constituie radiația corpusculară23, în timp ce X și Y sunt electromagnetice radiații. Mai exact, razele X sunt clasificate ca radiații ionizante electromagnetice, indirecte, deoarece produc electroni secundari cu energii cinetice ridicate. La rândul lor, acești electroni pot provoca daune materiei absorbante. Locul liber de electroni din învelișul atomic, cauzat de o ejecție, este umplut cu un electron dintr-un înveliș exterior care duce ulterior la emisia unui foton. O interacțiune tipică între un foton cu raze X și o moleculă de apă este 24:
Unde H20 + este un radical ionic foarte reactiv. Reacția dintre H20 + și molecula de apă produce radicalul hidroxil H0 -
Care este o specie de oxigen foarte reactivă și este responsabilă pentru efectele biologice ale razelor X. Acumularea ROS duce la moartea celulelor apoptotice25 și este asociată cu acumularea de daune care nu pot fi recuperate în mitocondrii și nucleu. De exemplu, caracteristicile tipice induse de radiații implică nucleul cu inducerea mutațiilor punctuale26. Cu toate acestea, atunci când procesul apoptotic nu elimină o celulă transformată, daunele citogenetice, cum ar fi translocațiile, trec la celulele fiice27. Astfel, referindu-se la întregul organism, radiația induce daune ADN poate duce la cancer sau la boli ereditare în funcție de celula specifică deteriorată.
În general, efectele biologice cu raze X sunt de obicei împărțite în două categorii. Prima categorie constă în expunerea la doze mari de radiații pe perioade scurte de timp, producând efecte acute sau pe termen scurt28. A doua categorie reprezintă expunerea la doze mici de radiații pe o perioadă extinsă de timp producând efecte cronice sau pe termen lung. Dozele mari tind să distrugă celulele, în timp ce dozele mici tind să deterioreze sau să schimbe funcțiile mai multor substructuri. Dozele mari pot ucide atât de multe celule încât țesuturile și organele sunt deteriorate sau chiar distruse29. La rândul său, acest lucru provoacă un răspuns rapid al întregului corp numit Sindromul de radiație acută (ARS).
Dozele mici se răspândesc pe perioade lungi de timp și nu provoacă o problemă clinică imediată. Efectele dozelor mici de radiații apar în primul rând la nivel celular și este posibil ca efectele să nu fie observate timp de mulți ani. Aici vom descrie în detaliu efectele biologice ale expunerii scăzute și cronice la raze X.
B. Efectele nucleare ale razelor X
Există trei categorii generale de efecte care rezultă din expunerea la doze mici de radiații. Acestea sunt: 1) Genetice, atunci când efectul este suferit de descendenții individului expus. 2) Somatic30, care implică în primul rând individul expus. Deoarece cancerul este rezultatul primar, este numit și Efect cancerigen. 3) In-Utero31,32, considerat greșit ca o consecință genetică a expunerii la radiații, deoarece efectul, suferit de un embrion/făt în curs de dezvoltare, este văzut după naștere.
Așa cum s-a menționat mai sus, razele X sunt în principal indirect ionizante, deoarece nu induc în mod direct daune chimice, ci produc electroni secundari cu energii cinetice ridicate, cum ar fi hidrogenul (H) și hidroxilii (OH). Aceste fragmente se pot recombina sau pot interacționa cu alte fragmente sau ioni pentru a forma compuși, cum ar fi apa, care nu ar afecta celula. Cu toate acestea, ele se combină și pentru a forma substanțe toxice, cum ar fi peroxidul de hidrogen (H2O2), care pot contribui la distrugerea structurii celulare, indicând faptul că o parte din efectele toxice ale razelor X sunt mediate de ROS.
C. Ros în semnalizarea intracelulară: doar un mediator al daunelor provocate de raze X.?
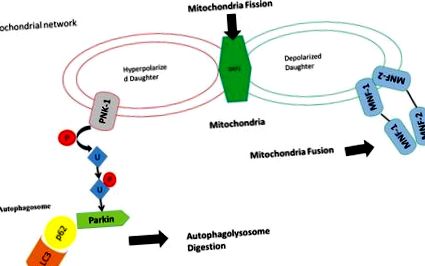
Generează un gradient Ph și
Un gradient de tensiune, care este definit ca potențialul membranei mitocondriale.
Ca răspuns la stres, o parte a pierderii mitocondriilor membranele sale potențiale mitocondriale și induce Drp-1 (fisiune mitocondrială), în consecință, PINK-1 se expune la daune mitocondriilor și conduce la degradarea mitocondriilor prin fosforilarea ubiquitinării și activării ubiquitinei ligazei parkin). Mitocondriile nu și-au pierdut potențialul de membrană activează fuziunea mitocondrială prin mitofusină 1, mitofusină 2 și Opa-1 cu altă parte a mitocondriilor care și-a păstrat membrana potențială a mitocondriilor pentru a forma o nouă mitocondrie funcțională (fuziunea Mitocondriilor).
Fuziunea și fisiunea mitocondriilor reglează dinamismul mitocondrial20, 65 și promovează supraviețuirea celulară ca răspuns la stres66. Pe scurt, dinamismul mitocondrial este implicat în remodelarea structurală a rețelei mitocondriale și în menținerea homeostatică a stabilității ADN-ului mitocondrial și a funcției respiratorii prevenind sau propagând moartea celulară programată, în special ca răspuns la stres67. Efectele combinate ale fuziunii și fisiunii continue dau naștere la rețele mitocondriale, pentru a păstra funcțiile organelor.
În acest context, este interesant să introducem efectul expunerii la raze X asupra funcțiilor mitocondriale43. Expunerea la raze X poate afecta direct membrana mitocondrială68, 69 și/sau indirect prin creșterea producției de ROS70. În ambele cazuri, consecința este reducerea membranelor potențiale mitocondriale și astfel activarea procesului de fisiune/fuziune20. Așa cum s-a descris mai sus, aceste mecanisme sunt fundamentale pentru supraviețuirea și menținerea celulelor în condiții fiziologice, prin urmare, producția crescută de ROS indusă de raze X poate chiar favoriza reînnoirea mitocondriilor71. Cu toate acestea, atunci când cantitatea de ROS acumulată, așa cum se întâmplă cu expunerea cronică la doze mici de raze X, depășește mecanismele de reparare și activează evenimente pro-apoptotice și moartea celulară programată72.
II. RADIUL X ȘI EFECTELE CARDIOVASCULARE: ROLUL MITOCHONDRIEI
Efectele razelor X asupra miocardului85 sunt mai puțin cunoscute, dar se pare că această radiație poate interfera cu funcțiile mitocondriilor, cu consecințe relevante, considerând inima ca un organ dinamic cu un număr abundent de mitocondrii86. Prin urmare, leziunile mitocondriilor pot fi esențiale în încurajarea alterărilor cardiace produse de iradierea cronică87.
Rolul mitocondriilor în medierea efectelor razelor X asupra supraviețuirii celulare a fost legat în parte de efectul direct asupra membranei mitocondriale externe și de fenomenul stresului oxidativ (Fig. 2).
Efectele celulare cu raze X mediate de ROS. Razele X de pe membrana plasmatică induc o creștere a ROS prin activarea NOX1 și (5 ’lipossigenazei). Radiografia poate viza mitocondriile direct și indirect: prin creșterea producției de ROS: 1) compușii lanțului respirator. 2) ADNmt generând proteine defecte de mutație și ștergere în lanțul respirator. 3) Alterarea semnalizării redox și a disfuncțiilor mitocondriale care induc necroză și evenimente apoptotice. 4) Eliberarea membranelor mitocondriei exterioare ale citocromului C în fracții citosolice și formarea canalului mPTP pentru a induce evenimente apoptotice și necroze, respectiv.
III. SUMAR SI CONCLUZII
Inimile expuse la radioterapie pot acumula leziuni mitocondriale care nu pot fi recuperate în continuare prin mecanismele mitogeneza și/sau controlul calității. Mecanismele moleculare nu sunt probabil atât de îndepărtate de ceea ce s-a observat în alte condiții, în care toleranța redusă la stres este asociată cu afectarea căilor care participă la rețeaua mitocondrie-nucleu-ER, fundamentală pentru a promova adaptarea celulară la stres. Modele de insuficiență cardiacă după infarctul miocardic, îmbătrânirea sau diabetul112 au arătat rolul central al disfuncției mitocondriale în progresia bolii și descoperirile aferente conduc la abordări specifice care vizează recuperarea dinamicii și funcțiilor mitocondriale107. Prin urmare, o nouă provocare pentru anii următori va fi identificarea rolului specific jucat de acest organel în alterările cardiace induse de stresul cu raze X și astfel dezvoltarea de noi abordări pentru îmbunătățirea și/sau păstrarea funcțiilor mitocondriale și a rețelei în timpul perioadei cronice. stres de radiații.
- NOU) Top 5 Cele mai bune pastile de pierdere în greutate Bee Sting Efecte secundare Pierdere extremă în greutate masculin de vânzare online
- Reductil - dozaj de revizuire a medicamentului, efecte secundare, acțiune, cumpărați Reductil
- Utilizări orale de Naltrexone-Bupropion, Efecte secundare, interacțiuni, imagini, avertismente; Dozare - WebMD
- Utilizări Reglan, dozare; Efecte secundare
- Raze Reiki