Elena Priante
1 Unitate de terapie intensivă neonatală, Departamentul pentru sănătatea femeilor și copiilor, Universitatea din Padova, 35128 Padova, Italia; [email protected] (GV); [email protected] (VM); [email protected] (E.B.)
Giovanna Verlato
1 Unitate de terapie intensivă neonatală, Departamentul pentru sănătatea femeilor și copiilor, Universitatea din Padova, 35128 Padova, Italia; [email protected] (GV); [email protected] (VM); [email protected] (E.B.)
Giuseppe Giordano
2 Departamentul pentru sănătatea femeilor și copiilor, Universitatea din Padova, 35128 Padova, Italia; [email protected] (G.G.); [email protected] (MS)
3 Institutul de Cercetări Pediatrice, Fundația „Città della Speranza”, 35129 Padova, Italia
Matteo Stocchero
2 Departamentul pentru sănătatea femeilor și copiilor, Universitatea din Padova, 35128 Padova, Italia; [email protected] (G.G.); [email protected] (MS)
Silvia Visentin
4 Unitatea de ginecologie și obstetrică, Departamentul pentru sănătatea femeilor și copiilor, Universitatea din Padova, 35128 Padova, Italia; moc.liamg@87nitnesiv
Veronica Mardegan
1 Unitate de terapie intensivă neonatală, Departamentul pentru sănătatea femeilor și copiilor, Universitatea din Padova, 35128 Padova, Italia; [email protected] (GV); [email protected] (VM); [email protected] (E.B.)
Eugenio Baraldi
1 Unitate de terapie intensivă neonatală, Departamentul pentru sănătatea femeilor și copiilor, Universitatea din Padova, 35128 Padova, Italia; [email protected] (GV); [email protected] (VM); [email protected] (E.B.)
3 Institutul de Cercetări Pediatrice, Fundația „Città della Speranza”, 35129 Padova, Italia
Abstract
1. Introducere
Primele mii de zile de viață - între concepție și cea de-a doua zi de naștere a unui copil - sunt o perioadă delicată, când sunt puse bazele sănătății unei vieți. Hrana adecvată în această perioadă crucială a vieții are un impact profund nu numai asupra creșterii și dezvoltării timpurii a vieții, ci și asupra sănătății individuale pe tot parcursul vieții [1]. Acest concept ar trebui extins pentru a include mai mult decât nutriția în sens strict, întrucât întregul mediu la care este expus sugarul este extrem de important. Restricția creșterii intrauterine (IUGR) este o afecțiune paradigmatică în care un „mediu intrauterin ostil” poate împiedica dezvoltarea fetală cu un potențial impact asupra sănătății pe termen lung [2].
Termenul emergent „expozom” se referă la întregul set de expuneri nongenetice care, împreună cu genomul, determină fenotipul final pe parcursul vieții [3]. Metabolomica nedestinată evoluează ca un instrument nou pentru studierea efectelor mediului endogen și exogen. Luând o abordare generată de ipoteze neintenționate, metabolomica permite analiza calitativă și cantitativă simultană a mii de metaboliți diferiți într-o probă biologică, permițând identificarea biomarkerilor și a modelelor metabolice caracteristice unei condiții date. Dintre științele „-omice”, metabolomica este cea care se apropie cel mai mult de fenotipare. Astfel de studii sunt de obicei efectuate pe biofluide, care sunt analizate cu platforme precum spectroscopia cu rezonanță magnetică nucleară (RMN) sau spectrometria de masă (MS). Metaboliții neașteptați sau chiar necunoscuți pot fi dezvăluiți ca fiind importanți în caracterizarea grupurilor specifice de indivizi, determinând noi ipoteze fiziopatologice asupra afecțiunii studiate [4].
În această revizuire narativă, prezentăm mai întâi câteva aspecte cheie ale fiziopatologiei și prezentării clinice a IUGR. Apoi, ne concentrăm pe toate dovezile care rezultă din studiile metabolomice publicate până acum. Aruncăm o privire critică asupra instrumentelor statistice și bioinformatice utilizate pentru a analiza datele metabolomice din studiile care fac obiectul revizuirii noastre. Scopul acestei abordări este de a oferi cititorilor o imagine de ansamblu adecvată asupra IUGR, deoarece credem cu tărie că înțelegerea datelor complexe derivate din analizele metabolomice nu poate fi separată de o cunoaștere aprofundată a fiziopatologiei bolii fiind luată în considerare.
1.1. IUGR: Definiție și diagnostic obstetric
Se estimează că IUGR afectează între 5% și 10% din toate sarcinile din întreaga lume [2] și este o afecțiune care poate influența puternic sănătatea nou-născutului pe termen scurt și lung.
1.2. Rezultate pe termen scurt și lung pentru nou-născuții IUGR
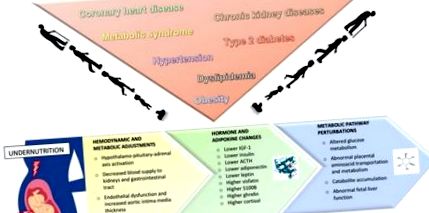
Pentru sugarii SGA, riscul de mortalitate este de 2 până la 4 ori mai mare decât pentru sugarii născuți la termen sau prematuri, dar nu și SGA [10]. Pentru sugarii cu creștere limitată, consecințele imediate la naștere pot include hipotermie, hipoglicemie, hiperglicemie, hipertensiune pulmonară persistentă, hemoragie pulmonară, policitemie, naștere mortală și asfixie intrapartum [11]. Deoarece IUGR este frecvent asociat cu nașterea prematură, bolile multisistemice de prematuritate, cum ar fi creșterea fizică afectată sau dezvoltarea cognitivă și motorie, pot afecta rezultatele pe termen mediu și lung ale nou-născuților IUGR. Mai multe studii sugerează, de asemenea, că o creștere fetală afectată poate predispune la anumite boli majore mai târziu în viață, inclusiv sindromul metabolic, obezitatea, bolile coronariene, hipertensiunea arterială, dislipidemia, diabetul de tip 2 și bolile cronice pulmonare și renale [12,13,14, 15] (Figura 1). Presupunerea este că fătul face o serie de ajustări hemodinamice și metabolice pentru a face față mediului uterin advers, ceea ce poate duce la modificări permanente ale funcției și structurii mai multor sisteme de organe. Postnatal, atunci când condițiile de mediu se schimbă, răspunsul nou-născutului cu creștere limitată ar putea fi inadecvat, crescând în continuare riscul consecințelor pe termen lung [16].
Rezumatul cunoștințelor actuale privind consecințele pe termen scurt și lung ale restricției de creștere intrauterină. Expunerea prenatală a fătului la subnutriție și hipoxie induce ajustări hemodinamice și metabolice, precum și modificări ale hormonilor și adipokinelor. IGF-1: Factor de creștere asemănător insulinei; ACTH: hormon adrenocorticotrop.
Cu câteva decenii în urmă, Hales și Barker au avansat ipoteza așa-numitului „fenotip gospodar”, conform căruia rezistența la insulină și diabetul de tip 2 în timpul maturității ar putea proveni dintr-o adaptare fetală pentru a economisi glucoza ca răspuns la malnutriția intrauterină [17]. Bolile cronice la vârsta adultă pot fi de fapt consecința unei „programări modificate”, atunci când un stimul sau o insultă într-un moment critic din viața timpurie are efecte permanente asupra structurii, fiziologiei și metabolismului. Studiile anterioare au arătat că anumite proporții ale corpului la naștere pot oferi o predicție mai puternică și mai specifică a bolii ulterioare decât greutatea la naștere [18]. Făturile IUGR au o masă de grăsime disproporționat de mică comparativ cu masa slabă [19] și o afectare a dezvoltării mușchilor scheletici [20]. Când Barker a studiat diferite măsurători ale nașterii, circumferința abdominală a fost cea mai capabilă să prezică concentrațiile plasmatice ale colesterolului total și LDL și ale apolipoproteinei B. O mică circumferință abdominală la naștere reflectă dimensiunea ficatului și, deoarece metabolismul colesterolului este reglat de ficat, putem deduceți că o creștere hepatică afectată în uter realinează concentrațiile de colesterol cu un profil mai aterogen [21].
Expunerea prenatală la subnutriție și hipoxie determină activarea axului hipotalamo - hipofiză - suprarenală ca răspuns adaptativ la stres. Analizele asupra probelor de sânge din cordonul ombilical au evidențiat niveluri mai ridicate de cortizol și hormoni adrenocorticotropi (ACTH) mai mici în cazurile de IUGR [22]. Restricția creșterii fetale duce la o redistribuire a fluxului sanguin prin reducerea aportului la rinichi și tractul gastro-intestinal și la păstrarea fluxului către creier, miocard și glandele suprarenale [16]. Greutatea redusă la naștere a fost, de asemenea, asociată cu disfuncție endotelială [23] și s-a constatat o creștere a grosimii mediului intima aortic la nou-născuții IUGR la ultrasunete [24].
O sensibilitate sporită la insulină la naștere, urmată de o creștere postnatală accelerată și apariția ulterioară a rezistenței la insulină, este o altă caracteristică a nou-născuților IUGR [25]. Factorul de creștere asemănător insulinei din sângele ombilical (IGF-1) și nivelurile de insulină s-au găsit mai mici pentru nou-născuții IUGR decât pentru bebelușii a căror dimensiune a fost adecvată pentru vârsta gestațională (AGA) [26].
Interesant este că macrosomia fetală coincide cu modificări similare în ceea ce privește dezvoltarea țesutului adipos fetal, modificări permanente în reglarea funcției hormonale și o tendință puternică de obezitate și tulburări metabolice asociate mai târziu în viață [27].
1.3. Biomarcatori pre- și postnatali ai restricției de creștere intrauterină
2. Metode
Principala întrebare de cercetare pentru această revizuire a fost: „Este metabolomica un instrument bun pentru identificarea noilor markeri ai IUGR?” Am căutat (2000–2019) Pubmed, Web of Science și Google Scholar publicații despre metabolomică aplicate cercetărilor IUGR. „Restricție de creștere intrauterină”, „restricție de creștere fetală”, „nou-născut” și „metabolomică” au fost folosite ca cuvinte cheie. De asemenea, ne-am extins căutarea urmărind referințele din articolele identificate. Au fost selectate doar studii originale la om în limba engleză (au fost excluse studiile in vitro și animale). Fiecare document a fost examinat cu atenție de către doi recenzori independenți și s-au extras informații despre criteriile de înscriere, metodele analitice, probele biologice și rezultatele. Numai studiile efectuate pe specimene colectate din sânge din cordonul ombilical sau din fluidele biologice ale nou-născuților au fost reținute pentru această analiză.
- Restricția de energie intermitentă o nouă abordare de scădere în greutate pentru adolescenți
- Prevenirea herniei pentru o creștere continuă!
- HGH pentru scăderea în greutate Comandă online - Hormon de creștere uman injectabil
- HGH de vânzare - Cele mai bune pastile de hormoni pentru creșterea umană # 1 de cumpărat - Alegeri în ChildBirth
- Cum să slăbești ca acest tip care a slăbit 28 de kilograme cu o abordare unică a pierderii în greutate în loc de