Utilizată pentru prima dată în anii 1920, dieta ketogenică este cea mai cunoscută pentru eficacitatea sa stabilită în tratarea epilepsiei intratabile și este cel mai bine cunoscută clinic pentru acest rol. Din păcate, mecanismele dietei ketogene sunt complexe și nu sunt încă pe deplin înțelese. Deși, probabil implică adaptarea metabolică în căile de semnalizare celulară, scăderea excitabilității neuronale și neuroprotecția. Ca atare, este probabil ca dieta ketogenică să se dovedească a fi un tratament eficient chiar și pentru bolile neurologice, inclusiv scleroza laterală amiotrofică (SLA).
În prezent, explorarea efectelor terapeutice ale unei diete ketogene asupra tulburărilor neurologice, altele decât epilepsia, este embrionară, în cel mai bun caz. Astfel, eficacitatea lor în tratarea tulburărilor, altele decât epilepsia, la oameni rămâne speculativă. Cu toate acestea, vom discuta despre potențialele aplicații ale dietei Keto ca tratament pentru SLA.
Simptome ale sclerozei laterale amiotrofice (SLA)
În timp ce bolile neurologice, cum ar fi epilepsia, deficitul de GLUT1, tulburarea bipolară depresivă maniacală și SLA au puțin în comun fiziopatologic, fiecare prezintă anomalii în metabolismul energiei celulare. Și, metabolismul energiei cerebrale modificate indică modificarea funcției mitocondriale. Scleroza laterală amiotrofică (SLA) este o boală rapid progresivă datorată degenerării neuronilor motori ai cortexului cerebral și a cornului anterior al măduvei spinării, care este universal fatală. A luat viața multor persoane, printre care fizicianul Stephen Hawking, campionul la boxe grele Ezzard Mack Charles și legenda de baseball Lou Gehrig, de care boala este numită colocvial.
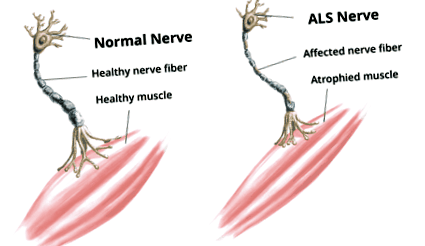
Majoritatea pacienților cu SLA prezintă simptome precum crampe, slăbiciune și atrofie musculară a brațelor sau picioarelor. Mai târziu, slăbiciunea progresează spre antebrațe, umeri și membre inferioare. Fasciculările, spasticitatea, reflexele hiperactive ale tendonului profund, reflexele plantare extensoare, stângăcia, rigiditatea, pierderea în greutate, oboseala și dificultatea de a controla expresia feței și mișcările limbii. Alte simptome includ răgușeala, disfagia și vorbirea neclară. Apoi, pe măsură ce înghițirea devine mai dificilă, pacienții se sufocă adesea cu lichide.
În cele din urmă, moartea este cel mai adesea cauzată de eșecul mușchilor respiratori. 50% dintre pacienții cu SLA mor în decurs de trei ani de la debut, 20% trăiesc timp de cinci ani, iar 10% vor avea o rată de supraviețuire de 10 ani. Supraviețuirea pentru mai mult de 30 de ani este extrem de rară [1]. Stephen Hawking a trăit cu ALS 55 de ani.
Cu alte cuvinte, SLA este o boală degenerativă devastatoare, fără un tratament cunoscut și există puține opțiuni de tratament. Tratamentele pentru SLA includ blocante ale glutamatului precum Riluzole, iar relaxantele musculare sunt administrate pentru a reduce durerea și disconfortul. La fel ca epilepsia, mecanismele patologice exacte care stau la baza SLA nu sunt pe deplin înțelese. Dar ceea ce se știe este că mecanic, ALS implică probabil leziuni oxidative, excitotoxicitate glutamat, inflamație și disfuncție a membranei mitocondriale în celulele nervoase [2, 3, 4].
ALS și dieta ketogenică
Persoanele cu boală prezintă o mutație a genei care codifică superoxidul dismutază cupru/zinc (SOD1) [1]. Deci, atunci când a fost creat un model de șoarece transgenic de SLA în care gena SOD 1-G93A a fost supraexprimată, aceasta a condus la slăbiciune musculară progresivă și la moarte rezultată din insuficiența respiratorie, similar cu ceea ce se întâmplă la oamenii cu SLA. Studiile asupra șoarecilor mutanți SOD 1-G93A mutanți au dat o mulțime de direcții pentru viitoarele studii ALS și tratament.
De exemplu, într-un studiu, șoarecilor mutanți SOD 1-G93A li s-a administrat o dietă ketogenică și s-a constatat că au un număr semnificativ mai mare de neuroni motori - și funcție motoră conservată - comparativ cu șoarecii martor [5]. Autorii au descoperit, de asemenea, că șoarecii mutanți au prezentat o funcție afectată a lanțului de transport al electronilor. Cu toate acestea, administrarea β-hidroxibutiratului corpului cetonic a restabilit activitatea în neuroni, unde funcția lanțului de transport al electronilor a fost fie deja scăzută, fie a fost blocată farmacologic [5]. În timp ce aceste rezultate sunt într-adevăr impresionante, acest studiu nu a indicat o creștere a duratei de viață a șoarecilor mutanți. Cu toate acestea, studiile au constatat că, în modelul de șoarece ALS, șoarecii mutanți hrăniți cu o variantă de dietă ketogenică numită Protocolul Deanna (DP) au arătat progresia întârziată a bolii, au extins speranța de viață și au demonstrat o funcție motoră îmbunătățită în comparație cu martorii [6].
Protocolul Deanna
Protocolul Deanna este un program dezvoltat de Dr. Vincent Tedone, un medic pensionar a cărui fiică, Deanna, are SLA. Protocolul Deanna (DP) solicită o dietă ketogenică și suplimentarea suplimentară. Componentele principale ale Protocolului Deanna includ o dietă ketogenică suplimentată cu alfa ketoglutarat de arginină (AAKG), Nicotinamidă Adenină Dinucleotidă (NAD), GABA, glutation, Idebenonă și Ubiquinol (CoQ10) și trigliceride cu lanț mediu (MCT).
Utilizarea dietei ketogenice în protocolul Deanna are ca scop utilizarea corpurilor cetonice ca substraturi energetice, ocolind astfel transportul limitat de viteză al glucozei către neuronii motorii și mitocondriile compromise. În modelele de șoarece ALS, aceasta are ca rezultat îmbunătățirea performanței și controlului motorului, deficiențelor neurologice întârziate și supraviețuirii extinse [4, 5, 7]. Pacienții SLA care participă la Protocolul Deanna raportează anecdotic creșterea mobilității, a forței și a mersului, precum și o progresie încetinită a bolii [4]. În timp ce sunt necesare cercetări suplimentare pentru a elucida mecanismele care stau la baza acestor rezultate, suplimentarea necesară pentru Protocolul Deanna este ușor disponibilă fără prescripție medicală, iar dieta ketogenică devine mai ușor de urmat. Aceste rezultate sunt promițătoare și oferă posibilitatea ca, prin creșterea cetonelor, dieta ketogenică și variantele sale împreună cu suplimentarea, așa cum este subliniat de Protocolul Deanna, să beneficieze pacienții cu SLA.
Referințe
1. Hulisz, D. (2018). Scleroza laterală amiotrofică: prezentare generală a stării bolii. Am J Manag Care, S320-S326.
2. Vucic, S., Rothstein, J. D. și Kiernan, M. C. (2014). Progrese în tratarea sclerozei laterale amiotrofice: perspective din studiile fiziopatologice. Trends in Neurosciences, 37 (8), 433-442. doi: 10.1016/j.tins.2014.05.006
3. Martin, L.J. (2011). Patobiologie mitocondrială în SLA. J Bioenerg Biomembr 43, 569-579.
4. Ari, C., Poff, A. M., Held, H. E., Landon, C. S., Goldhagen, C. R., Mavromates, N. și D’Agostino, D. P. (2014). Terapia metabolică cu suplimentarea protocolului Deanna întârzie progresia bolii și extinde supraviețuirea în modelul de șoarece al sclerozei laterale amiotrofice (SLA). PLoS ONE, 9 (7), e103526. doi: 10.1371/journal.pone.0103526
5. Zhao, Z., Lange, D.J., Voustianiouk, A., MacGrogan, D., Ho, L., Suh, J., Humala, N., Thiyagarajan, M., Wang, J. și Pasinetti, G.M. (2006). O dietă ketogenică ca o potențială nouă intervenție terapeutică în scleroza laterală amiotrofică. BMC Neurosci 7, 29.
6. D’Alessandro G, Calcagno E, Tartari S, Rizzardini M, Invernizzi RW, și colab. (2011) Interacțiunea dintre glutamat și glutation într-un model neuronal motor al sclerozei laterale amiotrofice relevă metabolismul energetic modificat. Neurobiologia bolii. 43 (2): 346–55.
7. Zhao W, Varghese M, Vempati P, Dzhun A, Cheng A și colab. (2012) Triglicerida caprilică ca o abordare terapeutică nouă pentru îmbunătățirea eficientă a performanței și atenuarea simptomelor datorate pierderii neuronilor motori în boala SLA. Plus unu. 7 (11): e49191.
- Keto After 50 Review - James Wilson Ketogenic Diet Over 50 Book
- Keto și dieta 16 8 m-au ajutat să slăbesc și să-mi repar prediabetul
- Cum să obțineți un pachet de șase urmând o dietă Keto ... LEP Fitness
- Keto Diet 2 Manuscripts in 1 Book Audiobook Ted Duncan
- Keto Diet 101 Mănâncând hrană pentru păsări
