ANETTE JÖNSSON
1 Departamentul de Științe Clinice, Divizia de Medicină Internă, Spitalul Universitar Skåne, Universitatea Lund, 205 02 Malmö, Suedia
ELIN SAND
1 Departamentul de Științe Clinice, Divizia de Medicină Internă, Spitalul Universitar Skåne, Universitatea Lund, 205 02 Malmö, Suedia
2 Departamentul de Științe Medicale Experimentale, Unitatea de Neurogastroenterologie, BMC B11, Universitatea Lund, 221 84 Lund, Suedia
EVA EKBLAD
2 Departamentul de Științe Medicale Experimentale, Unitatea de Neurogastroenterologie, BMC B11, Universitatea Lund, 221 84 Lund, Suedia
BODIL OHLSSON
1 Departamentul de Științe Clinice, Divizia de Medicină Internă, Spitalul Universitar Skåne, Universitatea Lund, 205 02 Malmö, Suedia
Abstract
S-a demonstrat că câțiva pacienți dezvoltă dureri abdominale severe și dismotilitate gastro-intestinală în timpul tratamentului cu analogi ai hormonului de eliberare a gonadotropinei (GnRH). Un model de neuropatie enterică la șobolani a fost dezvoltat prin administrarea de buserelină analogică GnRH la șobolani. A fost descrisă pierderea neuronilor enterici și a ganglioneuritei pe tot tractul gastro-intestinal, fără alte modificări histopatologice. Scopul prezentului studiu a fost investigarea efectelor pe termen lung ale acestui model de șobolan asupra greutății corporale și asupra morfologiei și modificărilor inflamatorii ale tractului gastro-intestinal. Șobolanilor li s-au administrat injecții subcutanate de buserelină sau soluție salină o dată pe zi timp de 5 zile și li s-a permis să se recupereze timp de 3 săptămâni. Acest regim a fost repetat de patru ori. Șobolanii au fost cântăriți săptămânal și au fost sacrificați la 16 săptămâni după al patrulea tratament. Peretele intestinal a fost măsurat prin morfometrie și a fost evaluată prezența neuronilor enterici, mastocitelor, eozinofilelor și limfocitelor T. Șobolanii tratați cu Buserelin s-au dovedit a avea o greutate corporală mai mică la sacrificiu, în comparație cu martorii (P Cuvinte cheie: neuropatie enterică, hormon eliberator de gonadotropină, tract gastrointestinal, model de șobolan
Introducere
Hormonul care eliberează gonadotropina (GnRH) stimulează secreția hormonului foliculostimulant (FSH) și a hormonului luteinizant (LH) din glanda pituitară, care reglează secreția de hormoni steroizi, cum ar fi estrogenul și progesteronul (1). Receptorii GnRH și LH au fost identificați în tractul gastrointestinal uman și de șobolan (GI) (2-4), unde GnRH inhibă proliferarea celulară (5,6). Stimularea LH fragmentează complexul mioelectric care migrează în intestinul subțire (7) și reduce supraviețuirea neuronilor enterici de șobolan în cultură (8). Un număr de pacienți suferă de efecte secundare GI în timpul tratamentului cu analogi GnRH, iar câțiva pacienți dezvoltă pseudo-obstrucție intestinală cronică (CIPO) sau dismotilitate enterică (DE) cu modificări degenerative și inflamatorii în tractul gastrointestinal (3,9).
Studiile anterioare la șobolani au arătat că analogii GnRH provoacă pierderea neuronilor submucoși și myenterici în fund, ileon și colon, fără niciun efect asupra greutății corporale, biomarkeri circulanți inflamatori sau morfometrie a peretelui intestinal (4,10). Numărul de mastocite și eozinofile s-a dovedit a fi nealterat; cu toate acestea, au fost identificate semne de ganglioneurită cu infiltrare a limfocitelor T în ganglionii enterici (4,11). Au fost observate niveluri ridicate de estradiol în plasmă și un strat muscular uterin îngroșat, împreună cu un număr relativ redus de neuroni imunoreactivi la receptorii LH și imunoreactivitate crescută a caspazei-3 activate (4,10). Astfel, tratamentul cu buserelină la șobolani constituie un model de neuropatie enterică la șobolani și se anticipează că pierderea neuronală va fi mediată prin eliberare crescută de LH și hiperactivare a neuronilor enterici purtători de receptor LH (4,10,11), rezultând apoptoza crescută (4)., 12).
Rezultatele anterioare se bazează pe studii în care animalele au fost sacrificate la scurt timp după tratamentul final cu buserelină (4,10,11). Scopul prezentului studiu a fost de a investiga efectul pe termen lung al neuropatiei enterice induse de buserelină asupra greutății corporale și asupra tractului gastrointestinal în ceea ce privește pierderea celulelor neuronale, morfologia și modificările inflamatorii.
Materiale și metode
Animale
Au fost folosiți șobolani Sprague-Dawley femele (n = 20; vârstă, 7 săptămâni; greutate, 170-180 g), achiziționate de la Charles River Laboratories (Sulzfeld, Germania). Șobolanii au fost lăsați să se aclimatizeze la instalația pentru animale controlate de lumină și climă timp de cel puțin 5 zile înainte de experimentare. Chow de șobolan standard (4% grăsime/g) (Lactamin R36, Stockholm, Suedia) și apă au fost furnizate ad libitum. Proiectul experimental a fost aprobat de Comitetul de etică a animalelor, Lund și Malmö, Suedia (M350-12, data aprobării: 14.11.12). Animalele au fost utilizate în conformitate cu Directiva Consiliului Comunităților Europene (2010/63/UE) și Legea suedeză privind bunăstarea animalelor (SFS 1988: 534).
Design de studiu
Șobolanilor (n = 12) li s-a administrat 20 μg de buserelină analogică GnRH (1 mg/ml) (Suprefact, Sanofi-Aventis, Bromma, Suedia) (dizolvat în 0,2 ml soluție salină) subcutanat, o dată pe zi timp de 5 zile, urmat de 3 săptămâni de recuperare, reprezentând o sesiune de tratament (4). Doza și administrarea de buserelină se bazează pe studii anterioare care au demonstrat efecte fiziologice fiabile în ceea ce privește hipertrofia uterină, fără efecte adverse (4,10,13). Animalele martor (n = 8) au primit 0,2 ml injecții saline. Animalele au fost cântărite înainte de includerea în studiu și săptămânal dimineața în timpul studiului. La 30 de săptămâni după începerea studiului și la 4 luni de la ultima ședință de tratament, șobolanii au fost anesteziați cu hidrat de clor (300 mg/kg greutate corporală; C8383; Sigma-Aldrich, St. Louis, MO, SUA) și uciși prin puncție aortică. Probele de țesut din fundul, ileonul distal, colonul proximal și partea distală a cornului uterin au fost colectate și prelucrate pentru evaluare histologică.
Pregătirea țesuturilor
Regiunea fundului/corpului stomacului, ileonului (începând de la 8 cm proximal către cecum și continuând în direcția proximală) și colonului (începând cu 2 cm distal față de cecum și continuând în direcția distală) au fost deschise și aplatizate pe hârtie de filtru . O secțiune din fiecare regiune intestinală a fost fixată în fixativul lui Stefanini (un amestec de 2% formaldehidă (Sigma-Aldrich) și 0,2% acid picric (Sigma-Aldrich) în tampon fosfat, pH 7,2) timp de 22 ore la 4 ° C și altă secțiune și coarnele uterine au fost fixate în paraformaldehidă 4% (Sigma-Aldrich) în tampon fosfat 0,1 M timp de 22 ore la 4 ° C. Specimenele fixate de Stefanini au fost clătite de trei ori în soluția Tyrode conținând zaharoză 10%, înainte de a fi orientate și montate pentru secționarea transversală și longitudinală în Tissue-Tek (Sakura, Histolab, Gothenburg, Suedia), înghețate pe gheață uscată și secționate (10 μm) într-un criostat (HM500; Microm GmbH, Walldorf, Germania). Probele fixate în paraformaldehidă au fost deshidratate în etanol, curățate în xilen, orientate pentru secțiuni transversale și longitudinale, încorporate în parafină și secționate (5 μm). Secțiunile au fost prelucrate pentru imunocitochimie și histochimie.
Histochimie
Morfometria a fost efectuată pe secțiuni scanate, deparafinizate, hidratate și cu parafină colorată cu hematoxilină și eozină (toate Histolab Products AB, Göteborg, Suedia) din coarne uterine secționate transversal și regiuni GI tăiate longitudinal folosind un sistem computerizat de analiză a imaginii (Imagescope, Aperio ScanScope GL SS5082, Vista, CA, SUA). Miometrul și straturile intestinale ale fundului, ileonului distal și colonului proximal (mucoasa și straturile musculare circulare și longitudinale) au fost indicate manual și apoi măsurate folosind un cursor binar computerizat. Valorile medii de 6-10 măsurători reprezentative au fost calculate de la fiecare șobolan în fiecare regiune.
Imunocitochimie
Mastocitele
Colorarea cu albastru de toluidină (Histolab Products AB) a fost efectuată pe secțiuni de parafină pentru a identifica mastocitele din tractul GI (14). Secțiuni din fund, ileon și colon au fost deparafinizate, hidratate și colorate cu 0,1% albastru de toluidină în 60% etanol timp de 60 min la temperatura camerei. Secțiunile transversale și longitudinale ale peretelui întreg au fost scanate și analizate în Imagescope (Aperio ScanScope). Mucoasa, submucoasa și straturile musculare circulare și longitudinale au fost evaluate separat și toate mastocitele au fost numărate pentru cel puțin 12 mm, tăiate la 6-9 adâncimi diferite din fiecare regiune și șobolan. Rezultatele sunt exprimate ca număr de mastocite pe mm lungime regiune a tractului GI.
Eozinofile
Pentru identificarea eozinofilelor a fost utilizată o procedură de colorare bazată pe peroxidază eozinofilă rezistentă la cianură (EPO) (15). Secțiunile crio din fund, ileon și colon au fost spălate în tampon PBS (pH 7,2), DAB (75 mg/100 ml), H2O2 (100 μl/100 ml) și NaCN (50 mg/100 ml) timp de 8 minute și apoi clătit în apă timp de 10 minute înainte de a fi montat în glicerină gelatină (Kaiser, Merck K, Damstadt, Germania). Ambele secțiuni transversale și longitudinale ale peretelui întreg au fost analizate folosind un microscop cu lumină (Olympus BX43, cu camera atașată Nikon XC30, instrument LRI, Hamburg, Germania). Numărul de celule a fost evaluat separat în mucoasa, submucoasa și straturile musculare ale fiecărei regiuni într-un interval de la 0 la +++, unde 0 nu indică celule, + indică câteva celule, ++ indică un număr moderat și + ++ indică un număr mare, așa cum s-a descris anterior (4,15). În regiunile care au prezentat o diferență între grupuri, eozinofilele au fost numărate pentru cel puțin 30 mm, tăiate la 6-9 adâncimi diferite din fiecare regiune și șobolan. Rezultatele sunt exprimate ca număr de eozinofile pe mm sau cm lungime regiune a tractului GI.
Limfocitele T
Prezența limfocitelor T imunoreactive CD3 a fost analizată pe secțiuni de parafină de perete întreg tăiate transversal și longitudinal din fund, ileon și colon. Secțiunile au fost incubate peste noapte cu anticorpi policlonali primari împotriva CD3 crescute la capră (diluare 1: 1.000; nr. Cat. 1127, Santa Cruz Biotechnology, Inc., CA, SUA). Secțiunile au fost apoi expuse la IgG anti-iepure de măgar conjugat DyLight-TM-594 (diluare 1: 1.000; Jackson ImmunoResearch Europe, Ltd., Newmarket, Marea Britanie) timp de 1 oră și montate în tampon fosfat: glicerol 1: 1. Fluoroforul a fost excitat și limfocitele T au fost vizualizate la 488 nm folosind un microscop Olympus BX43.
Limfocitele T au fost evaluate separat în straturi musculare epiteliale, mucoase, submucoase, circulare și longitudinale și seroase ale fundului, ileonului și colonului, într-un interval de la 0 la +++, unde 0 indică lipsa celulelor, + indică puține, + + indică un număr moderat, iar +++ indică un număr mare, așa cum s-a descris anterior (4,15). Au fost numărate doar acele regiuni care au prezentat o diferență între grupuri, pentru cel puțin 20 mm lungime GI, tăiate la 6-9 adâncimi diferite din fiecare regiune și șobolan. Rezultatele sunt exprimate ca număr de limfocite T per mm lungime regiune a tractului GI.
analize statistice
Mastocitele
În fund, numeroase celule adipoase au fost identificate în submucoasă și în stratul muscular circular, cu o variație individuală ridicată, independentă de tratament (Fig. 4A și B). În ileon și colon, mastocitele au fost găsite doar în submucoasă, fără nicio diferență între grupuri (Fig. 4C și D).
Numărul de mastocite analizate în (A) SM și (B) CM în fundus și în SM ale ileonului (C) și colonului (D), între șobolani tratați cu ser fiziologic sau buserelină. Numărarea celulelor a fost efectuată pe secțiuni transversale și longitudinale, cu pereți întregi. C = 8 șobolani și B = 11 șobolani. Rezultatele sunt prezentate ca date individuale și mediane. Testul U Mann-Whitney a fost utilizat pentru analiză. SM, submucoasa; CM, strat muscular circular; C, martor tratat cu ser fiziologic; B, buserelin.
Eozinofile
Discuţie
Un număr redus de neuroni myenterici din ileon și colon au fost detectați la șobolanii tratați cu buserelină, comparativ cu martorii din prezentul studiu pe termen lung. Tratamentul cu Buserelin a dus la o greutate corporală mai mică la sfârșitul studiului, un strat muscular mai subțire circular în ileon, un strat muscular mai subțire longitudinal în colon, un număr crescut de eozinofile în submucoasa ileonului și un număr mai mare de Limfocitele T în submucoasa fundului și straturile musculare circulare ale fundului și colonului, comparativ cu martorii.
La șaisprezece săptămâni după ultima sesiune de tratament, în săptămâna de studiu 32, șobolanii tratați cu buserelină au prezentat o pierdere a neuronilor myenterici în ileon și colon, așa cum s-a descris în studiile anterioare în care șobolanii au fost sacrificați la scurt timp după terminarea tratamentului (4, 10). În conformitate cu studiile anterioare, pierderea neuronală a fost mai pronunțată în ileon și colon decât în fund și în neuronii myenterici decât în neuronii submucoși (4,10). Regenerarea neuronilor enterici și a celulelor gliale este posibilă, deoarece au fost identificate celule progenitoare specifice țesutului (16,17), iar studiile la șoareci au arătat regenerarea neuronilor după leziuni intestinale (18). Cu toate acestea, amploarea pierderii neuronale myenterice a fost aceeași cu cea determinată în studiile anterioare (4,10), chiar dacă șobolanii actuali au fost ținuți în viață timp de 16 săptămâni.
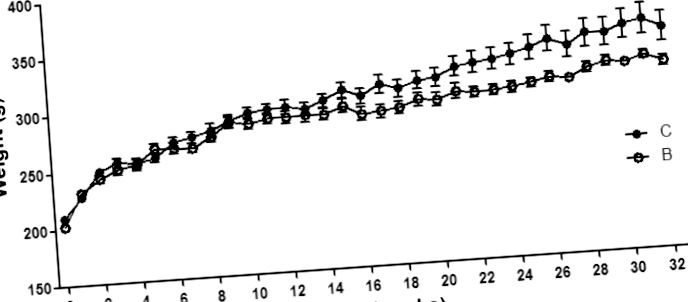
Diferența de greutate corporală între grupuri a început în săptămâna 23 și nu a fost observată în studiile pe termen scurt care s-au încheiat în săptămâna 16 și 18 (4,10), ceea ce sugerează că daunele care apar în timpul tratamentului conduc în cele din urmă la malnutriție. Sistemul nervos enteric (ENS) are un impact asupra digestiei și absorbției nutrienților, în special a carbohidraților și a grăsimilor (19,20) și s-a observat un conținut crescut de grăsimi în fecale după tratamentul cu buserelină (10). Neuropatia enterică poate duce astfel la malnutriție la șobolani, precum și la pacienți (3.9). Hormonii sexuali stimulează consumul crescut de alimente, iar nivelurile scăzute de estradiol din plasmă s-au dovedit a reduce consumul de alimente (21). Într-un studiu anterior, nu a fost identificată nicio diferență în greutatea corporală; cu toate acestea, nivelurile plasmatice de estradiol au fost crescute și stratul muscular uterin a fost îngroșat după tratamentul cu buserelină (10). Grosimea neafectată a miometrului din prezentul studiu sugerează niveluri normalizate de hormoni sexuali după încetarea tratamentului, iar efectele negative ale neuropatiei asupra absorbției de nutrienți intestinali nu pot fi contracarate prin creșterea poftei de mâncare și aportul alimentar secundar nivelurilor crescute de hormoni sexuali, ca explicație presupusă pentru reducerea greutatea corporală în urmărirea actuală pe termen lung.
În concluzie, urmărirea pe termen lung a neuropatiei enterice indusă de buserelină la un model de șobolan arată pierderea ireversibilă a neuronilor myenterici. În al doilea rând, modificările histopatologice ale GI au fost agravate în timp și șobolanii au prezentat straturi musculare mai subțiri și un număr crescut de eozinofile și limfocite T. În plus, creșterea în greutate corporală este redusă în timp. Viitoare studii mecaniciste sunt necesare pentru a explica fiziopatologia care stă la baza neuropatiei enterice și modificările asociate.
Mulțumiri
Fundația Regelui Gustaf V și Regina Victoria Free Mason's, Dezvoltarea Regiunii Skåne, Fundația Bengt Ihre, Fundația Lundström și Societatea Regală Fiziografică din Lund. Autorii doresc să îi mulțumească Anna Themner Persson pentru asistența sa tehnică.
- Urmărirea pe termen lung a programului de telemonitorizare de reducere a greutății „Controlul activ al corpului”
- Multe femei au pierdut în greutate pe termen lung după abdomen, raportează o intervenție chirurgicală plastică și reconstructivă
- Impactul distribuției grăsimii corporale asupra rezultatelor clinice pe termen lung după implantarea stentului cu eluare a medicamentului
- Urmărirea sfaturilor privind stilul de viață îmbunătățește controlul glicemic, redox și starea inflamatorie la pacienții cu
- Pierderea în greutate pe termen lung este fără speranță; Dr. Dawn MacLaughlin