Abstract
fundal
Este larg acceptat faptul că sindromul metabolic este asociat cu un risc crescut de boli renale cronice (CKD). Pentru a investiga dacă sindromul metabolic coexistent este o condiție necesară pentru BCR la supraponderali și obezi.
Metode
Un studiu de cohortă pe 6852 de persoane chineze din august 2007 până în decembrie 2012. Examinările au inclus un chestionar, măsurători fizice și prelevare de sânge. Raporturile de pericol pentru incidentul CKD au fost estimate în funcție de combinațiile categoriei IMC și absența sau prezența sindromului metabolic.
Rezultate
Pentru CKD, raporturile de pericol ajustate multivariabile vs. persoanele cu greutate normală fără sindrom metabolic au fost de 1,31 (95% CI, 0,89-1,92) în excesul de greutate și 2,39 (95%) CI, 1,27-4,52) la obezi fără sindrom metabolic și 1,54 (95% CI, 1,18-3,95) în greutate normală, 2,06 (95%) CI, 1,27-3,36) la supraponderali și 2,77 (95%) CI, 1.42–4.31) la obezi cu sindrom metabolic. Nu au existat interacțiuni între IMC și absența sau prezența sindromului metabolic cu risc de BCR atunci când IMC a fost clasificat (greutate normală, supraponderalitate, obezitate) (P = 0,17). În rândul persoanelor cu și fără sindrom metabolic s-au înregistrat creșteri ale incidenței cumulative a CKD de la greutatea normală până la persoanele supraponderale la cele obeze (tendința log-rank) P = 0,04 până la P
fundal
În studiul de față, am testat ipoteza că supraponderabilitatea și obezitatea cu și fără sindrom metabolic sunt asociate cu un risc crescut de boli cronice de rinichi. În acest scop, am studiat apariția CKD la 6852 subiecți fără CKD la momentul inițial 2007 până în 2012 în sudul Chinei centrale și le-am clasificat în funcție de indicele lor de masă corporală (IMC) ca greutate normală, supraponderală sau obeză și în funcție de absență sau prezență a sindromului metabolic.
Metode
Cohorta de studiu
Examinări de bază
Sindromul metabolic
Sindromul metabolic a fost definit utilizând criteriile Panoului de tratament III pentru adulți (NECP-ATP-III) din Programul Național de Educație pentru Colesterol ca ≥ 3 din următoarele 5 componente metabolice: 1) circumferință ridicată a taliei: ≥ 90 cm (masculi) sau ≥ 80 cm) 2) trigliceride crescute: ≥ 1,69 mmol/l sau utilizarea medicamentelor lipidice; 3) tensiune arterială crescută: tensiune arterială sistolică ≥ 130 mmHg sau tensiune arterială diastolică ≥ 85 mmHg sau utilizarea medicamentelor antihipertensive; 4) nivel ridicat de glucoză în repaus alimentar: ≥ 5,6 mmol/l sau utilizarea medicamentelor pentru diabet; 5) HDL-c redus: 2) = 175 × (Scr în metoda enzimatică) -1.234 × vârstă - 0.287 (× 0.79, dacă este femeie) [14]. Diagnosticul proteinuriei s-a făcut folosind un test cu joja de urină. S-a considerat că proteinuria pozitivă este prezentă pentru un rezultat al jojei de ≥ 1+, corespunzător unui nivel de proteină urinară> 30 mg/dL [15]. CKD a fost definită ca proteinurie pozitivă sau eGFR 2 .
Urmărire și rezultate
Rezultatele primare au fost definite ca apariția CKD la momentul controlului anual din 2007 până în 2012. Dacă un participant a experimentat mai mult de un eveniment CKD în timpul urmăririi, doar primul rezultat pentru individ a contribuit la analiza rezultatului. Data apariției CKD a fost definită ca punctul de mijloc între ultima dată când subiecții nu aveau CKD și prima dată când subiectul a fost diagnosticat cu CKD. Perioada de urmărire a fost definită ca numărul de zile de la data observării până la data diagnosticului de BCR sau la data controlului final. În mod similar, un eGFR 2 sau o proteinurie pozitivă izolată au fost analizate ca rezultate primare individuale. Rezultatele secundare au fost definite ca un compozit de CKD sau deces din toate cauzele.
Analize statistice
Toate analizele statistice au fost efectuate utilizând software-ul SAS, versiunea 8.1 (SAS Institute, Inc.). Analize ale varianțelor și χ Au fost utilizate 2 teste pentru a compara valorile și frecvențele medii. Incidențele cumulate au fost reprezentate grafic folosind curbele Kaplan-Meier și s-a folosit un test log-rank pentru a compara curbele de incidență. Modele de regresie a riscurilor proporționale cu Cox raporturile de risc (HR) estimate pentru BCR ajustate multifactorial pentru vârstă, sex, fumat, nivel plasmatic de colesterol lipoproteic cu densitate scăzută, utilizarea medicamentelor antihipertensive/hipolipemiante/antidiabetice, precum și inactivitatea fizică și valoarea probabilității pentru omogenitate au fost estimată prin adăugarea unui termen de interacțiune la modelul statistic. Procentul de exces de risc de BCR pentru un model de bază, incluzând IMC și caracteristicile clinice, care a fost explicat prin sindromul metabolic, a fost calculat utilizând formula: procent de risc în exces = [(HRcon adj - HRcon + med adj)/(HRcon adj - 1) ] × 100%, unde HRcon adj este HR-ul ajustat pentru confundator pentru CKD și HRcon + med adj este confundatorul și mediatorul - HR ajustat [16].
Rezultate
Caracteristicile inițiale ale celor 6852 de indivizi incluși în studiu sunt văzute în Tabelul 1 stratificat după categoria IMC (greutate normală, supraponderal, obez) și prin absența sau prezența sindromului metabolic. Dintre aceștia, 3864 persoane (56,4%) aveau greutate normală, 2508 supraponderale (36,6%) și 480 persoane (7,0%) erau obeze. Sindromul metabolic a fost prezent la 6,0% din greutatea normală, la 26,2% din excesul de greutate și la 57,5% dintre persoanele obeze. Caracteristicile stratificate în funcție de sex sunt prezentate în tabelele 2. Dintre cei 3704 participanți de sex masculin, 1432 au avut greutate normală (38,7%), 1876 au fost supraponderali (50,6%) și 396 persoane (10,7%) au fost obezi. Numerele corespondente dintre cele 3148 de femei participante au fost 2432 (77,3%), 632 (20,1%) și 84 (2,7%), respectiv.
În cursul unei perioade medii de urmărire de 54,3 luni, dintre cei 6852 de participanți, numărul pacienților cu debut de BCR a fost de 776 subiecți, care au inclus doar un eGFR Fig. 1
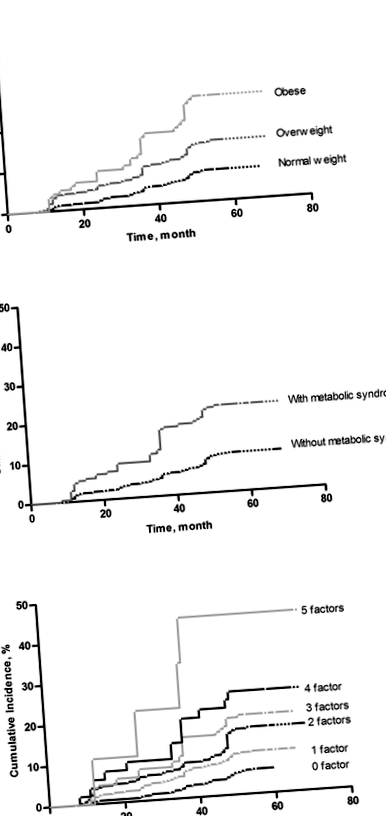
Curbele Kaplan-Meier pentru incidentul cumulativ al bolii renale cronice (CKD) în funcție de categoria indicelui de masă corporală (IMC) și sindromului metabolic. A Raporturile de pericol (HR) pentru bolile renale cronice (CKD) în funcție de categoria indicelui de masă corporală (IMC). b HR pentru CKD în funcție de sindromul metabolic. c HR pentru CKD în funcție de componentele sindromului metabolic
Când indivizii au fost împărțiți în grupuri în funcție de categoria lor de IMC (greutate normală, supraponderalitate, obezitate) și absența sau prezența sindromului metabolic, riscul de BCR a crescut cu o categorie IMC mai mare, independent de prezența sau absența sindromului metabolic (Tabelul 3). Pentru CKD, HR ajustate multivariabile vs. indivizii cu greutate normală fără sindrom metabolic au fost 1,31 (IÎ 95%, 0,89-1,92) la supraponderali și 2,39 (IÎ 95%, 1,27-4,52) și indivizii obezi fără sindrom metabolic și 1,54 (IÎ 95%, 1,18-3,95) în greutate normală, 2,06 (95% CI, 1,27-3,36) la supraponderali și 2,77 (95% CI, 1,42-4,31) la persoanele obeze cu sindrom metabolic. Nu au existat interacțiuni între IMC și absența sau prezența sindromului metabolic cu risc de BCR atunci când IMC a fost clasificat (greutate normală, supraponderalitate, obezitate) (P = 0,17). Stratificarea pentru sex a dat estimări de risc ușor mai mari pentru BCR la bărbați, dar rezultate atenuate la femei.
În rândul persoanelor fără sindrom metabolic, s-au înregistrat incidențe cumulative crescânde ale CKD de la greutatea normală până la persoanele supraponderale la cele obeze (tendința log-rank) P FIG. 2
Curbele Kaplan-Meier pentru incidentul cumulativ al bolii renale cronice (CKD) după categoria indicelui de masă corporală stratificat prin absența/prezența sindromului metabolic. A Raporturile de pericol (HR) pentru bolile renale cronice (CKD) după categoria indicelui de masă corporală fără sindrom metabolic. b HR pentru CKD după categoria indicelui de masă corporală cu sindrom metabolic. c HR pentru CKD cu vs. fără sindrom metabolic
Așa cum se arată în fișierul suplimentar 1: Tabelul S1, procentul de exces de risc mediat de sindromul metabolic în asocierea dintre IMC (ca variabilă continuă) și CKD a fost de 26,1%; adică 26,1% din mărimea efectului asociat al IMC asupra riscului de CKD se explică prin sindromul metabolic. Când IMC a fost clasificat (greutate normală, supraponderal, obez), această proporție a crescut la 33,3%.
Discuţie
În acest studiu de cohortă al unei populații urbane chineze generale, riscul de BCR la supraponderalitate și obezitate a fost semnificativ crescut, independent de prezența sau absența sindromului metabolic.
plasament și colab. [25] s-a constatat că obezitatea este asociată cu un risc crescut de a dezvolta IRC în stadiul 3, care nu a mai fost semnificativ după ajustarea factorilor de risc cunoscuți ai bolilor cardiovasculare. În contrast, mai multe studii au descoperit un risc crescut de CKD la supraponderali și obezi chiar și după ajustarea covariabilelor de bază [18, 26]. Inconsistențele dintre aceste studii anterioare pot fi cauzate de diferențe în definirea CKD și/sau criteriile de selecție a cohortei. De asemenea, studiile cu dimensiuni mici ale eșantionului sau cu un număr redus de evenimente pot să nu aibă suficientă putere statistică pentru a discrimina diferențele. Din câte știm, prezentul studiu este cel mai mare până în prezent, incluzând atât bărbați, cât și femei din diferite grupe de vârstă în limba chineză. Rezultatele noastre sugerează că supraponderalitatea și obezitatea, chiar și în absența sindromului metabolic, nu sunt condiții benigne pentru funcția renală.
Obezitatea poate contribui la dezvoltarea CKD prin căi legate de rezistența la insulină care pot provoca leziuni renale, cum ar fi activarea sistemului renină-angiotensină-aldosteron, activarea căilor de semnalizare a insulinei/factorului de creștere asemănător insulinei, stresul oxidativ, suprimarea al receptorului gamma activat de proliferator peroxizom, afectarea țesuturilor legate de inflamație, nefroscleroza și activarea sistemului simpatic renal [4, 27]. Hipotensiunea glomerulară/hiperfiltrarea ca declanșator al progresiei CKD în excesul de greutate/obezitate este evidențiată de observațiile recente [28]. Între timp, există dovezi crescânde că acumularea de lipide și modificările citokinelor celulelor adipoase se pot traduce prin modificări inflamatorii la nivelul rinichilor [4].
Unele limitări ale studiului nostru trebuie luate în considerare la evaluarea rezultatelor noastre. În primul rând, studiul nostru s-a desfășurat într-un singur centru dintr-un mare spital urban de predare, iar populațiile studiate au fost participanți la un control anual de sănătate care ar putea duce la o prejudecată de selecție datorită unei supra-reprezentări a persoanelor supraponderale și obeze relativ sănătoase. O altă limitare este că nu am avut detalii despre medicamente care ar putea tinde să subestimeze efectul potențial al agenților. În cele din urmă, diagnosticul de BCR în acest studiu a depins de valoarea creatininei sau proteinuriei pozitive cu o singură ocazie și, prin urmare, este mai predispus la clasificare greșită.
Ca o problemă globală de sănătate publică, obezitatea este un factor cauzal fundamental în dezvoltarea sindromului metabolic. Cu toate acestea, pe baza prezentelor date, este rezonabil să sugerăm că, chiar și în absența sindromului metabolic, strategiile de sănătate publică ar trebui să se concentreze pe a ajuta persoanele să-și reducă expunerea la un mediu care promovează obezitatea.
De asemenea, deoarece adipozitatea abdominală pare să preceadă apariția altor anomalii ale sindromului, supraponderalitatea și obezitatea pot fi la unii indici un semn de avertizare timpurie pentru viitoarele tulburări metabolice. Modelele animale au arătat că restricția calorică întârzie leziunile renale și aceste efecte pot fi mediate de reglarea în sus a expresiei Sirt1, care este exprimată abundent în medula renală internă și în celulele interstițiale medulare și probabil protejează celulele interstițiale medulare de stresul oxidativ [29, 30 ]. În plus față de acest studiu, la oamenii cu BCR, intervențiile non-chirurgicale de scădere în greutate reduc proteinuria și tensiunea arterială [31]. Mai mult, la persoanele cu obezitate morbidă, cu hiperfiltrare glomerulară, intervențiile chirurgicale bariatrice normalizează RFG și reduc tensiunea arterială și microalbuminuria [32]. În plus, efectul antiproteinuric al ECA pare a fi maxim la pacienții supraponderali/obezi și mai puțin proeminent la pacienții cu IMC normal, sugerând un rol al hiperfiltrării glomerulare în patogeneza proteinuriei în obezitate [33]. Astfel, pierderea în greutate și menținerea pe termen lung a acestei pierderi în greutate ar putea fi încurajate la persoanele supraponderale și obeze, indiferent de prezența sau absența sindromului metabolic, pentru a reduce riscul de leziuni renale legate de obezitate.
Concluzie
În concluzie, excesul de greutate și obezitatea cu sau fără sindrom metabolic sunt asociate cu un risc crescut de BCR la populația generală. Aceste constatări sugerează că excesul de greutate și obezitatea, chiar și în absența sindromului metabolic, nu sunt condiții benigne și că pierderea în greutate ar putea fi încurajată, indiferent de prezența sau absența sindromului metabolic, pentru a reduce povara BCR. Descoperirile noastre sugerează, de asemenea, că prezența sindromului metabolic crește riscul de CKD, asocierile nu sunt puternice și sunt similare asociațiilor observate între supraponderalitate și obezitate și incidentul CKD. Deși hipertensiunea și diabetul sunt mediatori importanți, pot exista și căi suplimentare. Sunt necesare mai multe studii clinice pentru a evalua impactul supraponderalității și obezității asupra incidenței și progresiei bolilor renale.
- Ramadanul de post la pacienții cu afecțiuni renale cronice Efecte clinice și biochimice Bernieh B, Al
- Excesul de greutate crește riscul de boli renale severe - Nuffield Department of Primary
- Postul în Ramadan nu este asociat cu deteriorarea bolii renale cronice A prospective
- CNC supraponderal și obezitate la vârsta de 14 ani
- Efectele exercițiilor aerobice asupra somnului acasă la bărbații supraponderali și obezi cu cronică