Brian Y. Hsueh
1 Microbiologie și genetică moleculară, Michigan State University, East Lansing, MI, 48824, SUA
Christopher M. Waters
1 Microbiologie și genetică moleculară, Michigan State University, East Lansing, MI, 48824, SUA
Abstract
Infecțiile cu holera cauzate de gamma-proteobacterium Vibrio cholerae au devastat populațiile umane de secole, iar pandemiile de holera au afectat toate colțurile globului. Din fericire, intervenții precum terapia de rehidratare orală, antibiotice/antimicrobiene și vaccinuri au salvat nenumărate persoane afectate de holeră, iar noi intervenții precum probiotice și terapia cu fagi sunt dezvoltate ca abordări promițătoare pentru a trata și mai multe infecții cu holeră. Deși terapiile actuale sunt în cea mai mare parte eficiente și pot reduce transmiterea bolilor, focarele de holeră rămân mortale, așa cum s-a observat în timpul recentelor focare din Haiti, Etiopia și Yemen. Acest lucru se datorează unor complicații politice și socio-economice semnificative care stau la baza, inclusiv lipsa vaccinurilor și a alimentelor și a apei curate și a lipsei supravegherii sănătății. În această revizuire, subliniem punctele tari și punctele slabe ale terapiilor actuale pentru holeră, discutăm despre tehnologiile emergente și susținem că este necesară o abordare flexibilă și multilaterală pentru a continua să reducem povara globală a holerei.
Introducere
Obiectivul acestei revizuiri este de a descrie strategiile actuale de terapie de rehidratare orală (ORT), antibiotice și vaccinare care sunt utilizate pentru a trata și preveni holera. (A se vedea Figura 1 pentru o prezentare generală.) De asemenea, subliniem noi abordări emergente pentru tratarea și prevenirea holerei - cum ar fi tratamentul cu probiotice și terapia cu fagi - care au demonstrat succes în condiții de laborator, dar nu sunt încă utilizate în populațiile umane. Deoarece focarele de holeră sunt adesea legate de infrastructura slabă, lipsa accesului la apă curată sau perturbări societale, părerea noastră este că este necesară o strategie flexibilă și multipluă pentru a combate aceste infecții și fiecare dintre aceste strategii de tratament poate satisface o nevoie specifică. pentru a reduce povara holerei (Figura 1).
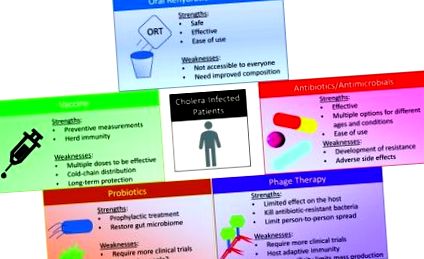
figura 1.
Această diagramă rezumă punctele tari și punctele slabe ale a cinci tratamente diferite pentru holera discutate în această revizuire. Luând în considerare punctele tari și punctele slabe ale terapiilor actuale și valorificând diversitatea resurselor și noilor tehnologii, o abordare cu mai multe direcții ar putea îmbunătăți șansele de succes în combaterea infecțiilor cu holeră la nivel mondial și ar putea stabili soluții rentabile, preventive, mai rapid decât metode convenționale de tratament.
Terapia de rehidratare orală
Deși modificarea ingredientelor ORT pentru a obține absorbția optimă a Na + și a apei în intestine reduce simptomele, rămân cazuri în care ORT nu a putut ține sub control simptomele holerei. De exemplu, deshidratarea severă necesită rehidratare intravenoasă. Deoarece ORT nu este 100% eficientă, tratamente concomitente precum antibiotice/antimicrobiene 23-25 și vaccinarea 26 pot fi necesare pentru a susține reducerea simptomelor holerei, așa cum se va discuta în următoarele două secțiuni.
Antibiotice/Antimicrobiene
Deși aceste clase de antibiotice pot obține efecte terapeutice pozitive, este important să se ia în considerare efectele secundare adverse ale acestor tratamente. Reacțiile de hipersensibilitate sunt cel mai frecvent efect secundar care pune viața în pericol în tratamentul antibiotic al holerei, în timp ce starea neregulată a ritmului cardiac este frecventă numai la ciprofloxacină și azitromicină 24. ORT și terapia cu antibiotice funcționează pentru tratarea infecțiilor cu holera, dar nu împiedică pacienții să dobândească holera. Prin urmare, următoarea intervenție despre care vom discuta care are potențialul de a limita infecțiile cu holeră la populațiile sensibile este vaccinurile.
Vaccinuri
OMS pledează pentru utilizarea vaccinurilor orale împotriva holerei (OCV), incluzând atât vaccinuri cu celule orale întregi (WC) atenuate în viață, cât și inactivate, în zone endemice sau în timpul focarelor, ca protecție tranzitorie, deoarece s-au dovedit a fi eficiente în combinație cu alte tratamente corelative, inclusiv antibiotice, ORT și managementul sănătății 17, 28. OCV stimulează în principal imunitatea mucoasei mediată de anticorpi, în special IgA, împotriva agentului patogen. Acești anticorpi sunt direcționați împotriva antigenelor, cum ar fi polizaharida specifică O1 și CT 28. Deși IgA are circulație sistemică limitată (
6 luni), celulele B de memorie care sunt responsabile pentru prevenirea infecției cu holeră persistă și se pot extinde și diferenția rapid în plasmablaste și în cele din urmă celule plasmatice, care pot resemna anticorpi de protecție la activarea antigenului 28. Mai mult, OCV-urile ar putea oferi imunitate turmei adulților nevaccinați, dar efectul la copiii nevaccinați necesită un studiu suplimentar 29 .
În afară de vaccinurile V. cholerae inactivate, vaccinul viu atenuat oral Vaxchora (CVD 103-HgR) este un vaccin administrat în SUA pentru alimente și medicamente, aprobat, care protejează împotriva serotipului Inaba sau Ogawa și conține CTB din ambele. biotip clasic și El Tor 2, 30, 33. Datorită protecției solide și rapide mediată de celule a Vaxchora, eficacitatea sa împotriva holerei este estimată la aproximativ 90% după vaccinare și 80% la 3 luni după vaccinare la călătorii în zonele cu risc crescut de holeră 2, 30, 33. Pașii următori pentru dezvoltarea Vaxchora sunt evaluarea siguranței și eficacității acesteia în populațiile endemice de holeră și optimizarea pregătirii vaccinului, deoarece se bazează pe transportul în lanțul rece și amestecarea apei, care sunt problematice pentru distribuția în unele regiuni endemice sau perturbate 33 .
Mai multe forme alternative de vaccinuri sunt în curs de dezvoltare și acestea includ un vaccin combinat cu veziculă cu membrană externă (OMV) împotriva V. cholerae și Escherichia coli care sa dovedit a induce un răspuns imunogen puternic 12, o formă manipulată genetic de V. cholerae viu fără factorii diareici care mediază protecția de tip probiotic împotriva holerei 34 și glicoconjugații antimicrobieni, în special epitopii lipopolizaharidelor din diferite serotipuri (Ogawa și Inaba) 35. Aceste forme alternative de vaccinuri nu sunt încă în studiile clinice.
Utilizarea eficientă a vaccinurilor pentru prevenirea sau reducerea focarelor de holeră se bazează în mare măsură pe cercetări epidemiologice, deoarece diferite regiuni endemice au nevoie de vaccinuri distincte pentru a viza tulpinile circulante divergente. Mai mult, vaccinurile ideale împotriva holerei nu vor depinde de transportul cu lanțul rece. În plus față de aceste trei tratamente, care sunt utilizate în prezent, apar noi abordări pentru prevenirea sau tratarea infecțiilor cu holeră.
Probiotice
Un concept emergent în microbiologie este capacitatea microbiomului gazdă de a preveni sau limita infecțiile. Un concept relativ nou pentru V. cholerae, această idee începe să fie explorată ca tratament sau prevenire a infecțiilor cu holera. Datorită acumulării excesive de lichide, V. cholerae provoacă o perturbare severă a microbiomului intestinal în timpul infecției, astfel încât majoritatea bacteriilor găsite în scaunele caracteristice de apă de orez sunt V. cholerae 36. În plus, sistemul de secreție de tip VI al V. cholerae poate furniza toxine efectore către microbiomul intestinal sau poate modula celulele gazdă în sine, ambele modificând microbiota intestinului pentru a facilita colonizarea 37, 38. Din aceste motive, restaurarea microbiomului intestinal sau prevenirea colonizării prin tratament probiotic este o nouă abordare promițătoare pentru tratarea infecțiilor cu holeră.
Probioticele sunt adesea luate cu antibiotice și cu alte medicamente, inclusiv adjuvanți antiinflamatori, dar efectul secundar advers al medicamentelor asupra probioticelor justifică testarea ulterioară 43. Cu toate acestea, probioticele care reduc holera pot limita tulpinile de V. cholerae rezistente la antibiotice prin reducerea cantității de antibiotice utilizate 41, 42. Mai mult, probioticele ar putea servi ca un tratament mai bun în regiunile în care pregătirea vaccinului cu lanț de frig nu este fezabilă și nu este disponibilă apă curată 40 .
Terapia cu fagi
Un alt tratament nou pentru holera implică utilizarea terapeutică a bacteriofagilor litici. Terapia cu fagi a fost utilizată de zeci de ani în Europa de Est și Rusia și, odată cu apariția bacteriilor rezistente la antibiotice, a fost dezvoltată și utilizată pentru tratarea infecțiilor cauzate de Pseudomonas, Salmonella și Staphylococcus 45. Terapia cu fagi are multe avantaje față de antibiotice. De exemplu, fagii sunt capabili să omoare bacteriile rezistente la antibiotice, cantitatea de fagi crește proporțional cu numărul de bacterii infectante, iar fagii exercită un impact minim asupra microbiomului rezident 45. Această strategie de tratament este inspirată de ciclul natural de viață al V. cholerae, în care florile de bacterii în timpul focarelor sunt urmate de expansiunea bacteriofagilor litici, în primul rând ICP1, ICP2 și ICP3, care în cele din urmă reduc populația de bacterii viabile 46, 47 .
Un studiu realizat pe un model de șoarece pentru sugari a arătat că un cocktail din cei trei bacteriofagi virulenți ai ICP ar putea reduce efectiv încărcătura V. cholerae după provocare într-o manieră dependentă de doză din cauza replicării rapide a fagului și a capacității de a ucide bacteriile 48. Deși prezintă rezultate promițătoare la modelele animale, terapia cu fagi pentru holeră necesită mai multă optimizare pentru eficacitatea și calendarul său pentru a fi avansate la studiile clinice 48. Terapia cu fagi ar putea fi, de asemenea, utilizată pentru a limita răspândirea de la persoană la persoană, deoarece chiar și un număr mic din acești fagi litici s-ar putea extinde rapid în timpul infecțiilor cu V. cholerae.
Deși terapia cu fagi are multe caracteristici promițătoare, are și dezavantaje potențiale. În timpul terapiei cu fagi, sistemul imunitar adaptiv al gazdei poate genera anticorpi care neutralizează fagii, care ar putea inhiba capacitatea lor de a liza bacteriile vizate in vivo sau de a preveni tratamentele ulterioare 45. Ca și în cazul antibioticelor, V. cholerae va evolua rezistența la infecția cu fagi și, prin urmare, cea mai probabilă aplicare a fagilor ar necesita un cocktail de fag litic care ar necesita mutații independente multiple pentru rezistență. Datorită legăturii complexe dintre V. cholerae și fagii litici, această bacterie codifică mecanisme de apărare moleculară pentru a limita infecția cu fagi 49. Datorită specificității gazdei, care are un impact semnificativ asupra dezvoltării și testării tratamentului, producției în masă și distribuției terapiei cu fagi, nu sunt încă practice 50. Înainte ca terapia cu faguri să fie validată ca terapeutică pentru holeră, trebuie să existe o evaluare a răspunsului imunologic la fagi și a eficacității în timpul focarelor de holeră.
Concluzii
Note
[versiunea 1; evaluare inter pares: 2 aprobate]
Declarație de finanțare
Această lucrare a fost susținută de subvențiile Institutelor Naționale de Sănătate GM109259 și AI130554 și de către Fundația Națională pentru Știință MCB1714612 către CMW.
Finanțatorii nu au avut niciun rol în proiectarea studiului, colectarea și analiza datelor, decizia de publicare sau pregătirea manuscrisului.
Note
Notă editorială privind procesul de revizuire
Recenziile Facultății F1000 sunt comandate de la membrii prestigioasei Facultăți F1000 și sunt editate ca un serviciu pentru cititori. Pentru ca aceste recenzii să fie cât mai cuprinzătoare și accesibile posibil, arbitrii furnizează informații înainte de publicare și este publicată doar versiunea finală, revizuită. Arbitrii care au aprobat versiunea finală sunt enumerați cu numele și afilierile lor, dar fără rapoartele lor despre versiunile anterioare (orice comentarii vor fi deja abordate în versiunea publicată).
Arbitrii care au aprobat acest articol sunt:
Jeffrey Withey, Departamentul de Biochimie, Microbiologie și Imunologie, Wayne State University School of Medicine, Detroit, Michigan, SUA
Jyl Matson, Departamentul de Microbiologie Medicală și Imunologie, Universitatea din Toledo Colegiul de Medicină și Științe ale Vieții, Toledo, OH, SUA
- Izbucnirea holerei în Nigeria se răspândește la Lagos, ucide 3 ~ Îngrijirea sănătății, Sfaturi de slăbire, Nutriție,
- Toxina holerei - o prezentare generală Subiecte ScienceDirect
- Holeră și sănătate - Sfaturi de sănătate, articole și știri despre holeră și sănătate
- TARA VERDE
- Pulbere de scoarță de crampă, 1 oz (Viburnum opulus) - Penn Herb Co