Abstract
fundal
Silimarina derivată din planta de ciulin de lapte „Silybum marianum” este compusă din patru flavonolignani majori. Studiile clinice și experimentale indică efectele hepatoprotectoare ale silimarinei. Cu toate acestea, mecanismele de bază sunt doar înțelese incomplet.
Scopul acestui studiu a fost de a evalua efectul administrării orale a unui extract de silimarină definit în modelul leziunii hepatice induse de tetraclorură de carbon acută (CCl4).
Metode
O doză unică de extract de silimarină (SE; 20 sau 100 mg/kg greutate corporală) a fost administrată șobolanilor prin gavaj oral. Ulterior, șobolanilor li s-a injectat o doză unică de CCl4 (2 ml/kg greutate corporală).
Rezultate
După 24 de ore, analiza raportului greutate ficat-corp, nivelurile serice de transaminaze și analiza histologică au relevat o afectare hepatică marcată, care a fost inhibată de SE într-o manieră dependentă de doză. Expresiile induse de CCl4 ale genelor pro-inflamatorii și pro-fibrogene au fost reduse semnificativ la șobolanii tratați cu SE. Analiza moleculară a relevat că SE a redus expresia chemokinei pro-inflamatorii MCP-1, a citokinei pro-fibrogene TGF-beta, precum și a colagenului I din celulele stelate hepatice umane izolate (HSC), care sunt celulele efectoare cheie ale fibrozei hepatice.
Concluzie
Administrarea orală a extractului de silimarină testat a inhibat afectarea hepatocelulară într-un model de leziuni hepatice acute. Mai mult decât atât, am descoperit recent că extractul de silimarină a avut efecte directe asupra expresiei genelor pro-inflamatorii și pro-fibrogene în HSC. in vitro. Acest lucru indică faptul că efectele directe asupra HSC contribuie, de asemenea, la in vivo efectele hepatoprotectoare ale silimarinei și promovează în continuare potențialul său ca agent anti-fibrogenic și în bolile hepatice cronice.
fundal
Silimarina (COM)Silybum marianum) este un produs medicamentos pe bază de plante care constă dintr-un amestec de patru izomeri flavonolignan, și anume silibina, izozilibina, silidianina și silicristina cu formula empirică C25H22O10 Silibina este componenta majoră și cea mai activă și reprezintă aproximativ 60-70% din silimarină, urmată de silicristină (20%), silidianină (10%) și izozilibină (5%). Mai multe studii au arătat silimarina ca medicament pe bază de plante hepatoprotector [5, 15, 18].
Unul dintre modelele studiate cel mai frecvent în contextul leziunilor hepatice acute este modelul de hepatotoxicitate indusă de carbontetraclorură (CCl4). Se știe că hepatotoxicitatea indusă de CCl4 provine din metaboliții săi foarte letali, cum ar fi radicalii triclorometil (CCl3 •) și peroxi triclorometil (CCl3OO •), care sunt generați de citocromul microsomal P450 (CYP) în ficatul mamiferelor [19]. CCl3 • poate reacționa cu o varietate de molecule celulare importante din punct de vedere biologic, cum ar fi proteinele, lipidele și acizii nucleici. Acest lucru determină afectarea funcției hepatice care poate afecta procesele celulare cruciale care duc la leziuni hepatocelulare [20, 27]. S-a demonstrat că silimarina este protejată împotriva hepatotoxicității induse de CCl4 prin eliminarea radicalilor liberi și a speciilor reactive de oxigen [13, 22]. Mai mult, au fost descrise proprietăți antiinflamatorii și anti-fibrotice (revizuite în [1]). În timp ce câteva studii au investigat eficacitatea silimarinei într-un model cronic de CCl4 la aplicarea orală și în ceea ce privește reacția fibrogenă [6, 16]. Am studiat pentru prima dată efectele acute ale extractului de ciulin de lapte administrat pe cale orală asupra evenimentelor timpurii din dezvoltarea fibrozei.
Activarea HSC este evenimentul cheie al fibrozei hepatice. Activarea acestor celule are loc ca răspuns la leziunile hepatice ale bolilor hepatice cronice. La activarea HSC, HSC își schimbă fenotipul în celule asemănătoare miofibroblastelor cu producție crescută de componente ale matricei extracelulare (ECM), cum ar fi colagenul de tip I [8, 17]. Mai mult, HSC activat contribuie la inflamația hepatică ca răspuns la leziuni hepatice acute, precum și cronice, prin sintetizarea diverselor citokine și chemokine, cum ar fi proteina-1 chimiotratantă monocitară (MCP-1) [24].
Scopul acestui studiu a fost de a evalua efectul unui extract definit de silimarină (SE; Silimarit®) împotriva daunelor hepatocelulare induse de CCl4, precum și asupra expresiei genelor pro-inflamatorii și pro-fibrogene. Mai departe, am interpretat in vitro analiză în care am investigat efectele aceluiași extract asupra expresiei genice a HSC uman activat. Am demonstrat că aplicarea extractului protejat de leziunea hepatică indusă de CCl4 într-o manieră dependentă de doză. Mai mult, datele noastre indică faptul că efectele directe asupra HSC activat au contribuit la efectele hepatoprotectoare ale extractului de silimarină.
Metode
Produse chimice
Tetraclorura de carbon (CCl4) și uleiul de porumb au fost obținute de la Sigma Pharmaceuticals (Hamburg, Germania). Pentru tratamentul animalelor, a fost utilizat extractul uscat Silimarit® (SE, extract de ciulin de lapte conform Pharmacopoea Europaea, Bionorica SE, Neumarkt, Germania). Pentru dizolvarea extractelor, a fost preparată o soluție apoasă de metil hidroxipropil celuloză (MHPC, 0,5%, methocel ™ E4M prem).
Izolarea și stimularea celulelor stelate hepatice activate
Celulele stelate hepatice (HSC) au fost izolate din probele de ficat utilizând un procedeu de perfuzie EGTA/colagenază modificat în 2 etape [28]. Ulterior, HSC-urile au fost purificate prin ultracentrifugare în gradient de arabinogalactan [11]. HSC-urile au fost cultivate în mediul Eagle modificat (DMEM) al lui Dulbecco suplimentat cu 10% FCS, 100 UI/ml penicilină și 100 μg/ml streptomicină într-o atmosferă 95% aer/5% CO2 umidificat. Pentru inducerea in vitro activare, HSC proaspăt izolate au fost însămânțate pe vase de plastic neacoperite timp de două săptămâni [11].
Animale și model de leziuni hepatice acute
Șobolanii Sprague-Dawley au fost obținuți de la Laboratoarele Charles River (Sulzfeld, Germania). Animalele au fost adăpostite în facilitățile pentru animale de la Universitatea din Regensburg și hrănite cu o dietă standard. Pentru in vivo aplicarea SE a fost suspendată în soluție 0,5% de MHPC și administrată șobolanilor masculi în vârstă de șase săptămâni la o singură doză de 20 sau 100 mg/kg greutate corporală (BW) prin gavaj oral (n = 4-5/grup). Șobolanii martor (n = 5) au primit solvent MHPC prin gavaj oral. După 3 ore, șobolanilor li s-a injectat i.p cu o singură doză de tetraclorură de carbon (CCl4) (1 ml/kg BW.; 1: 1, v/v în ulei de porumb) sau un volum egal de solvent (ulei de porumb). La 24 de ore după injecția CCl4, șobolanii au fost sacrificați prin puncție cardiacă sub anestezie profundă cu ketamină/xilazină (2: 1) și au fost recoltate probe de țesut hepatic și sânge pentru analize ulterioare. Ficatele și sângele de la animalele tratate cu HPMC/ulei de porumb au servit drept controale.
Histologie
Pentru analiza histologică, specimenele de țesut hepatic au fost fixate timp de 24 de ore în 4% formalină la temperatura camerei, deshidratate cu etanol gradat și încorporate în parafină. Secțiunile de țesut (grosimea de 5 μm) au fost deparafinizate cu xilen și colorate cu hematoxilină și eozină (H&E). Colorarea hepatică pentru Ki67 (un marker de regenerare) a fost examinată folosind o procedură imunohistochimică standard, așa cum este descris [3]. Numărul de celule cu balon sau hepatocite Ki67 pozitive a fost numărat în 4 zone selectate aleatoriu pe fiecare secțiune.
Analiza cantitativă în timp real a PCR
Izolarea ARN din țesuturile hepatice sau celulele cultivate și transcrierea inversă au fost efectuate așa cum s-a descris [10]. PCR cantitativ în timp real a fost realizat aplicând tehnologia LightCycler (Roche) [10] folosind seturi specifice de teste QuantiTect Primer conform instrucțiunilor producătorului (Qiagen, Hilden, Germania). Amplificarea ADNc derivat din ARNr 18s (pentru: 5'-TGATTAAGTCCCTGCCCTTTGT; rev: 5'-GATCCGAGGGCCTCACTAAAC) a fost utilizată pentru normalizare.
Analiza nivelurilor de colagen hepatic
Probele de ficat au fost supuse analizei colagenului solubil în acid-pepsină utilizând testul Sircol Collagen (Biocolor, Carrickfergus, Marea Britanie) conform instrucțiunilor producătorului.
Cuantificarea nivelurilor de proteine MCP-1
Nivelurile de proteine MCP-1 din supernatantul de cultură celulară au fost analizate utilizând testul imunologic Quantikine Human MCP-1 (sisteme de cercetare și dezvoltare, Wiesbaden, Germania) conform instrucțiunilor producătorului.
analize statistice
Valorile sunt prezentate ca medie ± SEM. Comparația între grupuri a fost făcută utilizând studenții nepereche t-Test. O valoare p
Rezultate
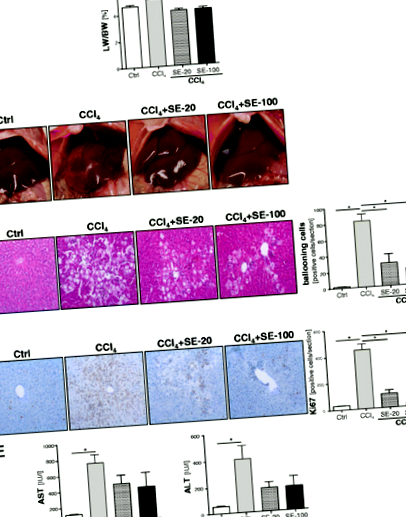
Efectul extractului de silimarină (SE) asupra afectării hepatocelulare în modelul leziunii hepatice acute induse de CCl4
Efectul extractului de silimarină (SE) asupra expresiei genelor pro-inflamatorii și pro-fibrogene în modelul leziunii hepatice acute induse de CCl4
Hemoxigenaza-1 (HMOX-1) este o enzimă esențială în catabolismul hemului, care este indus de stresul oxidativ. PCR cantitativă în timp real a relevat o inducție semnificativă a expresiei HMOX-1 ca răspuns la tratamentul CCl4 (Fig. 2a). Această creștere a HMOX-1 a fost abrogată în mod dependent de doză de SE, indicând stresul oxidativ redus (Fig. 2a).
Stresul oxidativ este un inductor bine cunoscut al unei reacții pro-inflamatorii și, în conformitate cu aceasta, am observat o inducere semnificativă a nivelurilor de expresie hepatică a mARN-ului factorului de necroză tumorală (TNF) și interleukinei-1 beta (IL-1ß) în CCl4 -ficatul rănit (Fig. 2b și c). Inducerea TNF și IL-1ß a fost semnificativ redusă de SE într-o manieră dependentă de doză (Fig. 2b și c).
Efectul extractului de silimarină (SE) asupra expresiei genelor pro-inflamatorii și pro-fibrogene în celulele stelate hepatice activate
in vivo datele au indicat faptul că SE a afectat expresia genelor pro-inflamatorii și pro-fibrogene în HSC. Cu toate acestea, nu au permis diferențierea, indiferent dacă acesta este un efect indirect prin intermediul reducerea leziunilor și inflamației țesuturilor sau dacă SE prezintă, de asemenea, un efect direct asupra HSC. Pentru a aborda această întrebare, am stimulat HSC uman activat primar cu SE in vitro. Interesant, am constatat că SE a redus semnificativ expresia mARN a MCP-1 și TGF-beta în HSC într-o manieră dependentă de doză (Fig. 3a, b). Analiza nivelurilor de proteină MCP-1 în supernatantele culturii celulare a confirmat acest rezultat la nivelul proteinei (Fig. 3c). Mai mult, expresia colagenului-I, proteina matricei extracelulare predominante în țesuturile umane fibrotice, a fost afectată semnificativ de stimularea SE a HSC-urilor activate in vitro (Fig. 3d). Împreună, aceste descoperiri au indicat faptul că SE afectează direct expresia genei pro-inflamatorii și pro-fibrogene a HSC activat.
Discuţie
La om, precum și la rozătoare, biotransformarea CCl4 este mediată în principal de CYP2E1 și foarte marginal de alte CYP (CYP2B și CYP3A) (revizuite în [27]). În consecință, șoarecii knockout CYP2E1 sunt rezistenți la hepatotoxicitatea CCl4 [29]. Un studiu recent efectuat cu cobai (Cavia porcellus) au arătat o expresie hepatică crescută a CYP2E1 ca răspuns la administrarea cronică de alcool, în timp ce suplimentarea cu silimarină a redus semnificativ această inducție în comparație cu grupul de abținere a alcoolului [2]. Aici, am constatat că tratamentul cu CCl4 a cauzat o scădere considerabilă a expresiei hepatice CYP2E1, ceea ce a fost în concordanță cu un studiu anterior realizat de Wong și colab. [29]. Interesant, efectul inhibitor CCl4 asupra expresiei CYP2E1 a fost atenuat prin tratamentul cu SE. Aceste descoperiri indică faptul că silimarina are un efect modulant asupra expresiei hepatice a CYP2E1, care poate fi modificată de diferite hepatotoxine. Împreună, efectele hepatoprotectoare și efectul anti-fibrotic al SE combinate cu absența toxicității îl fac un bun candidat pentru investigații clinice suplimentare.
Important, al nostru in vitro studiile efectuate pe HSC uman primar au arătat că SE afectează direct expresia factorilor pro-fibrogenici în HSC. Aceste date indică faptul că efectele directe ale SE asupra HSC contribuie și la efectul hepatoprotector al SE in vivo. În ceea ce privește efectul SE asupra HSC și, respectiv, a expresiei genelor pro-fibrogene, trebuie remarcat faptul că am aplicat SE oral în studiul nostru. După administrarea orală, nivelurile maxime de Silibinin, o componentă majoră a SE, sunt atinse în ficat, plămâni și stomac [31].
Concluzii
În concluzie, am constatat că extractul de silimarină studiat a prezentat efecte hepatoprotectoare profunde într-un model de leziuni hepatice acute prin intermediul diferite mecanisme. În special, efectele inhibitoare asupra factorilor fibrogeni din acest model, precum și efectele directe anti-fibrogene ale extractului asupra HSC uman in vitro indicați în plus potențialul acestui compus natural în prevenirea și tratamentul fibrozei hepatice la pacienții cu boală hepatică (cronică).
- Efectul extractului hidroalcoolic al membranelor septice din nucă de nucă asupra termenului de valabilitate al tradiționalului
- Efectul extractului de coacăz negru din Noua Zeelandă asupra răspunsurilor fiziologice în repaus și în timpul brisk
- Tinctură de mărar (Anethum Graveolens), extract de lichid organic, Shi Luo, supliment de plante 64 oz
- Compararea capsulelor de octreotidă orală cu analogii injectabili de somatostatină în acromegalie - Text integral
- Efecte secundare frecvente și rare pentru ameliorarea menstruației orale