Ben J. Jones
Secția de medicină de investigație, spitalul Hammersmith, Imperial College London, clădirea Commonwealth la etajul 6, Du Cane Road, Londra, W12 0NN UK
Stephen R. Bloom
Secțiunea de medicină de investigație, spitalul Hammersmith, Imperial College London, clădirea Commonwealth la etajul 6, Du Cane Road, Londra, W12 0NN UK
Abstract
Există o nevoie urgentă de terapii farmacologice eficiente pentru a ajuta la combaterea epidemiei în creștere a obezității și a crizei medicale pe care o prezintă. În ultimii 3 ani a fost aprobată o serie de noi medicamente anti-obezitate. Majoritatea acestor influențează căile apetitului hipotalamic prin semnalizarea dopaminergică sau serotoninergică. Unele sunt terapii combinate, permițând doze mai mici pentru a minimiza potențialul de efecte în afara obiectivelor. O abordare alternativă este de a imita semnale de satietate endogenă folosind forme de lungă durată de hormoni periferici care suprimă apetitul. Există, de asemenea, un interes considerabil în direcționarea termogenezei de către țesutul adipos maro pentru a crește cheltuielile de energie în repaus. Farmacoterapia obezității a cunoscut mai multe zori false, dar o mai bună înțelegere a căilor care reglementează echilibrul energetic și studii mai bine concepute oferă mult mai multă încredere că agenții recent aprobați vor fi atât eficienți, cât și siguri. Cu toate acestea, o serie de aspecte legate de dezvoltarea preclinică și clinică continuă să atragă dezbateri și încă sunt necesare studii suplimentare la scară largă pentru a aborda domeniile de incertitudine.
Puncte cheie
| Pentru prima dată în peste un deceniu, mai multe medicamente noi au fost autorizate pentru gestionarea greutății pe termen lung. |
| Reducerea în greutate poate fi realizată farmacologic prin reducerea poftei de mâncare, creșterea cheltuielilor de energie sau ambele. |
| Înțelegerea îmbunătățită a homeostaziei energetice a oferit noi ținte terapeutice. |
Introducere
Prevalența globală în creștere a obezității amenință să inverseze îmbunătățirile speranței de viață observate în ultimele decenii. În prezent, 600 de milioane de adulți, 13% din populația globală, sunt obezi, definiți ca având un indice de masă corporală (IMC) ≥30 kg/m 2 [1]. O creștere substanțială a obezității la copii este un motiv special de îngrijorare, deoarece IMC-ul copilului persistă adesea până la maturitate [2, 3]. Proiecțiile actuale anticipează că 20% dintre adulți vor fi obezi până în 2030 [4].
Obezitatea crește riscul de boli cardiometabolice, demență, boli de rinichi, cancer, boli respiratorii și osteoartrita. Acest lucru prezintă provocări enorme de asistență medicală pentru viitor. Măsurile preventive pentru combaterea factorilor determinanți de mediu ai obezității la nivel de populație sunt esențiale, dar până acum au fost insuficient aplicate pentru a inversa tendința. Prin urmare, sunt necesare tratamente eficiente pentru indivizi. Intervențiile privind stilul de viață pot fi eficiente, dar răspunsurile inadecvate sunt observate la o proporție semnificativă de pacienți. În ciuda programului standard de aur utilizat în studiul Look AHEAD, doar 46% dintre pacienți au obținut o pierdere în greutate cu 5% [5]. Mai mult, recâștigarea greutății este obișnuită atunci când se termină aspectul intensiv al programelor de stil de viață [6]. Chirurgia bariatrică duce la pierderea în greutate susținută și beneficii pe termen lung pentru sănătate [7], dar prezintă o rată mică, dar semnificativă a mortalității perioperatorii și un risc de complicații pe termen lung, iar mulți pacienți aleg să nu fie supuși unei proceduri invazive pentru a-i ajuta să piardă. greutate.
Prin urmare, există un stimulent clar pentru a dezvolta tratamente farmacologice eficiente pentru a ajuta la pierderea în greutate. În această revizuire, rezumăm fiziologia homeostaziei energetice pentru a dezvălui ținte farmacologice pentru reducerea greutății, înainte de a discuta despre tratamentele trecute și actuale, agenții noi în curs de desfășurare, obstacolele de reglementare cu care se confruntă și poziția lor în managementul general al obezității.
Strategii pentru pierderea în greutate farmacologică
Mediul, comportamentul și trăsăturile genetice influențează greutatea corporală. Cu toate acestea, calea comună finală pentru fiecare dintre acești factori dispariți este modificarea aportului de energie sau a cheltuielilor de energie. Obezitatea rezultă din dezechilibrul energetic susținut de mai mulți ani, iar tratamentele pentru obezitate pot funcționa numai inversând acest lucru. În consecință, toți agenții anti-obezitate au cel puțin unul dintre următoarele efecte:
Reduceți aportul de alimente sau absorbția nutrienților.
Creșteți cheltuielile energetice legate de odihnă sau de activitate.
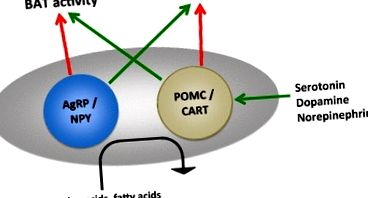
Schema simplificată a căilor de reglare a energiei hipotalamice. Alte căi, inclusiv circuitele de recompensă, sunt implicate în apetitul și consumul de energie, dar înțelegerea rolului central al hipotalamusului este utilă pentru a aprecia mecanismele de acțiune ale mai multor agenți de slăbire. AgRP peptidă legată de agouti, BAT țesut adipos maro, transcripție CART cu cocaină și amfetamină, GLP-1 glucagon-like peptide-1, NPY neuropeptidă Y, POMC pro-opiomelanocortină, PYY peptidă YY
Cum sunt judecate medicamentele pentru slăbit?
O scurtă istorie a farmacoterapiei anti-obezitate
Agenți anti-obezitate în uz curent
În ciuda unei istorii nepotrivite, recunoașterea viitoarelor crize de sănătate provocate de epidemia de obezitate și o mai bună înțelegere a mecanismelor fiziologice care stau la baza apetitului și a homeostaziei energetice, au condus la progrese semnificative în domeniul farmacoterapiei obezității. În ultimii 4 ani a fost aprobată o serie de agenți noi. Totuși, nu toți au fost întâmpinați cu aprecieri universale; doi agenți (lorcaserin și fentermină/topiramat) nu au reușit să obțină aprobarea pentru utilizare în Europa. În general, atât FDA, cât și EMA au recunoscut unele incertitudini legate de siguranță și eficacitate cu noii agenți; cu toate acestea, FDA a considerat că riscul raportului beneficii este acceptabil pentru probleme specifice care trebuie abordate cu studii post-introducere pe piață, în timp ce EMA a cerut obținerea de date suplimentare înainte de acordarea licenței.
Orlistat
Singurul supraviețuitor din era pre-2010 este orlistat (comercializat ca Xenical), un inhibitor de lipază activ intestinal, care reduce absorbția grăsimilor cu 30% [45]. Estimările cumulate din studiile pe termen lung indică o pierdere în greutate susținută de 2,9% față de placebo atunci când sunt administrate la doza standard de 120 mg de trei ori pe zi [46]. De asemenea, s-a observat o progresie redusă către diabet [47] și un control glicemic îmbunătățit la pacienții care au deja diabet [48]. Malabsorbția grăsimilor poate da naștere la efecte secundare, inclusiv scaune uleioase, urgență fecală și pete dacă pacienții continuă să consume o dietă bogată în grăsimi, dar acestea pot fi evitate cu o restricție dietetică adecvată. Într-adevăr, se presupune că eficacitatea orlistatului reflectă probabil schimbări alimentare impuse mai degrabă decât o reducere directă a absorbției caloriilor [49].
Lorcaserin
Fentermină/Topiramat
Bupropion/Naltrexone
Liraglutidă
Evoluții viitoare probabile
Recunoașterea persistenței BAT termogene la vârsta adultă a dus la un interes intens asupra posibilelor modalități de a exploata acest lucru farmacologic. Dincolo de expunerea la frig, activitatea simpatică este cel mai cunoscut activator al BAT; pacienții cu feocromocitom au depozite extinse de BAT [81]. Pentru a fi util din punct de vedere clinic, un agent simpatomimetic ar trebui să fie relativ specific pentru BAT pentru a evita sechelele cardiovasculare. Prin urmare, ținta cea mai promițătoare ar putea fi adrenoreceptorul β3, care este exprimat la niveluri ridicate în BAT [82], deși se găsește și în țesutul adipos alb, tractul gastro-intestinal, prostata și vezica urinară [83, 84]. S-a descoperit recent că un agonist β3, mirabegron, stimulează consumul de energie la oameni [85]. În acest caz, cu toate acestea, s-au observat creșteri ale ritmului cardiac și ale tensiunii arteriale, indicând probabil acțiune la alți adrenoreceptori. Succesul acestei abordări poate depinde deci de generarea de agenți cu o selectivitate mai bună pentru adrenoceptorul β3 sau de metode alternative de activare a BAT. O dezvoltare ulterioară este posibilitatea ca o subpopulație de adipocite albe să aibă potențialul de a fi „rumenită”, formând țesut adipos „bej” activ din punct de vedere termogen și crescând capacitatea de irosire a energiei terapeutice [86].
Poziția farmacoterapiei în gestionarea obezității
Măsurile privind stilul de viață sunt o parte esențială a oricărui plan de tratament pentru obezitate și oferă beneficii pentru sănătate, independent de pierderea în greutate. Cea mai bună dovadă a eficacității lor este cu programe intensive care abordează dieta, activitatea și factorii comportamentali [33, 94, 95]. Cea mai puternică intervenție pentru pierderea în greutate este chirurgia bariatrică, care duce la o reducere medie a greutății corporale cu 25-33%, în funcție de procedura chirurgicală. Chirurgia bariatrică este superioară abordărilor non-chirurgicale în ceea ce privește pierderea în greutate și remisiunea diabetului, cel puțin pe termen scurt-mediu [96]. Cu toate acestea, pacienții sunt expuși riscului de complicații chirurgicale obișnuite, inclusiv moarte perioperatorie, scurgeri anastomotice și infecții, precum și probleme pe termen mai lung care reflectă alterarea fiziologiei gastro-intestinale, cum ar fi sindromul de dumping, hipoglicemia, malabsorbția micronutrienților și colelitiaza [97-99]. Implicațiile resurselor și riscurile de complicații înseamnă că intervenția chirurgicală este în general limitată la pacienții cu un IMC ≥40 kg/m 2 sau ≥35 kg/m 2 la cei cu o comorbiditate asociată obezității [100, 101].
Pentru persoanele care nu doresc să fie supuse (sau nu îndeplinesc criteriile pentru) intervenții chirurgicale bariatrice, dar nu sunt în măsură să piardă în greutate doar prin stilul de viață, farmacoterapia este un adjuvant util. Agenții de slăbire sunt, în general, autorizați pentru utilizare la pacienții cu un IMC ≥30 kg/m 2 sau ≥27-28 kg/m 2 la cei cu o comorbiditate asociată cu obezitatea [102]. Alegerea agentului trebuie să reflecte preferințele pacientului, co-indicațiile relative (cum ar fi diabetul pentru liraglutidă) și contraindicațiile (cum ar fi tulburările convulsive pentru bupropion/naltrexonă) și eficacitatea relativă (vezi Tabelul 1). Pierderea în greutate trebuie evaluată la 3 luni, iar tratamentul trebuie întrerupt sau înlocuit dacă nu s-a realizat cel puțin 5% pierdere în greutate.
tabelul 1
Caracteristicile agenților farmacologici autorizați în prezent pentru pierderea în greutate pe termen lung
| Orlistat (Xenical) | 120 mg de trei ori pe zi (imediat înainte, în timpul sau după mese) | Inhibitor de lipază intestinală | 3,0% [46] | Frecvente/ușoare: scaune uleioase, malabsorbție a vitaminelor liposolubile (se recomandă multivitamine) B rar/sever: poate reduce absorbția unor medicamente, cum ar fi ciclosporina și unele antiretrovirale, colelitiaza | Sindroame de malabsorbție, colestază, sarcină/alăptare |
| Lorcaserin (Belviq) | 10 mg de două ori pe zi | 5-HT2C agonist | 3,0–3,6% [50, 51] | Frecvente/ușoare: cefalee, greață, gură uscată, amețeli, oboseală, constipație Rare/severe b: sindrom serotoninergic, boli cardiace valvulare, tulburări cognitive, priapism, hipoglicemie | SSRI/SNRI și medicamente conexe, insuficiență cardiacă congestivă coexistentă, valvulopatie, sarcină |
| Fentermină/topiramat (Qsymia) | Doza inițială 3,75 mg/23 mg zilnic, doza standard de întreținere 7,5 mg/46 mg zilnic, cea mai mare doză 15 mg/92 mg zilnic | Norepinefrină + eliberare de dopamină/modulație GABA | 6,6% la doza standard, 8,6-9,3% la cea mai mare doză [58, 59] | Frecvente/ușoare: parestezie, amețeli, gust modificat, insomnie, constipație, gură uscată B rar/sever: teratogen, tahicardie, miopie acută și glaucom secundar cu unghi închis, tulburări cognitive, acidoză metabolică, creșterea creatininei, hipoglicemie | Sarcina, boli cardiovasculare recente sau instabile, glaucom, hipertiroidism, inhibitori MAO sau amine simpatomimetice |
| Bupropion/naltrexonă (Contrave, Mysimba) | 16 mg/180 mg de două ori pe zi, titrat timp de 4 săptămâni | Inhibitor al recaptării dopaminei + norepinefrină/antagonist opioid | 3,2-5,2% [64-67] | Frecvente/ușoare: greață, constipație, cefalee, vărsături, amețeli, insomnie, gură uscată, diaree Rare/severe b: gânduri suicidare, convulsii, hipertensiune arterială, hepatotoxicitate, glaucom cu unghi închis, hipoglicemie | Tulburări convulsive, hipertensiune arterială necontrolată, anorexie nervoasă, sevraj de alcool sau opiacee, tulburare bipolară, boală renală în stadiu final, inhibitori MAO |
| Liraglutidă 3 mg (Saxenda) | 3 mg zilnic prin injecție subcutanată, titrat timp de 5 săptămâni | Agonist al receptorului GLP-1 | 4,0-6,0% [70, 71] | Frecvente/ușoare: greață, vărsături Rare/severe b: pancreatită acută, tumori ale celulelor tiroidiene C, boală a vezicii biliare, tahicardie, insuficiență renală, hipoglicemie | Carcinom tiroidian medular, neoplazie endocrină multiplă, gastropareză, sarcină |
5-HT serotonină, acid gamma-aminobutiric GABA, GLP-1 peptidă asemănătoare glucagonului-1, monoaminooxidază MAO, inhibitor al recaptării serotoninei/noradrenalinei SNRI, inhibitor selectiv al recaptării serotoninei SSRI
a Nu am enumerat toate efectele adverse raportate
b Am inclus evenimente adverse care nu s-au dovedit în mod concludent că sunt legate de tratament în categoria „rare/severe”
Pe lângă intervenția chirurgicală și farmacoterapia, procedurile de intervenție non-chirurgicală pentru obezitate reprezintă o nouă dezvoltare interesantă, care ar putea lărgi opțiunile de gestionare a pierderii în greutate în viitor. De exemplu, sistemul EndoBarrier este un manșon inserat endoscopic, care reproduce unele aspecte ale by-passului gastric Roux-en-Y prin accelerarea livrării nutrienților către intestinul subțire distal [103]. Dispozitivele implantabile de blocare a nervului vagal sunt concepute pentru a exploata semnalele de sațietate mediată vag pentru a reduce consumul de alimente [104] și au fost recent aprobate de FDA. În timp ce aceste abordări mai puțin invazive sunt mai ușor reversibile și mai puțin susceptibile de a provoca complicații pe termen lung decât chirurgia bariatrică, ele pot fi efectuate numai în centre specializate; în consecință, rolul continuu al farmacoterapiei în gestionarea greutății este asigurat.
Concluzie
Mulțumiri
Secțiunea de medicină de investigație, Imperial College London, este finanțată prin subvenții de la Consiliul de cercetare medicală (MRC), Consiliul de cercetare a biotehnologiei și științelor biologice (BBSRC) și Institutul Național pentru Cercetări în Sănătate (NIHR); un premiu de consolidare a capacității de biologie integrativă a mamiferelor (IMB); și o subvenție FP7-HEALTH-2009-241592 EuroCHIP. De asemenea, este susținut de schema de finanțare a Centrului Imperial de Cercetare Biomedică NIHR. Ben Jones este finanțat de o bursă MRC de cercetare clinică.
Conflict de interese
Autorii declară că nu există conflicte de interese.
- Medicamentul pentru scăderea în greutate Belviq pare sigur pentru inimă, arată studiul
- Medicamentul pentru slăbit pare să condimenteze lucrurile Medicilon Inc.
- Medicamentul pentru slăbit Belviq a fost retras de pe piață din cauza riscului crescut de cancer
- Medicamentul pentru slăbit Belviq crește riscul de cancer, avertizează FDA; Știri-Medical
- Interacțiuni medicamentoase cu Wellbutrin