Piotr Ladyzynski
1 Institutul Nalecz de Biocibernetică și Inginerie Biomedică al Academiei Poloneze de Științe, strada Trojdena 4, 02-109 Varșovia, Polonia; [email protected]
Janusz Krzymien
2 Departamentul de Diabetologie și Medicină Internă, Universitatea de Medicină din Varșovia, str. Banacha 1A, 02-097 Varșovia, Polonia; [email protected] (J.K.); [email protected] (M.R.); lp.ude.muw@baidnilk (B.B.)
Piotr Foltynski
1 Institutul Nalecz de Biocibernetică și Inginerie Biomedică al Academiei Poloneze de Științe, strada Trojdena 4, 02-109 Varșovia, Polonia; [email protected]
Monika Rachuta
2 Departamentul de Diabetologie și Medicină Internă, Universitatea de Medicină din Varșovia, str. Banacha 1A, 02-097 Varșovia, Polonia; [email protected] (J.K.); [email protected] (M.R.); lp.ude.muw@baidnilk (B.B.)
Barbara Bonalska
2 Departamentul de Diabetologie și Medicină Internă, Universitatea de Medicină din Varșovia, str. Banacha 1A, 02-097 Varșovia, Polonia; [email protected] (J.K.); [email protected] (M.R.); lp.ude.muw@baidnilk (B.B.)
Date asociate
Abstract
1. Introducere
Diabetul este una dintre bolile cronice care necesită multă atenție atât din partea pacientului, cât și a echipei de asistență medicală. Indiferent de tipul de diabet, pacienții necesită informații complete despre boală prin educație continuă și promovarea comportamentelor de căutare a sănătății, precum și monitorizarea regulată a glucozei, planuri individuale de tratament și un diagnostic precoce pentru a preveni amenințările la adresa sănătății asociate cu complicațiile diabetului. Telemedicina oferă o serie de instrumente care ar putea fi de ajutor în alegerea planului corect de tratament, sprijinirea acțiunilor de schimbare a stilului de viață al pacientului, consolidarea motivației în ceea ce privește activitățile legate de sănătate, facilitarea capacității pacientului de a-și auto-monitoriza și controla starea și de a atinge obiectivul dorit. obiectiv terapeutic.
Sistemele automate sau semi-automate de analiză a imaginii alimentelor pentru evaluarea dietei sunt în continuă dezvoltare. Aceștia obțin o precizie de recunoaștere sub 90% atunci când sunt testați pe baze de date care conțin până la câteva sute de imagini de mese/feluri de mâncare [15]. În ultimii ani, s-au dezvoltat traductoare de imagine care realizează fotografii în serie, documentând etapele consecutive ale consumului de masă și permițând estimarea cantității unei resturi de masă nemâncată [16]. Unele dintre aceste dispozitive de înregistrare a vieții, cum ar fi camera Microsoft SenseCam, împreună cu datele obținute dintr-un jurnal alimentar convențional, permit îmbunătățirea preciziei calculelor aportului de calorii [17]. De asemenea, au fost raportate abordări alternative, care se bazează pe descrierea vocală a meselor [18,19] sau monitorizarea activităților legate de consumul de masă, de exemplu, mestecarea sau înghițirea [20,21].
Toți subiecții și-au dat consimțământul în cunoștință de cauză pentru includere înainte de a participa la studiu. Studiul a fost realizat în conformitate cu Declarația de la Helsinki, iar protocolul a fost aprobat de Comitetul de Etică al Universității Medicale din Varșovia (KB/16/2014).
Pentru fiecare participant, a fost colectat un istoric medical unificat, referitor la dieta și obiceiurile alimentare, activitatea fizică, terapia cu insulină (cu accent deosebit pe bolusurile de insulină și perfuzia bazală), numărul de teste zilnice ale glicemiei, frecvența și severitatea episoadelor hipoglicemiante, și informații despre alte boli diagnosticate, meditația utilizată, obiceiurile de fumat și abuzul de alcool și droguri. Medicul a analizat aceste date pentru a identifica factorii care ar putea afecta controlul glicemic al participanților la studiu.
2.2. Proiectarea sistemului vocal
Sistemul consta dintr-un smartphone controlat de Android, cu aplicația client care comunică fără fir cu serverele pentru a efectua următoarele sarcini: (1) recunoașterea automată a vorbirii (ASR) și transformarea descrierii vocale a mesei în text; (2) analiza descrierii textuale pentru a determina compoziția mesei; (3) calcularea dozei de insulină care compensează masa conform algoritmului, luând în considerare fie numai conținutul de CHO, fie conținutul de CHO, proteine și grăsimi din masă. O descriere detaliată a sistemului poate fi găsită în altă parte [29]. Este de remarcat faptul că baza de date a sistemului conține caracteristici de 900 de produse alimentare unice și 5000 de termeni, facilitând conversia eficientă vorbire-text, inclusiv alimente care erau prezente în meniul spitalului. Cu toate acestea, nici numărul de calorii, cantitățile de CHO, proteine și grăsimi care caracterizează fiecare produs și nici alte date stocate în baza de date a sistemului nu au fost adaptate la caracteristicile meniului spitalului.
2.3. Utilizarea sistemului vocal și calculatorul de bolus încorporat
Fiecare participant la studiu a folosit sistemul în modul următor. Înainte de a începe o masă, participantul și-a descris verbal compoziția, dând numele și mărimea (fie în unități precum grame, uncii sau litri, fie în unități de măsură obișnuite, cum ar fi linguri, căni sau porții) ale fiecărui produs alimentar prezent în masa. Descrierea a fost transmisă către server și, după conversia vorbirii în text, fiecare produs alimentar a fost identificat și afișat pe ecranul smartphone-ului pentru verificare de către participant. Dacă identificarea a eșuat, un mesaj de avertizare a arătat că recunoașterea a eșuat din cauza unui eșec ASR sau a lipsei informațiilor necesare în descrierea mesei, de exemplu, atunci când pacientul a specificat un produs alimentar care nu era prezent în baza de date a sistem. În cazul eșecului ASR, pacientul a repetat descrierea produsului alimentar care nu fusese identificat corect. Pentru fiecare produs recunoscut, sistemul a calculat conținutul de calorii și conținutul de CHO, proteine și grăsimi în grame.
La activare, calculatorul bolus a rezumat valoarea calorică totală, unitățile de schimb de carbohidrați (CU) și unitățile de schimb proteine - grăsimi (PFU) din întreaga masă și, în cele din urmă, doza de insulină necesară pentru a compensa masa. PFU a fost calculat utilizând următoarea ecuație:
Dacă PFU este mai mare de 1,0, se recomandă un bolus cu două unde care constă dintr-un bolus simplu și un bolus cu undă pătrată cu o durată de 4 până la 8 ore, în funcție de valoarea PFU. Doza totală de insulină prandială a fost determinată pe baza următoarei ecuații [30]:
Prima parte a sumei din ecuația (2) denotă cantitatea de insulină administrată în bolusul simplu și a doua parte denotă insulina administrată în infuzia cu undă pătrată cu durată variabilă. Dacă PFU este mai mic de 1,0, atunci sistemul îl reduce la zero și, în consecință, recomandă o doză de insulină sub forma unui bolus simplu [30].
2.4. Impactul metodei de numărare a macronutrienților asupra controlului glicemic
Pentru a evalua dacă estimarea automată a conținutului de masă pe baza descrierii vocale a unei mese poate fi utilizată pentru a controla glicemia, grupul de studiu a fost împărțit aleatoriu în două subgrupuri. În primul, format din 14 subiecți, cu vârsta de 23,5 ± 3,8 ani, cu HbA1c egal cu 8,6 ± 1,8% (70 ± 20 mmol/mol), bolusii de insulină au fost decideți de un medic pe baza datelor referitoare la conținutul mesei. În cel de-al doilea, implicând subiecți cu vârsta de 23,7 ± 5,4 ani cu HbA1c egal cu 8,5 ± 1,3% (69 ± 14 mmol/mol), medicul a avut acces doar la datele furnizate de sistem atunci când a determinat doza de insulină. Fiecare participant la studiu a fost monitorizat utilizând sistemul continuu de monitorizare a glucozei.
S-au comparat următorii parametri între subgrupuri: concentrația medie de glucoză plasmatică (PG), procentul de timp când concentrația de glucoză a fost normoglicemică, adică mai mare de 3,9 mmol/L (70 mg/dL) și mai mică de 10,0 mmol/L 180 mg/dL) (PNPG), creșterea maximă medie a PG după mesele principale și numărul și durata episoadelor hipoglicemiante (de exemplu, concentrația de glucoză egală sau mai mică de 3,9 mmol/L sau 70 mg/dL).
2.5. Analize statistice
tabelul 1
Conținutul caloric estimat de dietetician și sistemul VoiceDiab.
| Mic dejun | 110 | 388 ± 85 166-602 | 381 ± 84 159–586 | 1 SD, abaterea standard. |
Conținutul mediu de calorii din ambele gustări estimat de sistem nu a diferit de cele calculate de dietetician. În cazul meselor principale, diferențele au fost semnificative statistic. În general, sistemul a avut tendința de a subestima numărul de calorii, dar diferențele medii au fost relativ mici și egale cu −7,2 ± 24,4 kcal (−1,7 ± 6,2%), −55,6 ± 54,8 kcal (−10,8 ± 10,4%) și −6,5 ± 26,0 kcal (−1,2 ± 5,4%) pentru micul dejun, respectiv prânzul și cina.
În cazul fiecărei mese, cu excepția prânzului, sistemul a estimat valorile UC care au fost mai mari decât cele calculate de dietetician (Tabelul 2). Diferențele medii au fost egale cu 0,3 ± 0,3 CU (8,8 ± 6,4%), 0,0 ± 0,6 CU (0,6 ± 12,4%) și 0,3 ± 0,2 CU (9,2 ± 5,9%), pentru mesele principale consecutive începând cu micul dejun. În total, pentru cele trei mese principale, diferența dintre conținutul de CHO estimat de sistem și de către dietetician a fost mai mică sau egală cu ± 1 CU (adică ± 10 g de CHO) în 96,3% din cazuri.
masa 2
Unitatea de schimb carbohidrați (CU) și unitatea de schimb proteine - grăsimi (PFU) numărate de dietetician și sistemul VoiceDiab.
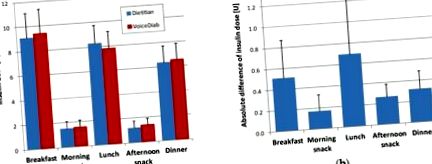
| Mic dejun | 110 | 3,8 ± 0,8 2.2–6.0 | 4,1 ± 0,9 2.4–6.5 | Figura 1 a prezintă o comparație între bolusurile de insulină calculate pe baza compoziției de masă oferite de dietetician față de sistem, în timp ce Figura 1 b ilustrează diferențele absolute dintre aceste doze de insulină. |
(A) Compararea dozelor de insulină și (b) diferențe absolute ale dozelor de insulină calculate pe baza conținutului de carbohidrați (CHO), proteine și grăsimi furnizate de dietetician și sistemul VoiceDiab.
În cazul tuturor meselor, cu excepția gustărilor de dimineață, diferențele dintre bolusurile de insulină au fost semnificative statistic (p Figura 2 a arată, pentru fiecare masă și pentru toate mesele împreună, procentul dozelor de insulină prandială calculat pe baza estimărilor mesei realizate de sistem care au fost egale cu valorile lor de referință, cele care au fost în intervalul 0,0-0,5 U, 0,5-1,0 U, 1,0-2,0 U și cele care au diferit cu mai mult de 2 U față de valorile de referință. (78,7%) au diferit cu ± 0,5 U cel mult de valorile de referință și doar 1,3% au depășit intervalul de ± 2 U. Când am folosit valorile CU pentru a calcula bolusuri simple de insulină (Figura 2 b), neglijând conținutul de proteine și grăsimi din mese, rezultatele au fost similare, adică 81,7% din bolusuri au fost diferite de valorile lor de referință cu 0,5 U sau mai puțin și doar 1,1% au diferit cu mai mult de 2 U (din care 0,9% au fost legate de insulină mic dejun care compensează dozele).
Diferențele absolute medii relative ale dozelor de insulină calculate în conformitate cu ecuația (2) pe baza estimărilor unităților de schimb de carbohidrați (CU) și a unităților de schimb proteine-grăsimi (PFU) furnizate de dietetician și sistemul VoiceDiab pentru (A) bolusuri cu două unde; (b) bolusuri simple. S-a presupus că raportul insulină la carbohidrați (ICR) este de 1,5 U/CU pentru micul dejun și 1,0 U/CU pentru toate celelalte mese.
3.3. Impactul metodei de numărare a macronutrienților asupra controlului glicemic
PG mediu și PNPG au fost similare pentru ambele subgrupuri, adică 7,3 ± 0,8 mmol/L (131 ± 15 mg/dL) vs. 7,5 ± 0,9 mmol/L (135 ± 16 mg/dL) și 76 ± 7% (p = 0,42) vs. 75 ± 7% (p = 0,79), respectiv. Creșterea maximă a PG a fost egală cu 4,3 ± 1,4 mmol/L (77 ± 25 mg/dL) vs. 4,7 ± 1,8 mmol/L (85 ± 33 mg/dL) (p = 0,37) după micul dejun, 3,7 ± 1,7 mmol/L (67 ± 30 mg/dL) vs. 4,0 ± 1,7 mmol/L (72 ± 30 mg/dL) (p = 0,55) după prânz și 3,9 ± 1,3 mmol/L (71 ± 24 mg/dL) vs. 4,3 ± 0,9 mmol/L (77 ± 17 mg/dl) (p = 0,11) după cină, în primul și al doilea subgrup, respectiv. În primul subgrup, episoadele de hipoglicemie au apărut de 2,1 ± 0,8 ori pe zi, în timp ce în al doilea subgrup, au apărut 2,0 ± 1,3 pe zi (p = 0,77). Durata zilnică a episoadelor hipoglicemiante a fost egală cu 120 ± 70 min în primul subgrup și 95 ± 74 min în al doilea subgrup (p = 0,35).
4. Discuție și concluzii
Analizând și rezumând impactul diferențelor în calculele CU și PFU asupra dozelor de insulină rezultate estimate conform algoritmului implementat în sistemul VoiceDiab, am demonstrat că în peste 91% din mese, diferența absolută în dozele de insulină a fost mai mică de 1 U Cele mai mari discrepanțe au fost observate în calculul dozelor de insulină înainte de prânz, unde 26% din diferențe au fost mai mari de 1 U.
Rezumând, persoanele cu diabet de tip 1, în ciuda educației, se confruntă cu mai multe dificultăți în ajustarea dozelor de insulină pe baza propriilor estimări ale conținutului de CHO al meselor. Aceste dificultăți pot fi chiar mai pronunțate atunci când un bolus de insulină complex este determinat să compenseze nu numai CHO, ci și conținutul de proteine și grăsimi. Sistemul dezvoltat, care utilizează o interfață intuitivă a utilizatorului, este simplu de utilizat și oferă rapid informații despre compoziția meselor care pot fi utilizate pentru a calcula automat dozele de insulină prandială. Rezultatele obținute și datele din literatură indică faptul că acuratețea estimărilor CU și PFU calculate de sistem este suficientă pentru a calcula dozele de insulină, fie folosind automat algoritmul implementat în sistemul VoiceDiab, fie folosind manual algoritmul bazat pe cunoștințele și experiența un fizician; aceste doze s-au dovedit a fi apropiate de cele calculate pe baza valorilor de referință ale CU și PFU stabilite de dietetician.
Mulțumiri
Acest studiu, inclusiv costurile de publicare în acces deschis, a fost finanțat de Centrul Național pentru Cercetare și Dezvoltare (subvenția nr. PBS1/B9/13/2012).
- Tehnologia de numărare a caloriilor și de urmărire a fitnessului Asociații cu simptomatologia tulburărilor alimentare
- Energia calorică descompune lumea „numărării caloriilor”; PA mănâncă
- Numărarea caloriilor și înșelătoria cu 2000 de calorii Kris M Beal
- Aplicația de numărare a caloriilor utilizează balize Bluetooth în frigidere pentru a ajuta utilizatorii să piardă în greutate; NFCW
- Numărarea caloriilor 101 Nu conta caloriile!