Abstract
fundal
Eficacitatea tratamentelor antipaludice rămâne o provocare critică pentru programele de control. Cu toate acestea, când se stabilește eficacitatea medicamentului, doza se calculează pe baza unei greutăți predefinite în funcție de vârsta pacientului. Pe baza ipotezei că asumarea standard a greutății în funcție de vârstă la administrarea medicamentului ar putea duce la un eșec terapeutic potențial datorat subdozării (în cazul supraponderalității) sau supradozării (în cazul supraponderalității). În acest studiu, relația dintre starea greutății și eficacitatea medicamentelor împotriva malariei în curățarea curentului Plasmodium falciparum infecția și prevenirea reinfecției după tratament a fost investigată.
Metode
Datele au fost înecate dintr-un studiu clinic efectuat anterior pentru a investiga eficacitatea medicamentelor împotriva malariei la 749 de copii din Mali (2002-2004). Participanții au fost tratați fie cu arteunat + amodiaquină (AS + AQ, n1 = 250), arteunat + sulfadoxină - pirimetamină (AS + SP, n2 = 248), fie cu artesunat (AS, n3 = 251) și urmat timp de 28 de zile după tratament. Scorul z al Organizației Mondiale a Sănătății (OMS) a fost utilizat pentru a defini starea greutății. Un test Chi pătrat a fost utilizat pentru a compara rezultatele în funcție de medicamente, starea greutății și dinamica nivelului ALAT, ASAT, creatinină și hemoglobină. Modele de regresie logistică au fost dezvoltate pentru a determina efectul parametrilor de bază (starea greutății, aspartat transaminază, alanină aminotransferază, nivel creatinină și hemoglobină) asupra eficacității medicamentului conform criteriilor OMS.
Rezultate
Fără corecție moleculară, în brațul AS + AQ, rata răspunsului clinic și parazitologic adecvat (ACPR) a fost mai mare în grupul de copii subponderali cu 94,74% comparativ cu copiii cu normal și supraponderal (91,24% și respectiv 80,43%, p = 0,03) . După corectarea PCR, eficacitatea tratamentului a fost similară la cele trei grupuri de pacienți și a fost peste 98% (p = 0,4). S-a observat că supraponderalitatea nu are impact asupra recrudescenței. Cu toate acestea, a fost asociat cu un risc crescut de infecții noi în brațul (AS + AQ) (OR = 0,21, 95% CI [0,06; 0,86], p = 0,03).
Concluzii
Constatările sugerează că deficiența de greutate nu are niciun efect dăunător asupra eficacității medicamentului antimalaric. O creștere a ratei de reinfecție la copiii supraponderali tratați cu AS + AQ ar trebui explorată în continuare în studii mai ample.
fundal
Malaria este o povară globală majoră pentru sănătatea publică, cu 212 milioane de cazuri și 429.000 de decese asociate estimate în cel mai recent recensământ al bolilor [1, 2]. Pe baza cifrelor din 2015, Africa subsahariană rămâne în special afectată pentru aproximativ 90% din cazurile și decesele din întreaga lume [3].
În Mali, malaria este principala cauză de morbiditate și mortalitate, în special în rândul celor mai tineri [4, 5]. În 2012, Studiul demografic și de sănătate a raportat o prevalență de 52% a deceselor cauzate de malarie în rândul copiilor malieni cu vârsta sub cinci ani [5], în timp ce Organizația Mondială a Sănătății (OMS) estimează aproximativ 17% din decesele asociate copiilor [6]. ]. Unul din cinci copii malieni mor chiar înainte de al cincilea an [6]. Printre cele cinci specii de paraziți ai malariei care infectează oamenii, Plasmodium falciparum este cel mai răspândit, provocând cea mai mare morbiditate și mortalitate [7].
Intervențiile recomandate în prezent de OMS pentru gestionarea malariei sunt utilizarea plasei de țânțari insecticide de lungă durată, pulverizarea reziduală în interior pentru controlul vectorilor, chimioprevenția sezonieră a malariei (SMC), tratamentul preventiv intermitent pentru malaria la sugari (IPTi), un prompt accesul la testarea rapidă de diagnostic (RDT) a cazurilor suspectate și tratamentul cazurilor confirmate cu terapie combinată eficientă pe bază de artemisinină (ACT) [8]. Artesunatul + amodiaquina (AS + AQ) este una dintre cele două combinații pe bază de artemisinină recomandate de Programul național de control al malariei din Malia și este utilizată pe scară largă în Mali și se știe că este sigură și eficientă [9, 10]. Artesunatul + sulfadoxina - pirimetamina (AS + SP) este una dintre combinațiile pe bază de artemisinină recomandate de OMS [11], deși utilizarea sa este descurajată. Artesunatul (AS) în monoterapie a fost administrat ca tratament de referință al malariei necomplicate [9]. În studiul actual, cazurile înscrise au fost toate malaria falciparum necomplicată.
Mai mulți factori pot influența manifestarea clinică a malariei, cum ar fi vârsta pacientului [12], nivelul parazitemiei/virulenței, în special P. falciparum [13] și/sau subnutriție [14]. În general, subnutriția slăbește sistemul corpului și încurajează dezvoltarea infecțiilor [7], din cauza deficitului de micronutrienți și a afectării sistemului imunitar. S-a raportat că 450.000 de malieni sub 5 ani au suferit de subnutriție acută moderată în 2013 [15]. În contextul specific al infecțiilor cu malarie, aceasta poate reduce imunitatea dobândită specifică malariei încă din copilărie [12, 13].
Eficacitatea tratamentelor antimalarice rămâne o provocare continuă în conformitate cu literatura de specialitate [16], în special în cazul reinfectării. De obicei, doza de medicament care trebuie administrată este calculată pe baza indicilor greutății populației, dacă există. Cu toate acestea, o modificare a greutății în raport cu vârsta la administrarea medicamentului ar putea fi cauza unui eșec terapeutic potențial datorat subdozării (în cazul supraponderalității) sau supradozării (în cazul supraponderalității).
Utilizarea medicamentelor concomitente și/sau starea de sănătate a pacientului ar putea afecta, de asemenea, eficacitatea și siguranța medicamentului [17]. Aspartatul transaminazic (ASAT), alanina aminotransferaza (ALAT) și creatinina ar putea fi crescute, iar hemoglobina (Hb) a scăzut înainte de administrarea anti-malarică a medicamentului și ar putea afecta eficacitatea și siguranța tratamentului.
Aici, eficacitatea și siguranța a două combinații pe bază de artemisinină (AS + AQ și AS + SP) și artezinat în monoterapie au fost investigate în funcție de starea de greutate, ASAT, ALAT, creatinină și nivelul Hb. în plus, P. falciparum au fost abordate clearance-ul și prevenirea reinfecției în timpul urmăririi post-tratament la copii.
Metode
Manipularea datelor
Această lucrare este o analiză secundară a datelor dintr-un studiu clinic anterior (http://www.pactr.org, PACTR201802003020160) efectuat pentru a investiga eficacitatea medicamentului împotriva malariei la pacienții care locuiesc în Bougoula-Hameau, Mali, pe o perioadă de 3 ani (2002-2004). Participanții au fost randomizați pentru a primi fie AS + AQ, AS + SP, fie monoterapia artezunată. În total, 250 de participanți au fost tratați cu „AS (3 zile) + AQ (3 zile)”, 248 cu „AS (3 zile) + SP (1 zi)” și 251 cu „AS singur (5 zile)”. Medicamentele au fost administrate pe cale orală la următoarele doze: AS (4 mg/kg în prima zi și 2 mg/kg alte zile), AQ (10 mg/kg) și SP (25 mg/kg). Pacienții au fost urmăriți în decurs de 28 de zile de la includere. Pacienții au fost vizionați pentru examinări clinice și biologice în fiecare zi în primele 4 zile, apoi în zilele 7, 14, 21 și 28 [9].
Starea greutății
Greutatea a fost măsurată fără încălțăminte, dar purtând haine ușoare folosind o balanță mecanică Seca 761 gradată în kilograme. Pentru sugarii incapabili să stea în picioare, greutatea a fost măsurată cu un adult și apoi s-a scăzut greutatea adultului. Înălțimea a fost măsurată în poziție în picioare folosind o tijă de măsurare gradată în centimetri [18]. Programul OMS de acces gratuit AnthroPlus [19] a fost utilizat pentru a calcula indicele de masă corporală (IMC) și scorurile z aferente, care au fost utilizate ca un proxy al stării greutății. Definiția stării greutății s-a bazat pe următoarele puncte limită recomandate de OMS în 2007 [20,21,22]:
Subponderalitate: IMC scor z) 2) a fost efectuat pentru a investiga asocierile dintre starea greutății, caracteristicile clinice și biologice la înscriere, precum și rezultatul tratamentului. Au fost efectuate analize de regresie logistică pentru a analiza efectul stării greutății inițiale (subponderal, supraponderal, inclusiv obezitate) asupra eficacității tratamentului. Un al doilea model de regresie logistică a investigat efectul altor parametri de bază, cum ar fi ALAT, ASAT, creatinină și nivelul Hb, în plus față de starea de greutate, asupra eficacității medicamentului.
Rezultate
Caracteristicile inițiale sunt descrise în Tabelul 1. Distribuția brațelor de tratament (p = 0,11) și a sexului pacienților (p = 0,95) au fost similare în rândul grupurilor cu status de greutate. Aproximativ 40% dintre copiii cu vârsta sub 5 ani au avut o supraponderalitate, 50% au avut o greutate normală, 10% au avut o greutate subponderală. Dintre copiii mai mari, 71% au prezentat o greutate normală, 12% au avut o greutate subponderală și 17% au avut o greutate excesivă (p Tabelul 1 Caracteristici generale la înscriere în funcție de statutul de greutate
Microscopia a arătat că în ziua a 7-a un singur pacient din subponderalitatea și un pacient din grupul cu greutate normală a avut frotiu pozitiv. În ziua 14, 5,1% dintre copiii din grupul subponderal au purtat parazit al malariei, comparativ cu 1,6% și 2,5% în grupurile cu greutate normală și, respectiv, supraponderali (p = 0,16). În ziua 21, nu s-a observat niciun parazit în grupul subponderal, în schimb, frotiul de sânge a fost pozitiv la 7,5% dintre copiii cu greutate normală și 8,4% dintre copiii cu supraponderalitate (p = 0,03). În ziua 28 nu a existat nicio diferență semnificativă în transportul paraziților (p = 0,95) între cele trei grupuri.
Media ± SD a primelor doze de amodiaquină administrate a fost mai mică la copiii supraponderali 155,82 ± 48,07 mg/kg comparativ cu copiii cu greutate subponderală și cu greutate normală, respectiv 165,08 ± 69,89 și 185,3 ± 89,99 mg/kg (p = 0,04) (Tabelul 1) . Proporția răspunsului clinic și parazitologic adecvat (ACPR) după tratament fără corecție moleculară între categoriile de greutate, în brațul AS + AQ, a fost mai mare în grupul copiilor cu greutate sub 94,74% comparativ cu copiii cu greutate normală și supraponderal (91,24 și 80,43% respectiv, p = 0,03). După corectarea PCR, eficacitatea tratamentului a fost similară în cele trei grupe de greutate corporală și a fost peste 98% (p = 0,44). Nu a existat nicio diferență în eficacitatea tratamentului în brațele AS + SP și AS-alone în funcție de starea de greutate (Tabelul 2). Densitatea mediană a paraziților înainte de tratament a fost de 17.800, 14.850 și 17.660 trofozoizi/forl pentru copiii cu greutate subponderală, greutate normală și, respectiv, supraponderală. Densitatea de bază a paraziților a fost mai mare la copiii subponderali comparativ cu cei cu greutate normală (p = 0,03).
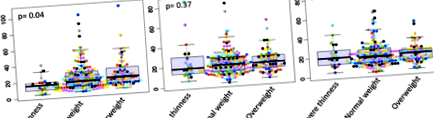
La înscriere, mediana nivelului ALAT (Tabelul 1), deși în limitele normale, a fost mai mare la copiii cu supraponderalitate (23,31 UI/l) comparativ cu copiii cu greutate normală (17,00 UI/l) și 15,15 UI/l la copiii cu greutate subponderală (p = 0,04). În timpul urmăririi, în ziua 7 și ziua 14, diferitele grupuri de stare a greutății au fost similare în ceea ce privește nivelul ALAT, valorile p au fost de 0,37 și respectiv 0,89 (Fig. 1).
Nivelul ALAT în timpul urmăririi în funcție de starea greutății. În ziua 0, un pacient cu greutate normală și altul cu supraponderalitate au avut respectiv 740,25 și 367 U/l ca nivel ASAT. În ziua 7, doi pacienți cu greutate normală au avut niveluri ASAT foarte ridicate, respectiv 484 și 237 U/l. Valorile anterioare nu au fost incluse în figură
Nivelurile ASAT s-au încadrat în limite normale în ziua a 7-a, cu cea mai ridicată mediană (Fig. 2) observată la copiii cu supraponderalitate (37,91 UI/l) comparativ cu 30,90 UI/l în greutatea normală și 30,35 UI/l în grupurile subponderale). La înscriere și ziua 14, cele trei grupuri erau similare, p = 0,11 și, respectiv, 0,05.
Nivelul ASAT în timpul urmăririi în funcție de starea greutății
Nivelul creatininei (Fig. 3) a fost similar la cele trei grupe de copii (greutate normală, subponderală și supraponderală) la înscriere (p = 0,07), la 7 zile după prima doză de medicamente (p = 0,41) și la 14 zile p = 0,99).
Nivelul creatininei în timpul urmăririi în funcție de starea greutății. În ziua 0, un pacient cu greutate normală și un pacient cu supraponderalitate au avut, respectiv, 3,84 și 4,8 mg/dl ca nivel de creatinină. În ziua 14, un pacient cu supraponderalitate avea 6,7 mg/dl ca nivel de creatinină. Valorile anterioare nu au fost incluse în figură
Nivelul mediu (Q1, Q3) de hemoglobină la înscriere a fost cel mai scăzut la copiii cu greutate excesivă 9,50 g/dl (8,48, 10,90). Cu toate acestea, mediana densității paraziților a fost similară la copii în funcție de starea de greutate (Tabelul 1). Pe parcursul urmăririi, copiii supraponderali și subponderali par să aibă niveluri similare de hemoglobină. Copiii cu greutate normală au avut un nivel de hemoglobină ușor mai ridicat. Valorile p au fost de 0,001, 0,001 și 0,01 la înscriere, zilele 7 și respectiv 14 (Fig. 4).
Nivelul hemoglobinei în timpul urmăririi în funcție de starea greutății
Modelul de regresie logistică (Tabelul 3) a arătat că supraponderabilitatea a fost asociată cu un risc crescut de infecții noi în brațul „AS + AQ” (OR = 0,21, p = 0,02). În brațul de monoterapie „AS”, fiecare creștere a unei unități (UI/l) a nivelului ALAT a fost observată a fi asociată cu o scădere a probabilității unui răspuns clinic și parazitologic adecvat (OR = 0,95, p = 0,02). Modelul utilizat nu prezintă nicio asociere între starea inițială a greutății, parametrii biologici de bază și răspunsul clinic și biologic adecvat după 28 de zile de urmărire în brațul de tratament „AS + SP”.
Analiza multivariată nu a arătat nicio asociere între starea greutății inițiale și nici brațul de tratament și evoluția ALAT în timpul studiului (Tabelul 4). Modelul multivariat (Tabelul 4) prezintă un nivel ASAT mai mare la copii randomizați în brațul „AS + SP” înainte de tratament (p = 0,04). Reunind starea greutății și brațul de tratament, modelul a arătat că deficiența de greutate este asociată cu un nivel ridicat de ASAT în brațul „AS + SP” (p = 0,04). După administrarea medicamentului, indiferent de medicamentul utilizat în acest studiu, excesul de greutate a fost asociat cu o creștere a nivelului ASAT în ziua 7 (p = 0,02) în timp ce nu a fost observată nicio asociere la 14 zile.
Modelul multivariant (Tabelul 4) a arătat o creștere a nivelului creatininei se observă în zilele 7 după prima doză de absorbție „AS” (p = 0,02). Reunind starea greutății și brațul de tratament, modelul a arătat o asociere între supraponderalitate, „AS” și creșterea nivelului de creatinină (p = 0,03). Înainte de tratament și la 14 zile după administrarea medicamentului nu a fost observată nicio asociere. Același model a arătat că în ziua 14 scăderea nivelului de hemoglobină este asociată cu brațul de tratament „AS + SP” (p = 0,01). Reunind starea greutății și brațul de tratament în model, observăm că deficiența de greutate și „AS + SP” (p = 0,03); iar supraponderalitatea și „AS + SP” (p = 0,04) sunt asociate cu scăderea nivelului de hemoglobină.
Discuţie
Rezultatele au arătat că, în ciuda densității mai mari de paraziți și a nivelului scăzut de hemoglobină observat la copiii subponderali la înscriere, nu s-a găsit nicio asociere între greutatea insuficientă și eficacitatea scăzută sau siguranța medicamentelor antimalarice utilizate în acest studiu. Mai mult, această analiză a arătat că supraponderalitatea tinde să crească riscul de noi infecții în brațul „AS + AQ”. Sunt necesare investigații suplimentare pentru a examina dacă regimul curent de tratament al „AS + AQ” este adecvat pentru toți copiii.
Din 749 de copii înscriși în acest studiu, 244 au fost în grupul supraponderal și 78 de copii în grupul subponderal (Tabelul 1). Această tendință ar putea fi influențată de criteriul de excludere a malnutriției severe la studiul clinic inițial. Un studiu realizat în același cadru în 1995 a constatat o prevalență a malnutriției cronice la copii cu aproximativ 25% [25].
La înscriere, densitatea parazitului malariei era mai mare la copiii subponderali. Sensibilitatea ridicată la infecție la copiii subnutriți ar putea fi explicată în principal prin suprimarea imunității lor din cauza subnutriției care afectează imunitatea umorală și mediată celular, activitatea bactericidă a fagocitelor și formarea complementului [26]. Deși o proporție mai mare de răspuns clinic și parazitologic adecvat a fost observată la copiii cu deficit de greutate înainte de corecția PCR în brațul „AS + AQ”, toate cele trei grupuri au fost similare după corectarea PCR.
Dozele de comprimate „AS + AQ” au fost determinate și administrate copiilor pe categorii de vârstă, asumându-și greutatea în funcție de vârstă. Scăderea eficacității tratamentului la copiii cu supraponderalitate poate fi legată de subdozarea. În schimb, creșterea eficienței tratamentului în prevenirea noilor infecții la copiii cu greutate mică ar putea fi explicată printr-un efect al supradozajului. Taylor și colab. [27] a descris într-o publicație anterioară că copiii mai mici și subponderali prezintă un risc mare de supradozaj și invers. La pacienții cu supraponderalitate și obezitate, se constată frecvent deficiența de fier [28]. Studiile arată că frecvența malariei a crescut la pacienții cu supliment de fier [29, 30].
Asocierea semnificativă observată între excesul de greutate și creșterea nivelului de ASAT și de creatinină în ziua 7 poate fi explicată prin posibila acumulare de medicamente în depozitele de grăsimi. Cel mai scăzut nivel de hemoglobină (Fig. 4) a fost observat la copiii cu deficit de greutate înainte de tratament. Ehrhardt și colab. [14] a raportat că anemia (nivelul de Hb
Concluzie
Deficitul de greutate nu are niciun efect dăunător asupra eficacității medicamentelor antimalarice. Statutul subponderal nu a afectat tolerabilitatea medicamentelor. Scăderea eficacității tratamentului la copiii supraponderali tratați cu arteunat + amodiaquină ar putea fi legată de o subdozare și ar trebui explorată în continuare în studii mai ample.
Abrevieri
răspuns clinic și parazitologic adecvat
- Siguranța și eficacitatea citrus aurantium pentru scăderea în greutate - Baza de date a rezumatelor de recenzii ale
- Nou medicament pentru slăbit aprobat de FDA
- Nou medicament pentru slăbit în lupta împotriva obezității Forskolin Green Vibe Qysmia Povești de succes - Furtună
- Percepția de sine a studenților la farmacie despre greutate și relația cu consilierea pacienților cu privire la stilul de viață
- Un tip mai nou de medicament HIV legat de creșterea în greutate Avert