Introducere
Tamoxifenul este utilizat pe scară largă ca tratament adjuvant eficient și pentru prevenirea cancerului de sân pozitiv la receptorii de estrogen [1]. Tamoxifenul scade aportul de alimente, greutatea corporală și (cel puțin pe termen scurt) masa de grăsime la rozătoare. În ciuda scăderii greutății corporale la femeile obeze, tamoxifenul poate crește incidența diabetului zaharat [2]. Acest efect secundar potențial a fost atribuit scăderii β-supraviețuirea și proliferarea celulelor, dar și steatoza hepatică la rozătoare [3]. Noi și alții am demonstrat recent că tamoxifenul afectează glucoza, metabolismul lipidic, modificările tranzitorii ale compoziției corpului care pot proveni din necroza țesutului adipos indusă de tamoxifen, urmată de recrutarea adipocitelor de novo și de redistribuirea grăsimilor, inclusiv acumularea de grăsime în ficat pe termen lung [3, 4]. Într-adevăr, dezvoltarea ficatului gras a fost observată încă la 3 luni de la inițierea tratamentului cu tamoxifen la femeile cu cancer de sân [5]. Cu toate acestea, mecanismele precise ale potențialelor efecte diabetogene ale tamoxifenului nu sunt încă pe deplin clare. Prin urmare, ne-am propus să elucidăm în mod sistematic dezvoltarea hiperglicemiei legate de tamoxifen utilizând cleme hiperinsulinemice - euglicemice.
Metode
Experimente pe animale
Toate studiile efectuate pe animale au fost aprobate de autoritățile locale ale statului Saxonia, Germania, după cum recomandă comitetul local de evaluare a eticii animalelor (Landesdirektion Leipzig, TVV21/12, T03/13 Germania). Șoareci femele C57BL/6NTac de 12 săptămâni (N = 8) au fost adăpostite într-un ciclu de lumină/întuneric de 12 ore cu apă și alimente (chow standard, Sniff Spezialdiäten, Soest, Germania) ad libitum. Animalele au fost crescute și ținute în Laboratoarele de animale de la Universitatea din Leipzig. Tamoxifenul (Tam, Sigma - Aldrich, Taufkirchen, Germania, # T5648) a fost soluționat în ulei de trigliceride (Fagron, Barsbüttel, Germania, # 700.282) și a fost injectat intraperitoneal cu 1 mg pe zi în cinci zile consecutive. Controalele au fost injectate numai cu solvent. După 24 de zile de tratament Tam, cateterele au fost implantate în vena jugulară stângă. Au fost efectuate cleme hiperinsulinemice - euglicemice la patru șoareci femele din fiecare grup experimental, așa cum este descris [3]. Pe scurt, clema hiperinsulinemică - euglicemică a fost efectuată cu o perfuzie continuă de insulină umană la o rată de 20 mU/kg/min pentru a reduce nivelurile de glucoză plasmatică în intervalul fiziologic (
5 mmol/l). Concentrațiile de glucoză din sânge au fost menținute prin ajustarea ratelor de perfuzie a unei soluții de glucoză de 20%. Starea de echilibru a fost definită ca niveluri constante de glucoză timp de 20 min la o rată stabilă de perfuzie a glucozei (GIR), care a fost atinsă în intervalul 120-240 min. Starea de echilibru a fost menținută timp de 45 de minute, iar probele de sânge (10 μL) au fost prelevate la momentul inițial, la fiecare 5 minute și la fiecare 10 minute în timpul stării de echilibru. Toate perfuziile au fost aplicate folosind pompe de micro-dializă (TSE Systems, Chesterfield, MO, SUA). Producția de glucoză hepatică (HPG, mg × kg -1 -1 min min -1) a fost calculată ca diferență între rata de apariție a glucozei și rata de perfuzie a glucozei. Imediat după clemă, șoarecii au fost uciși prin luxație cervicală și ficat, au fost extrase și cântărite grăsimi subcutanate (SC), epigonadale (EPI) și intercapulare brune.
Înainte de efectuarea studiilor cu clamp, valorile glicemiei au fost determinate din probe de sânge venos integral folosind un analizor automat (COBAS 8000, Roche Diagnostics, Mannheim, Germania). Concentrațiile serice de insulină au fost măsurate prin ELISA utilizând standarde pentru șoareci, conform recomandărilor producătorului (Insulina ELISA; CrystalChem. Inc, Downers Grove, IL). Într-un al doilea subgrup de animale (N = 6 per grup de tratament), concentrațiile serice de trigliceride (TG), acizi grași liberi (FFA), colesterol total (Chol) și aspartat aminotransferază (AST) au fost analizate folosind analizorul modular COBAS 8000 (Roche Diagnostics, Mannheim, Germania).
Secțiunile hepatice de 4 µm au fost colorate cu hematoxilină și eozină (H&E) pentru examinarea de rutină pentru detectarea leucocitelor care se infiltrează în țesutul hepatic.
Analize statistice
Software-ul Prism 6.0 (GraphPad Software) a fost utilizat pentru analize statistice. Datele sunt date ca medie ± SE. Seturile de date au fost analizate pentru semnificație statistică folosind un student cu două cozi nepereche t test sau Mann - Whitney U Test. P valori
Rezultate
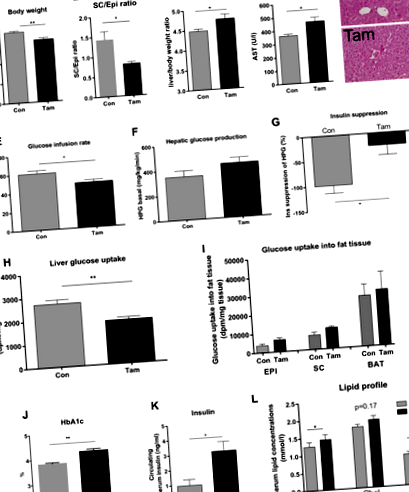
Am efectuat studii de clamp hiperinsulinemic - euglicemic la șoareci slabi sănătoși în faza de recâștigare în greutate după pierderea în greutate indusă de tamoxifen raportată anterior (14 zile după prima doză de tratament cu tamoxifen, Fig. 1a). Recâștigarea greutății este asociată cu creșterea depunerii de grăsime ectopică, inclusiv dezvoltarea ficatului gras și creșterea greutății hepatice relative (Fig. 1b, c). În plus, concentrația serică a AST este semnificativ mai mare la șoarecii tratați cu tamoxifen (Fig. 1d). Șoarecii tratați cu tamoxifen sunt caracterizați prin afectarea sensibilității la insulină la nivelul întregului corp (Fig. 1e) și la nivelul ficatului (Fig. 1f - h). Rata de perfuzie a glucozei și capacitatea insulinei de a reduce producția hepatică de glucoză au fost semnificativ mai mici la tamoxifenul tratat comparativ cu șoarecii martor (Fig. 1g). Absorbția glucozei hepatice a fost semnificativ mai mică la șoarecii tratați cu tamoxifen (Fig. 1h), unde țesutul adipos nu a fost afectat (Fig. 1i). Concentrațiile serice de HbA1c (Fig. 1j), insulina postată (Fig. 1k), trigliceride și acizi grași liberi (Fig. 1l) au fost semnificativ mai mari la șoarecii tratați cu tamoxifen comparativ cu martorii (Fig. 1).
Discuţie
Aici, arătăm că modelul nostru de tratament raportat anterior cu tamoxifen elucidează secvența de patomecanisme care stau la baza efectului secundar diabetogen al tamoxifenului [4]. La șoareci, tamoxifenul a provocat acut o
Referințe
Osborne CK (1998) Tamoxifen în tratamentul cancerului de sân. N Engl J Med 339 (22): 1609–1618. https://doi.org/10.1056/NEJM199811263392207
Xu B, Lovre D, Mauvais-Jarvis F (2017) Efectul modulatorilor selectivi ai receptorilor de estrogen asupra apariției diabetului de tip 2 la femei: perspective de bază și clinice. J Diabetes Complicat 31 (4): 773–779. https://doi.org/10.1016/j.jdiacomp.2016.12.010
Hesselbarth N, Pettinelli C, Gericke M et al (2015) Tamoxifenul afectează parametrii metabolismului glucozei și lipidelor, provoacă rumenirea țesutului adipos subcutanat și modificări tranzitorii ale compoziției corpului la șoarecii C57BL/6NTac. Biochem Biophys Res Commun 464 (3): 724-729. https://doi.org/10.1016/j.bbrc.2015.07.015
Ye R, Wang QA, Tao C și colab. (2015) Impactul tamoxifenului asupra urmăririi liniei adipocitelor: inductor al adipogenezei și translocație nucleară prelungită a cre recombinazei. Mol Metab 4 (11): 771–778. https://doi.org/10.1016/j.molmet.2015.08.004
Nguyen MC, Stewart RB, Banerji MA și colab. (2001) Relațiile dintre utilizarea tamoxifenului, grăsimea hepatică și distribuția grăsimii corporale la femeile cu cancer mamar. Int J Obes Relat Metab Disord 25 (2): 296-298. https://doi.org/10.1038/sj.ijo.0801488
Mulțumiri
Mulțumim Susan Berthold, Jenny Schuster și Eva Böge pentru asistență tehnică. Această lucrare a fost susținută de Deutsche Forschungsgemeinschaft (SFB1052/02, # 209933838, B01 (MB) și B04 (NK)) și susținută de Ministerul Federal al Educației și Cercetării (BMBF), Germania, FKZ: 01EO1001 (N. Klöting) și DZD: 82DZD00601.
Informatia autorului
Afilieri
Helmholtz Institute for Metabolic, Obesity and Vascular Research (HI-MAG) al Helmholtz Zentrum München, Universitatea din Leipzig și Spitalul Universitar Leipzig, Liebigstr. 20, 04103, Leipzig, Germania
Nora Klöting, Michael Stumvoll și Matthias Blüher
IFB AdiposityDiseases, Universitatea din Leipzig, Leipzig, Germania
Nora Klöting și Michael Stumvoll
Centrul german de diabet, Universitatea din Leipzig, Leipzig, Germania
Matthias Kern, Michele Moruzzi și Matthias Blüher
Departamentul de Medicină, Universitatea din Leipzig, Leipzig, Germania
Nora Klöting, Matthias Kern, Michele Moruzzi, Michael Stumvoll și Matthias Blüher
Puteți căuta acest autor și în PubMed Google Scholar
Puteți căuta acest autor și în PubMed Google Scholar
Puteți căuta acest autor și în PubMed Google Scholar
Puteți căuta acest autor și în PubMed Google Scholar
Puteți căuta acest autor și în PubMed Google Scholar
autorul corespunzator
Declarații de etică
Conflict de interese
Autorii declară că nu au niciun conflict de interese.
Divulgarea drepturilor omului și a animalelor
Au fost respectate toate orientările internaționale, naționale și/sau instituționale aplicabile pentru îngrijirea și utilizarea animalelor.
Consimțământ informat
Pentru acest tip de studiu, nu este necesar consimțământul formal.
Informatii suplimentare
Nota editorului
Springer Nature rămâne neutru în ceea ce privește revendicările jurisdicționale din hărțile publicate și afilierile instituționale.
- Direcționarea căii de semnalizare ERK ca tratament potențial pentru rezistența la insulină și tipul 2
- Prevenirea și tratamentul obezității, rezistenței la insulină și diabetului prin rășina care leagă acidul biliar
- Ciuperca unghiilor pe mâini - cauze ale educației și metode de tratament
- Cauzele piuriei, tratamentul și multe altele
- Pericardita - cauze, simptome; tratament British Heart Foundation