John M. Nolan (a) R, Riona Mulcahy (b), Rebecca Power (a), Rachel Moran (a) și Alan N. Howard (c)
(a) Nutrition Research Center Ireland, School of Health Science, Carriganore House, Waterford Institute of Technology, West Campus, Waterford, Irlanda
(b) Unitatea de îngrijire legată de vârstă, Spitalul Universitar Waterford, Waterford, Irlanda
(c) Fundația Howard, Cambridge, Marea Britanie
Acceptat la 17 aprilie 2018
Abstract.
Fundal: Un număr tot mai mare de dovezi științifice sugerează că îmbogățirea anumitor compuși nutriționali din creier poate reduce riscul bolii Alzheimer (AD).
Obiectiv: Pentru a investiga impactul carotenoizilor suplimentari ai xantofilelor plus acizilor grași omega-3 asupra progresiei bolii la pacienții cu AD.
Metode: Au fost efectuate trei experimente de încercare. În studiile 1 și 2 (efectuate la pacienți cu AD pe o perioadă de 18 luni), 12 pacienți (starea AD la momentul inițial: 4 ușoare și 8 moderate) au fost suplimentați cu o formulare de xantofilă numai carotenoidă (Formulare 1; luteină: mezo-zeaxantină: zeaxantină 10: 10: 2 mg/zi) și 13 pacienți (starea AD la momentul inițial: 2 ușoare, 10 moderate și 1 severe) au fost suplimentate cu o combinație de xantofilă carotenoidă și ulei de pește (Formulare 2; luteină: mezo-zeaxantină: zeaxantina 10:10: 2 mg/zi plus 1 g/zi de ulei de pește care conține 430 mg acid docohexaenoic [DHA] și 90 mg acid eicopentaenoic [EPA]), respectiv. În Procesul 3, 15 subiecți liberi de AD (grupul de control) au fost suplimentați timp de 6 luni cu Formularea 1. Răspunsul carotenoid al xantofilei din sânge a fost măsurat în toate studiile prin HPLC. Acizii grași omega-3 au fost profilați prin spectrometrie de masă prin perfuzie directă.
Rezultate: Creșterea concentrației carotenoidelor de xantofilă a fost semnificativ mai mare pentru Formularea 2 comparativ cu Formularea 1 (p 13 mg/zi).
A fost utilizat pachetul statistic IBM SPSS versiunea 22 și s-a aplicat nivelul de semnificație de 5% pentru toate analizele. SigmaPlot versiunea 8.0 a fost utilizată pentru a genera grafică de linie pentru prezentare. Rezultatele au fost exprimate ca medii ± abateri standard în tabele și medii ± erori standard pentru grafică. Diferențele între grupuri au fost analizate folosind eșantioane independente t-teste, analiza unică a varianței (ANOVA) sau teste chi-pătrat, după caz. Au fost utilizate analize ale varianței măsurilor repetate (rANOVA) pentru a evalua efectele de interacțiune Timp și/sau Timp-Grup între grupurile de intervenție de tratament pentru concentrațiile serice de L, Z și MZ. Efectele de timp examinează dacă o variabilă de răspuns este sau nu diferită la diferitele puncte de timp de interes. Efectele TimeGroup examinează dacă efectul timpului diferă sau nu între grupurile de intervenție a tratamentului, testând astfel impactul intervenției.
REZULTATE
Tabelul 1 de mai jos prezintă datele inițiale pentru pacienții cu AD și subiecții de control înrolați în cele trei studii. După cum se vede în acest tabel, pacienții cu AD în Trial 1 și Trial 2 au fost comparabili ca vârstă, sex, IMC, aport dietetic L/Z, concentrații serice de Z și categorie AD. Pacienții din Trial 2 au avut concentrații semnificativ mai scăzute de L în sânge decât pacienții din Trial 1 (p = 0,031). Alte observații notabile la momentul inițial au fost relațiile pozitive și semnificative statistic între aportul de L și Z din dietă și concentrațiile serice de L și Z (r = 0,601, p = 0,000 și r = 0,330, respectiv p = 0,043).
Răspuns biochimic: carotenoide xantofile și acizi grași omega-3
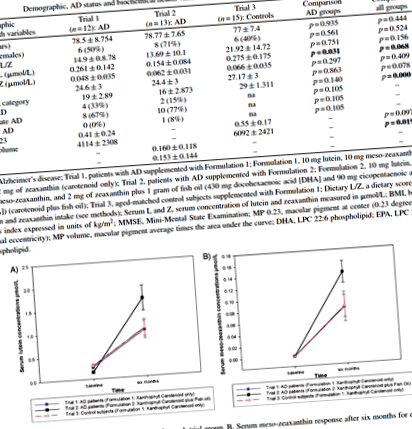
Creșterea observată în concentrațiile de L și MZ a fost semnificativ mai mare la pacienții cu AD care au fost suplimentați cu combinația de carotenoide xantofilă plus acizi grași omega-3 (Formularea 2), în comparație cu pacienții cu AD care au fost suplimentați cu formularea numai cu carotenoizi de xantofilă (Formularea 1) și în comparație cu grupul martor care au fost suplimentate cu formularea numai carotenoidă xantofilă (Formularea 1) (ser L: p = 0,002, Fig. 1A; ser MZ: p = 0,006, Fig. 1B). De asemenea, pentru Trial 2, concentrațiile de DHA și EPA au crescut în sângele pacienților cu AD (de remarcat, măsurătorile DHA și EPA au fost efectuate numai în acest studiu, deoarece celelalte studii nu au avut DHA sau EPA în formularea suplimentului). Creșterea observată în DHA, componenta principală a uleiului de pește utilizat în Formularea 2, a fost semnificativă statistic (p = 0,041, vezi Fig. 2).
Răspuns clinic/funcțional la pacienții cu boala Alzheimer
Figurile 3A și 3B prezintă starea AD pentru Procesul 1 la momentul inițial și, respectiv, la 18 luni. Figurile 4A și 4B prezintă starea AD pentru Procesul 2 la momentul inițial și, respectiv, la 18 luni. De remarcat, datele la 18 luni reprezintă observații medicale și starea de sănătate a pacientului (vezi Tabelul 2). După cum se vede din diagramele cu sectoare (Fig. 3A, B) și Tabelul 2, progresia AD a fost evidentă în acest grup (date din Procesul 1, intervenție numai xotofilă carotenoidă) pe parcursul perioadei de 18 luni, cu 42% din starea de sănătate a pacientului căzând până la punctul de a nu putea continua în proces. Motivele abandonului au fost: pacientul s-a mutat într-un azil de bătrâni din cauza progresiei AD și a imposibilității de a lua suplimentul; pacientul a devenit prea rău pentru a continua; declin cognitiv prea sever; nu mai poate urma instrucțiunile. Cu toate acestea, așa cum se vede în Fig. 4A și 4B (date din Procesul 2, carotenoid xantofilă și intervenție cu ulei de pește) și Tabelul 2, progresia AD a apărut mult mai puțin, îngrijitorii raportând beneficii funcționale în memorie, vedere și dispoziție. Analiza Pearson Chi-Square a demonstrat diferența semnificativă statistic între grupuri pentru modificările observate în starea AD de la momentul inițial până la 18 luni (p = 0,003).
- 20 de rețete pline de aplicații Bon pentru rețete cu acizi grași Omega-3; tit
- Cele mai importante povești din 2018 în domeniul cardiologiei sunt acizi grași omega-3 cardioprotectori, depinde ...
- Un caz de hipertrigliceridemie severă și acizi grași Omega-3
- O dietă bogată în acizi grași omega-3 cu lanț lung modulează sațietatea la voluntarii supraponderali și obezi
- Acizi grași polinesaturați omega-3 cu lanț lung cu text complet fără biomolecule în ecosistemele naturale