Divizia de malignități hematologice, Institutul de cancer Dana-Farber, Harvard Medical School, Boston, MA, SUA
Corespondență: Jorge J. Castillo, MD, Division of Hematologic Malignancies, Dana - Farber Cancer Institute, Harvard Medical School, 450 Brookline Ave, M221, Boston, MA 02215, SUA.
Divizia de hematologie și oncologie, Spitalul Miriam, Școala de medicină Warren Alpert a Universității Brown, Providence, RI, SUA
Program în Oncologie pentru femei, Spitalul pentru femei și sugari, Școala medicală Warren Alpert de la Universitatea Brown, Providence, RI, SUA
Divizia de hematologie și oncologie, Spitalul Miriam, Școala medicală Warren Alpert de la Universitatea Brown, Providence, RI, SUA
Divizia de malignități hematologice, Institutul de cancer Dana-Farber, Harvard Medical School, Boston, MA, SUA
Corespondență: Jorge J. Castillo, MD, Division of Hematologic Malignancies, Dana - Farber Cancer Institute, Harvard Medical School, 450 Brookline Ave, M221, Boston, MA 02215, SUA.
Divizia de hematologie și oncologie, Spitalul Miriam, Școala medicală Warren Alpert de la Universitatea Brown, Providence, RI, SUA
Program în Oncologie pentru femei, Spitalul pentru femei și sugari, Școala medicală Warren Alpert de la Universitatea Brown, Providence, RI, SUA
Divizia de hematologie și oncologie, Spitalul Miriam, Școala de medicină Warren Alpert a Universității Brown, Providence, RI, SUA
rezumat
Limfomul plasmablastic (PBL) este un limfom CD20 - negativ rar și agresiv. În ciuda îmbunătățirilor în biologia din spatele PBL, aceasta reprezintă încă o provocare din perspectivele de diagnostic și terapeutice pentru patologi și clinici. PBL se caracterizează prin rate ridicate de recidivă și supraviețuire medie scurtă cu abordări standard. Aici, raportăm utilizarea combinației de bortezomib și etopozidă perfuzabilă, prednison, vincristină, ciclofosfamidă și doxorubicină (V - EPOCH) la trei pacienți cu PBL; doi au fost HIV-pozitivi și unul a fost HIV-negativ. Toți cei trei pacienți au obținut un răspuns complet durabil la V - EPOCH cu timpi de supraviețuire de 24, 18 și respectiv 12 luni.
Limfomul plasmablastic (PBL) este o variantă negativă rară, agresivă a CD20 - limfom difuz cu celule B mari (DLBCL), care a fost descrisă inițial în cavitatea orală a pacienților cu virusul imunodeficienței umane (HIV) și colab, 1997). Mai recent, PBL a fost raportat la alte persoane imunosupresate, cum ar fi pacienții cu transplant de organe solide, precum și pacienții imunocompetenți (Morscio și colab, 2014). Indiferent de starea imunitară, se pare că există o asociere între PBL, infecția cu EBV și C-UL MEU aberații genetice (Castillo & Reagan, 2011). Din punct de vedere patologic, PBL se caracterizează printr-o lipsă de expresie CD20 și de exprimare a markerilor de celule plasmatice precum CD38 și MUM-1/IRF-4, cu un indice de proliferare ridicat (Stein și colab, 2008). Celula de origine a PBL este plasmablastul, o celulă B activată în procesul de diferențiere plasmacitică, dar care nu a devenit încă o plasmă celulă în repaus. Prognosticul PBL este uniform slab folosind schemele de chimioterapie tradiționale cu supraviețuire globală (OS) de aproximativ 12 luni și colab, 2012). Aici, vă prezentăm experiența noastră cu trei pacienți cu PBL tratați cu combinația de bortezomib și EPOCH ajustat la doză (etopozidă, doxorubicină și vincristină, împreună cu ciclofosfamidă în bolus și prednison).
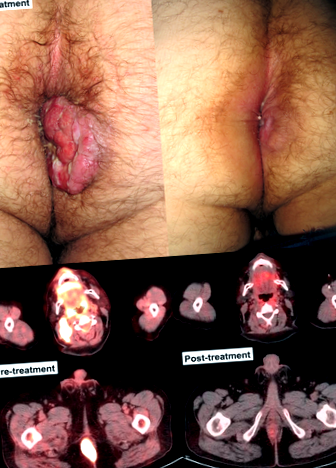
Pacientul 3 este un gastroenterolog de sex masculin, în vârstă de 66 de ani, cu antecedente de diverticulită, care a prezentat un curs de 2 săptămâni de agravare a durerii abdominale a cadranului inferior stâng, hematochezie și constipație. După un proces eșuat de antibiotice, pacientul a decis să se autodescopere și a găsit o masă sigmoidă neobstructivă de 5 cm (stenoză 75%) situată la 25 cm de marginea anală. Nu au fost febrile, transpirațiile nocturne sau pierderea în greutate. Starea de performanță a fost ECOG 0. CT nu a dezvăluit domenii suplimentare de implicare. Pacientul a suferit o hemicolectomie stângă de la flexura splenică la joncțiunea rectosigmoidă. Examinarea patologică a masei și a șase din 21 ganglioni limfatici a relevat implicarea difuză a celulelor mari cu nuclei rotunzi. Celulele maligne au fost negative pentru CD19 și CD20, dar pozitive pentru CD138 și MUM-1/IRF-4. Expresia KI-67 a fost> 90%. MYC a fost exprimat în 15% din celulele maligne. HIV ELISA a fost negativ, iar măduva osoasă nu a fost implicată. Diagnosticul final a fost stadiul II PBL la un individ HIV-negativ, altfel imunocompetent. PET/CT efectuate după operație, dar înainte de inițierea terapiei nu au prezentat zone de aviditate crescută a FDG.
Fiecare pacient a fost inițiat pe EPOCH ajustat la doză în asociere cu bortezomib la o doză de 1,3 mg/m2 administrată subcutanat (SQ) în zilele 1, 4, 8 și 11 pe un ciclu 21 - d (V - EPOCH). Terapia de susținere a constat în aciclovir zilnic 400 mg PO de două ori pe zi sau valaciclovir 1000 mg PO o dată pe zi pentru profilaxia herpesului zoster, trimetoprim/sulfametoxazol PO dublu o dată pe zi de trei ori pe săptămână sau dapsonă 100 mg PO o dată pe zi Pneumocystis carinii profilaxie și pegfilgrastim 6 mg SQ în ziua 6 a V - EPOCH. Citarabina lipozomală intratecală 50 mg a fost administrată în ziua 2 a fiecărui ciclu. Înainte de injecția intratecală, s-au obținut 5-10 cc lichid cefalorahidian și au fost supuse analizei citometriei în flux.
Aici, raportăm trei pacienți cu diagnostic patologic de PBL, doi pacienți HIV-pozitivi și un pacient HIV-negativ aparent imunocompetent, tratați cu linia frontală V-EPOCH. Pacienții au obținut un răspuns complet și rămân lipsiți de boală după terminarea terapiei, cu toxicitate relativ acceptabilă pe termen scurt, dar fără toxicitate pe termen lung. Având în vedere rezultatele slabe ale PBL cu CHOP standard (ciclofosfamidă, doxorubicină, vincristină și prednison), recomandarea Rețelei Naționale Comprehensive pentru Cancer este în favoarea terapiilor mai intensive, cum ar fi EPOCH (Wilson și colab, 2008). EPOCH perfuzional este o opțiune rezonabilă la pacienții cu limfoame agresive cu sau fără infecție cu HIV. Într-o analiză recentă a mai multor 1500 de pacienți cu infecție HIV, utilizarea EPOCH perfuzională a apărut asociată cu rezultate mai bune (Barta și colab, 2012). În prezent, grupul B pentru cancer și leucemie studiază, într-un studiu controlat randomizat, rituximab în combinație cu CHOP sau EPOCH la pacienții cu DLBCL cu profil molecular molecular încorporat (NCT00118209). De asemenea, Institutul Național al Cancerului evaluează EPOCH la pacienții cu DLBCL MYC-pozitiv, pentru care pacienții cu PBL sunt de asemenea eligibili (NCT01092182).
S-a dovedit că inhibitorul proteazomului bortezomib este foarte activ în mielom, pentru care este aprobat în Europa și Statele Unite. Bortezomib a demonstrat activitate preclinică și clinică în alte limfoame negative CD20, cum ar fi limfomul primar și colab, 2004; Sarosiek și colab, 2010). Bortezomib a arătat, de asemenea, eficacitate în mod specific la pacienții cu DLBCL cu celule B centrate activate sau post-germinale (Dunleavy și colab, 2009), oferind o justificare pentru utilizarea sa în PBL. Rapoartele de caz din trecut citează răspunsuri tranzitorii folosind inhibitorul proteazomului bortezomib singur și în combinație cu chimioterapie la pacienții cu PBL cu boală recidivantă (Bibas și colab, 2010; Salut și colab, 2014; Yan și colab, 2014). Credem că regimul V - EPOCH oferă posibilitatea de a îmbunătăți rezultatele pacienților cu PBL, la care este nevoie disperată de dezvoltarea unor terapii mai eficiente.
În concluzie, prezentăm un raport privind utilizarea V-EPOCH la pacienții cu PBL. Această combinație a prezentat eficacitate și un profil de toxicitate relativ acceptabil. Studiul nostru prezintă limitări evidente, cum ar fi proiectarea sa retrospectivă și dimensiunea redusă a eșantionului, dar lăsați acest lucru să servească drept o platformă potențială pentru a dezvolta studii terapeutice prospective multi-instituționale care vizează afectarea pozitivă a rezultatelor pacienților cu limfoame negative CD20, care sunt puțin probabil să obțină beneficii din adăugarea de anticorpi monoclonali anti-CD20 la chimioterapie.
Mulțumiri
JJC a proiectat studiul. JJC, JLR, WMS și ESW au oferit îngrijiri medicale pacienților. JJC și JLR au scris manuscrisul.
Dezvăluiri
Autorii nu au niciun conflict de interese de dezvăluit.
- 93% reducere Vita Skin Medical Clinic Tratament de albire și slăbire
- Simptome ale anorexiei nervoase; Tratarea semințelor speranței
- Definiția, simptomele, diagnosticul și tratamentul bronhiectaziei Britannica
- Vânătăi Simptome, cauze, diagnostic, tratament, remedii, prevenire
- Simptome, cauze, tratament, semne de avertizare ale sternului învinețit