Abstract
Restricția calorică (CR) extinde durata de viață și s-a demonstrat că reduce bolile legate de vârstă, inclusiv cancerul, diabetul și bolile cardiovasculare și neurodegenerative în modele experimentale. Studii translaționale recente au testat potențialul mimeticelor CR sau CR ca terapii adjuvante pentru a spori eficacitatea chimioterapiei, radioterapiei și a imunoterapiilor noi. CR cronic este dificil de utilizat la pacienții cu cancer și, prin urmare, postul intermitent, medicamentele mimetice CR sau dietele alternative (cum ar fi o dietă ketogenică) pot fi mai potrivite. S-a demonstrat că postul intermitent îmbunătățește tratamentul atât cu chimioterapie, cât și cu radioterapie. CR și postul determină răspunsuri diferite în celulele normale și canceroase și reduc anumite efecte secundare ale terapiei citotoxice. Rezultatele studiilor preclinice ale medicamentelor mimetice CR și ale altor intervenții dietetice, cum ar fi dieta ketogenică, sunt promițătoare pentru îmbunătățirea eficacității terapiilor anticancerigene și reducerea efectelor secundare ale tratamentelor citotoxice. Studiile clinice actuale și viitoare vor informa cu privire la ce tipuri de cancer și la ce etapă a procesului de cancer, schemele CR, post sau CR mimetic se vor dovedi cele mai eficiente.
fundal
Restricție calorică (CR) și cancer
Axa AMPK/mTOR controlează, de asemenea, autofagia, un proces prin care proteinele, macronutrienții și organele sunt învelite în vezicule cu membrană dublă și degradate în blocuri care pot fi apoi transportate în căi sintetice. În condiții de CR, activarea AMPK stimulează autofagia crescută pentru a recicla componentele celulare și a furniza substraturile necesare pentru metabolism și homeostazie [4, 15]. Autofagia poate acționa ca o sabie cu două tăișe în cancer - se crede că este supresivă a tumorilor, deoarece defectele autofagiei determină stresul oxidativ, defectele mitocondriale, deteriorarea ADN-ului, instabilitatea genomică și creșterea tumorii [25]. În schimb, se crede că promovează tumorile, deoarece tumorile stabilite pot utiliza autofagia pentru a reduce stresul oxidativ și pentru a crește funcția mitocondrială și metabolismul pentru a promova supraviețuirea și a depăși stresul și condițiile nutriționale scăzute [25, 26]. Datorită rolului dublu al autofagiei în cancer, inductorii și inhibitorii autofagiei au devenit ținte pentru terapia cancerului [27]. Cercetări recente efectuate în laboratorul nostru au arătat că combinarea inhibiției autofagiei cu un regim CR a redus creșterea tumorii mai mult decât oricare dintre tratamente [20].
RC și răspuns terapeutic
Lucrare elegantă de Rafaghello și colab. [40] a demonstrat că postul pe termen scurt determină răspunsuri diferențiale la chimioterapie în celulele normale și canceroase, celulele normale inactivând semnale de creștere, precum Ras, Akt și IGF-1, ca răspuns la postul pe termen scurt, protejându-le de toxicitatea terapeutică. În schimb, celulele canceroase, care au apărut datorită activării acestor semnale și evaziunea semnalelor care induc senescența, nu suferă această inactivare, rămânând vulnerabile la tratamentul citotoxic prin chimioterapie sau radioterapie. Inducerea acestor răspunsuri la stres specifice cancerului poate avea impact asupra mecanismelor legate de chimiorezistență, inclusiv rezistența multidrog [46].
În timp ce studiile preclinice se intensifică asupra efectelor CR intermitente în combinație cu chimioterapie și radioterapie, studiile clinice sunt lent de urmat, probabil din cauza preocupărilor enumerate mai sus. Un rezumat al studiilor clinice anterioare și actuale ale RC intermitent, dietelor care mimează postul și dietelor ketogenice în combinație cu terapiile anticanceroase este inclus în Tabelul 1. Un mic studiu cuprinzând zece subiecți diagnosticați cu tumori maligne, inclusiv sân, esofag, prostată și plămâni, care a suferit un post de 48-140 h înainte și un post de 56 h post-chimioterapie a relevat o îmbunătățire semnificativă a efectelor secundare auto-raportate ale terapiei, inclusiv greață, vărsături, diaree, slăbiciune și oboseală [51, 52].
În prezent sunt în curs de desfășurare studii mai mari pentru a determina potențialul de post pe termen scurt în reducerea efectelor secundare și a eficacității chimioterapiilor și vor fi probabil punctul de lansare pentru viitoarele studii clinice cu CR intermitent ca terapie adjuvantă potențială.
Mimetice CR
Având în vedere preocupările nutriționale ale RC și ale postului la unii pacienți cu cancer, mimeticele CR, și anume agenții farmacologici care vizează căile afectate de CR, cum ar fi rapamicina, metformina, resveratrolul și hidroxicitratul, sunt strategii atractive pentru a imita efectele protectoare ale RC atât pentru cancer prevenirea și ca terapii adjuvante fără restricție dietetică. Aceste mimetice CR afectează inflamația și metabolismul sistemic și specific tumorilor, iar vizarea acestor căi poate sensibiliza cancerele la terapiile tradiționale și emergente anti-cancer prin reducerea inflamației asociate tumorii sau provocând stres metabolic în celula canceroasă.
Administrarea rapamicinei mimetice CR (sirolimus), un medicament imunosupresor și inhibitor stabilit al mTOR, extinde durata de viață și întârzie cancerul la șoareci [53]. Laboratorul nostru a arătat că rapamicina sau analogul său, Afinitor® (everolimus), pot imita efectele anticancerigene ale RC la modelele de șoarece de pancreas și cancer de sân [54, 55]. Semnalizarea prin calea mTOR a fost implicată într-o gamă largă de cancere chimiorezistente [56], iar rapamicina s-a dovedit că inversează rezistența multidrog [57]. Studiile preclinice promițătoare demonstrează că rapamicina poate sensibiliza anumite tipuri de cancer la chimioterapie și radioterapie. Studiile clinice active de fază I și II sunt în desfășurare pentru a determina efectul combinării rapamicinei cu regimuri chimioterapeutice, inclusiv gemcitabină pentru osteosarcom, ciclofosfamidă, dexametazonă în mielom și mitoxantronă, etopozidă și citarabină pentru leucemie.
O altă mimetică CR, metformina, este o biguanidă utilizată în mod obișnuit pentru tratarea diabetului de tip 2 prin inhibarea gluconeogenezei prin activarea indirectă a AMPK, reducând astfel glicemia și insulina la nivelurile observate la șoarecii CR [58]. Metformina, ca monoterapie, suprimă dezvoltarea și/sau creșterea tumorii în mai multe modele experimentale, incluzând modele de cancer de colon, mamar și hematopoietic [59]. Metformina s-a dovedit a fi promițătoare atât în studiile preclinice cât și în cele clinice, îmbunătățind tratamentul cancerelor de colon, sân, ovar, prostată și plămâni [60, 61]. Mai multe studii de fază II sunt în curs de desfășurare pentru a evalua metformina ca terapie combinată potențială, inclusiv un studiu cu cancer pulmonar cu celule mici, care implică o dietă cu conținut scăzut de glucide.
Resveratrolul, un compus polifenolic găsit în struguri, fructe de pădure și, cel mai faimos, în vinul roșu, a fost, de asemenea, luat în considerare ca un mimetic CR. Se crede că resveratrolul stă la baza „paradoxului francez”, în care se crede că consumul de vin roșu reduce ratele mortalității cauzate de bolile cardiovasculare și anumite tipuri de cancer [62]. Resveratrolul prezintă proprietăți antiinflamatoare, anti-oxidante și anti-angiogene [63] și suprimă dezvoltarea și creșterea a numeroase tipuri de cancer în modele preclinice, inclusiv sân, prostată, colon și ficat. Deși mai multe studii in vitro și in vivo au indicat că resveratrolul poate spori tratamentele anticancer [64], Fukui și colab. [65] a sugerat că resveratrolul poate reduce efectiv eficacitatea tratamentului cu paclitaxel în cancerul de sân. Prin urmare, ar trebui efectuate mai multe studii preclinice înainte de a trece la studiile clinice care examinează resveratrolul ca terapie adjuvantă împotriva cancerului.
Un mimetic CR emergent este hidroxicitratul, un derivat al acidului citric și un medicament fără prescripție medicală pentru scăderea în greutate care inhibă ATP citrat liasa, enzima care catalizează conversia citratului în oxaloacetat și acetil CoA. Celulele canceroase utilizează acetil CoA ca precursor sintetic pentru a alimenta proliferarea și creșterea [66]; astfel, blocarea sintezei de acetil CoA este o abordare rațională pentru a viza în mod specific metabolismul cancerului. Mai mult, hidroxicitratul este un puternic inductor al autofagiei. Cu toate acestea, administrarea de hidroxicitrat singură nu afectează glucoza sistemică sau insulina [67]. Mai mult, deși Pietrocola și colab. [41] a arătat efecte anticanceroase îmbunătățite care combină hidroxicitratul cu doxorubicina și ciclofosfamida, un mic studiu nu a evidențiat niciun beneficiu suplimentar al hidroxicitratului atunci când este administrat cu acid α-lipoic, alături de standardul de îngrijire [68].
Abordări dietetice alternative
IER, cum ar fi dieta 5-2, în care o persoană respectă restricții severe (cu 75% mai puține calorii) în 2 zile non-consecutive în timp ce mănâncă o dietă normală și sănătoasă în restul de 5 zile, a fost o abordare de succes a pierderii în greutate în studii la om și are ca rezultat îmbunătățiri similare ale parametrilor metabolici, cum ar fi sensibilitatea la insulină [3]. În prezent se desfășoară un studiu randomizat care compară IER și CR cronică în combinație cu tratamentul cu taxan la pacienții cu cancer mamar. Rezultatele preliminare din acest studiu sugerează că IER este tolerabil la pacienții care primesc chimioterapie, iar rezultatul acestui studiu se va adăuga dovezilor pentru CR ca tratament de susținere și va evalua IER ca o alternativă fezabilă la CR ca terapie anticancerigenă.
Concluzii
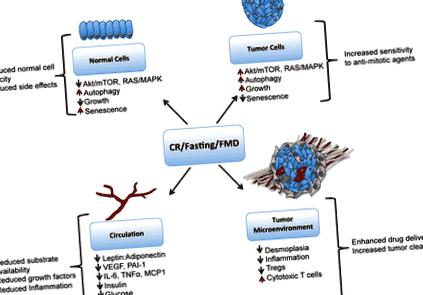
Mecanisme prin care restricția calorică (CR) afectează răspunsul la terapia anticancerigenă. CR, dietele sau dietele care mimează postul (FMD) determină reducerea semnalizării Akt/mTOR și Ras în celulele normale, rezultând senescență, creștere redusă și protecție împotriva tratamentului citotoxic, în timp ce în celulele tumorale rămân semnale oncogene și celulele sunt sensibile la terapii anti-mitotice. CR, postul și febra aftoasă reduc, de asemenea, citokinele pro-inflamatorii în circulație și în nișa micro-mediului tumoral, precum și reducerea leptinei, insulinei, IGF-1 și glucozei. CR poate reduce desmoplasia din jurul țesutului tumoral, ceea ce poate facilita o mai bună administrare terapeutică a medicamentului către celulele tumorale. CR poate ajuta, de asemenea, în imunosupravegherea tumorilor prin reducerea populațiilor Treg care inhibă celulele T citotoxice CD8 +. Această cifră nu a fost publicată în altă parte
- Beneficiile surprinzătoare ale restricției de calorii Grupul medical din Florida de Sud
- Două lucrări interesante de restricție a caloriilor; Lupta împotriva îmbătrânirii!
- Evaluarea ultrasonografică a tulburărilor anovulatorii la femeile slabe și supraponderale - Vizualizare text complet
- Studiul de traducere a greutății în greutate - Vizualizare text complet
- Actualizare privind restricționarea caloriilor și pierderea oaselor; Lupta împotriva îmbătrânirii!