Abstract
Nefrolitiaza este o problemă comună asociată cu costuri semnificative pentru sistemul de sănătate. Prevalența sa continuă să crească, în special la femei, care este atribuită schimbărilor în dietă și stil de viață. Costurile asociate cu evaluarea și gestionarea nefrolitiazei în Statele Unite au fost estimate la 1,83 miliarde de dolari și, fără nicio intervenție, riscul de recurență este mare. Acest articol trece în revistă opțiunile de gestionare a nefrolitiazei, inclusiv o nouă formulare de citrat de potasiu, Urocit®-K 15 mEq, care permite o flexibilitate de dozare care poate duce la îmbunătățirea conformității și tolerabilității.
Incidența nefrolitiazei la nivel mondial este de aproximativ 1%. În Statele Unite, prevalența a crescut de la 3,2% în anii 1970 la 5,2% în anii 1990. 1 Un studiu recent sugerează că prevalența bolilor de calculi continuă să crească, în special la femei, despre care se crede că se datorează schimbărilor în dietă și stil de viață. 2 Costurile asociate cu evaluarea și gestionarea nefrolitiazei în Statele Unite au fost estimate la 1,83 miliarde de dolari. 3 Ratele de recurență pentru boala de piatră sunt ridicate. După o piatră inițială, există o șansă de 30% până la 50% de a forma oa doua piatră în 5 ani.
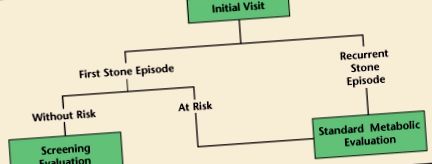
Având în vedere rata mare de recurență după un episod de calcul pentru prima dată, este necesară o evaluare metabolică inițială pentru a căuta cauzele care stau la baza nefrolitiazei. La pacienții care prezintă un singur episod de calcul, ar trebui făcută o evaluare a riscului pentru a determina amploarea evaluării (Figura 1). Există o serie de factori asociați cu riscul crescut de formare recurentă a pietrei (Tabelul 1). Acestea includ afecțiuni medicale, cum ar fi diabetul zaharat sau antecedente familiale de pietre la rinichi. În plus, anumite medicamente, cum ar fi topiramatul și guaifenesina, pot contribui, de asemenea, la formarea pietrei. Obezitatea este, de asemenea, un factor major de risc pentru nefrolitiază. 4 Pacienții cu oricare dintre acești factori de risc trebuie considerați expuși riscului și trebuie să fie supuși unei evaluări metabolice standard (IMM) (Tabelul 2). În plus, formatorii de piatră recurenți ar trebui să fie supuși unui IMM. Pentru formatorii de piatră pentru prima dată fără factori de risc, ar trebui efectuată o evaluare de screening care constă dintr-un istoric amănunțit, chimii serice de bază și o analiză a urinei. Orice pietre colectate ar trebui, de asemenea, trimise spre analiză.
Algoritm pentru evaluarea diagnosticului.
tabelul 1
Factori de risc pentru dezvoltarea pietrei
Istoria familiei pietrelor
Infecție cronică a tractului urinar
Diabetul de tip II
Compoziția specifică a pietrei (acid uric sau cistină)
masa 2
Identificarea anomaliilor metabolice utilizând evaluarea metabolică standard
| Găsirea urinară | Tulburări dietetice-de mediu implicate |
| Volumul total (TV) 200 mEq/zi | Abuz de sare |
| Oxalat (Bo)> 45 mg/zi | Aportul de alimente bogate în oxalat, aport foarte scăzut de calciu |
| Calciu (Ca)> 250 mg/zi | Aport ridicat de calciu în unele cazuri |
| Acid uric (UA)> 600 mg/zi | Aport ridicat de proteine animale |
| Sulfat (SO4)> 30 mmol/zi | Aport excesiv de proteine animale |
| Citrat 5 Aportul dietetic de sodiu și oxalat trebuie limitat. De asemenea, pacienții trebuie instruiți să reducă la minimum consumul de proteine animale. În general, aportul de calciu nu trebuie restricționat nici la cei cu hipercalcurie. Recomandarea pentru pacienții cu hipercalcurie trebuie să fie un aport modest de calciu, aproximativ 800 mg/zi sau 2 până la 3 porții de lactate pe zi. |
Hipercalcuria este definită ca urină calcică mai mare de 250 mg/zi. Cea mai frecventă cauză a creșterii calciului în urină este hipercalcuria absorbantă. La pacienții cu un nivel crescut de calciu seric și hipercalcurie, ar trebui urmărit un tratament pentru hiperparatiroidism. Pentru pacienții cu urină de calciu modest crescută și sodiu crescut de urină, poate fi oferit un studiu privind restricția de sodiu ca tratament inițial. Pentru pacienții cu urină normală de sodiu sau calciu în urină marcat crescut, precum și pentru cei care nu respectă restricția de sodiu, tratamentul de alegere este tratamentul farmacologic cu un diuretic tiazidic. Cei mai comuni agenți utilizați sunt indapamida 1,25 până la 2,5 mg/zi sau clorthalidona 25 până la 50 mg/zi. Atunci când se utilizează acești agenți, trebuie asigurată suplimentarea cu potasiu din cauza îngrijorării pentru hipokaliemie. Citratul de potasiu (Urocit®-K 15, Mission Pharmacal, San Antonio, TX) este agentul preferat, deoarece va crește și citratul urinar. De obicei, o doză inițială ar fi Urocit-K 15 mEq la micul dejun și 30 mEq la cină. Pentru pacienții cu pH urinar crescut (> 6,5), clorura de potasiu poate fi substituită cu citrat de potasiu din cauza îngrijorării supraalcalinizării.
Nivelurile ridicate de acid uric în urină pot provoca nefrolitiaza hiperuricosurică de oxalat de calciu. Hiperuricosuria este definită ca niveluri de acid uric urinar mai mari de 800 mg/zi. Pacienții trebuie sfătuiți să limiteze aportul de proteine animale la 6-8 oz zilnic. Dacă nivelurile de acid uric nu reușesc să se corecteze cu măsuri conservatoare, poate fi prescris alopurinol 300 mg/zi. 6 Citratul de potasiu este o alternativă la alopurinol. 7 Urocit-K 15 mEq la micul dejun și la cină poate fi util la pacienții cu hiperuricosurie modestă, în special la cei cu hipocitraturie.
Citratul este un inhibitor important al formării pietrei. Inhibă cristalizarea sării de calciu și crește pH-ul urinar acționând ca un tampon. Hipocitraturia, definită ca citrat urinar mai mic de 500 mg/zi, este un factor de risc pentru nefrolitiaza calciului. S-a demonstrat că citratul de potasiu reduce ratele de formare a calculilor cu 96% la pacienții cu hipocitraturie. 8 S-a dovedit că răspunsul la citratul de potasiu este durabil. 9 Cu o mediană de urmărire de 41 de luni, pH-ul urinar și nivelurile de citrat au rămas semnificativ mai mari la pacienții tratați cu citrat de potasiu în comparație cu valorile de pretratament. Citratul de potasiu a scăzut, de asemenea, semnificativ rata de formare a calculilor în acest studiu clinic pe termen lung (Figura 2). Dozajul trebuie titrat cu un obiectiv de citrat urinar mai mare de 500 mg/zi. Urocit-K a fost formulat recent într-o tabletă de 15 mEq, oferind o mai mare flexibilitate de dozare și potențialul de a reduce numărul total de tablete necesare. O doză inițială rezonabilă pentru hipocitraturia modestă ar fi un Urocit-K 15 mEq cu micul dejun și cina. Pentru pacienții cu hipocitraturie mai semnificativă, recomandarea este pentru Urocit-K 15 mEq la micul dejun și 30 mEq la cină.
Formarea pietrei determină pretratarea și posttratarea cu citrat de potasiu. 9
Nefrolitiaza acidului uric idiopatic este frecvent asociată cu diateza gută sau cu un pH urinar scăzut. Alcalinizarea urinei nu numai că poate preveni formarea viitoarelor pietre de acid uric, dar poate dizolva pietrele existente. Scopul alcalinizării ar trebui să fie un pH urinar între 6,0 și 6,5. Acest lucru se realizează cel mai bine cu citratul de potasiu. Urocit-K este de obicei prescris cu o doză cuprinsă între 15 și 30 mEq la micul dejun și la cină. Doza poate fi titrată pentru a obține pH-ul dorit. În cazurile în care pacienții continuă să formeze calculi de acid uric în ciuda alcalinizării adecvate sau dacă nivelurile serice de acid uric depășesc 8 mg/dl, se poate adăuga 300 mg alopurinol/zi.
Citratul de potasiu are un rol și în tratamentul calculilor cu cistină. Pacienții cu pietre de cistină trebuie instruiți să își mărească aportul de lichide pentru a menține un volum de urină mai mare de 4 L/zi. În plus, citratul de potasiu trebuie prescris pentru a menține pH-ul urinar între 6,5 și 7,0. Doza uzuală ar fi Urocit-K 15 până la 30 mEq cu micul dejun și cina. Tiopronina (Thiola®, Mission Pharmacal) trebuie inițiată atunci când concentrația de cistină este mai mare de 250 mg/L. Tiola se începe cu 200 mg de două ori pe zi. Doza este ajustată pentru a menține concentrațiile urinare de cistină sub 200 mg/L.
Pietrele de infecție sau pietrele de struvit sunt asociate cu bacterii care scindează ureasa. Pacienții prezintă adesea infecții recurente ale tractului urinar și pietre mari. Pacienții cu o analiză de piatră care dezvăluie struvit 100% nu necesită adesea un IMM. Dacă sunt prezenți factori de risc sau dacă există o componentă a nefrolitiazei de calciu pe analiza calculilor, ar trebui luată în considerare un IMM. Tratamentul pietrelor infectate constă în îndepărtarea completă a pietrei. Pacienții trebuie, de asemenea, tratați cu antibiotice profilactice. Acidul acetohidroxamic (Lithostat®, Mission Pharmacal) este un inhibitor de uree care este util la pacienții la care nu se poate îndepărta întreaga piatră sau la pacienții cu infecție persistentă. Se prescrie la o doză de 250 mg de două ori pe zi. Orice anomalii metabolice asociate găsite pe un IMM trebuie tratate în mod adecvat.
Nefrolitiaza este o problemă comună asociată cu costuri semnificative pentru sistemul de sănătate. Prevalența nefrolitiazei continuă să crească. Fără intervenții, riscul de recurență este mare. Formatorii de piatră recurenți și formatorii de piatră pentru prima dată cu factori de risc pentru recurență ar trebui să fie supuși unui IMM. O etiologie subiacentă pentru formarea calculilor poate fi găsită la 97% dintre pacienți. Odată constatată o anomalie metabolică, poate fi inițiată terapia medicală direcționată (Figura 3). 10 Majoritatea medicamentelor utilizate pentru a preveni recurența pietrelor sunt bine tolerate și extrem de eficiente. În special, citratul de potasiu poate reduce ratele de formare a pietrei cu până la 96% și are efecte durabile pe termen lung. O nouă formulare de citrat de potasiu, comprimate Urocit-K 15 mEq, mărește flexibilitatea dozării, ceea ce duce la îmbunătățirea conformității și tolerabilității.
Managementul medical al nefrolitiazei de la ABC’s of Medical Management of Stones. 10
Punctele principale
Datorită ratelor ridicate de recurență după un episod de calcul pentru prima dată, se recomandă o evaluare metabolică inițială pentru a căuta cauzele care stau la baza nefrolitiazei. Factorii de risc includ diabetul sau antecedente familiale de calculi renali, utilizarea medicamentelor precum topiramat și guaifenesin și obezitate.
Indiferent de anomalia metabolică, se recomandă modificări dietetice, precum și creșterea aportului de lichide. Pacienții trebuie să-și limiteze aportul de sodiu și oxalat și să reducă la minimum consumul de proteine animale. Aportul de calciu nu trebuie restricționat.
Nivelurile ridicate de acid uric în urină pot provoca nefrolitiaza hiperuricosurică de oxalat de calciu. Pacienții trebuie să limiteze aportul de proteine animale la 6-8 oz zilnic. Dacă nivelurile de acid uric nu reușesc să se corecteze cu măsuri conservatoare, poate fi prescris alopurinol 300 mg/zi. Citratul de potasiu este, de asemenea, o alternativă la alopurinol.
Terapia medicală țintită poate fi inițiată odată ce se constată o anomalie metabolică. Medicamentele utilizate pentru prevenirea recurenței pietrelor sunt bine tolerate și extrem de eficiente. Citratul de potasiu poate reduce ratele de formare a pietrei cu până la 96% și are efecte durabile pe termen lung. Urocit-K 15®, o nouă formulare de citrat de potasiu, crește flexibilitatea dozării, ducând la o mai bună conformitate și tolerabilitate.
Note de subsol
O abordare simplă pas cu pas a diagnosticului și prevenirii nefrolitiazei este disponibilă în ABC-ul de management medical al pietrelor 10 și ABC-urile pietrelor la rinichi: Ghidul pacientului pentru a ajuta la prevenirea pietrelor renale recurente 11 la stonedisease.org sau o copie gratuită poate fi obținut de la Mission Pharmacal.
Glenn M. Preminger, MD, este consultant pentru Mission Pharmacal.
- Dieta și nutriția; New Horizon Medical »Managementul greutății controlat medical» Foxboro MA
- Sindromul metabolic ecvin-management dietetic și medical (Proceedings) DVM 360
- Managementul francez al centrului de referință al necrolizei epidermice Stevens-Johnson sindrometoxice -
- Servicii de alimentație dietetică în tratamentul pacienților obezi cu diabet zaharat - MedCrave online
- Modificarea punctelor finale pentru determinarea unui management eficient al obezității - ScienceDirect