Kelle H. Moley
1 Departamentul de obstetrică și ginecologie, Facultatea de Medicină a Universității Washington, St Louis, MO 63110, SUA
Graham A. Colditz
2 Departamentul de Chirurgie și Siteman Cancer Center, Washington University School of Medicine, St Louis, MO 63110, SUA
Abstract
Obezitatea crește riscul unor numeroase rezultate slabe pentru sănătate, inclusiv cancer. Obezitatea este deosebit de problematică la femei, deoarece atât ele, cât și descendenții lor pot prezenta un risc crescut de cancer. Studierea transmiterii riscului de cancer indus de obezitate este o provocare la om, dar studiile pe animale încep să dezvăluie mecanismele care stau la baza.
Aproape 70% dintre americani sunt supraponderali sau obezi (1). În plus, prevalența obezității sa dublat la copii și de patru ori la adolescenții din Statele Unite în ultimele trei decenii (2); în 2012, o treime din copii și adolescenți erau supraponderali sau obezi (3). Excesul de greutate și obezitatea prezintă atât adulții, cât și copiii cu un risc crescut de a avea rezultate slabe pentru sănătate. De exemplu, adulții sunt afectați de morbidități legate de obezitate, precum boli de inimă, boli cardiovasculare, accident vascular cerebral și diabet. La femei, dintre care 37% sunt obezi în Statele Unite (3), un indice de masă corporală crescut (IMC) crește riscul de anovulație, sindrom ovarian polichistic, infertilitate și complicații ale sarcinii (4). Chiar și la copiii mici, obezitatea este asociată cu factori de risc pentru bolile cardiovasculare, cum ar fi colesterolul crescut și tensiunea arterială crescută, și prediabetul cu hiperglicemie intermitentă. Adolescenții obezi au, de asemenea, rate mai mari de depresie, apnee în somn și probleme articulare și osoase decât colegii lor cu greutate normală.
Pe lângă aceste efecte asupra obezității asupra sănătății, numeroase studii au raportat că supraponderabilitatea și obezitatea sunt asociate cu un risc crescut de cancer (5). Femeile obeze prezintă un risc crescut de cancer endometrial, iar obezitatea la începutul vieții este asociată cu un risc crescut de mielom multiplu și limfom non-Hodgkin (6), precum și cancer de colon, rinichi și ficat (5). În contrast direct, adipozitatea copilăriei și adolescenților este invers legată de riscul de cancer mamar pe parcursul vieții (7). Obezitatea la adulți este, de asemenea, legată de riscul crescut de cancer al tiroidei, ovarului, colului uterin, esofagului, pancreasului, vezicii biliare și prostatei (8). În această perspectivă, evidențiem date clinice și tradiționale recente din studii care urmăresc să înțeleagă ferestrele de dezvoltare în care obezitatea are cel mai mare impact asupra riscului de cancer și mecanismele prin care riscul este conferit.
ÎN EXPUNERI DE UTERO ȘI DE VIE DE TIMP
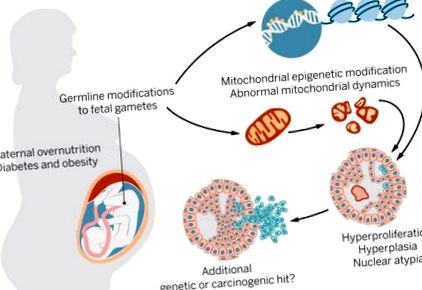
Printre statisticile privind obezitatea, una deosebit de alarmantă este că 37% dintre femeile în vârstă de reproducere (25 până la 54 de ani) sunt obeze (1). Acest lucru este alarmant, deoarece obezitatea maternă afectează dramatic sănătatea unei sarcini, iar studiile la rozătoare și la om demonstrează că efectele se manifestă într-o varietate de condiții la descendenți (4, 9, 10). Conform ipotezei dezvoltării originilor sănătății și bolilor, expunerile care apar în timpul vieții embrionare și fetale sunt esențiale pentru modelarea dezvoltării țesuturilor la descendenți (11). Acest lucru a fost exemplificat cel mai bine prin studii care au raportat defecte cardiometabolice la copiii mamelor care sunt obezi în timpul gestației [revizuită pe larg în (12)]. În plus, energetica maternă dereglementată a fost legată de dezvoltarea tumorilor mamare, tumorile de reproducere și hipofiză și hiperplazia de prostată (13). În special, un studiu recent din cohorta nașterii din Helsinki a constatat că obezitatea maternă este asociată pozitiv cu toate rezultatele cancerului la descendenții umani (14). În Fig. 1, rezumăm posibilele influențe materne asupra riscului de cancer la descendenți prin mitocondrii care funcționează defectuos și/sau semnături epigenetice dereglate.
Într-un mediu obezogen matern, celulele descendenților ar putea moșteni mitocondriile care funcționează defectuos și/sau semnături epigenetice dereglate. Aceste modificări contribuie la un mediu tisular caracterizat prin hiperplazie și atipie nucleară. Atunci când este combinat cu alte lovituri genetice sau cancerigene, acest fenotip predispus poate duce la cancer la descendenții expuși.
CREDIT: H. MCDONALD/MEDICINA TRANSLAȚIONALĂ ȘTIINȚĂ
O provocare a studierii transmiterii generaționale a riscului de cancer este latența lungă dintre expunerile perinatale și dezvoltarea cancerului, ceea ce face ca studiile prospective să fie dificile și costisitoare. De asemenea, studiile retrospective sunt contestate de faptul că, în momentul diagnosticării cancerului, amintirea greutății materne de către pacient în timpul sarcinii nu este fiabilă. Astfel, mulți au apelat la modele animale, cum ar fi șoareci și șobolani, care oferă timpi de generație mai scurți, capacitatea de a controla fereastra de timp a expunerii la obezitate și capacitatea de a controla strict compoziția dietei, permițând astfel evaluarea componentelor dietetice specifice.
O altă posibilitate puternică este că obezitatea maternă provoacă modificări ale metabolismului țesutului. De exemplu, mai multe studii pe animale au sugerat că consumul matern al unei diete obezogene, în timpul sau chiar înainte de gestație, modifică direct sănătatea atât a ovocitelor, cât și a embrionilor timpurii (28). În plus, s-au raportat modificări marcante ale structurii mitocondriale și ale funcției metabolice ale ovocitelor la șoareci femele după doar 6 săptămâni de consum al unei diete bogate în grăsimi/zaharoză (28, 29). Aceste diferențe mitocondriale materne ar putea fi reportate generației următoare, fie prin moștenirea mitocondrială, fie ca modificări epigenetice ale genomului nuclear sau mitocondrial. Aceste modificări ale liniei germinale ar putea afecta ulterior fiecare țesut din descendenți, predispunând descendenții la performanțe mitocondriale anormale și, probabil, la dezvoltarea cancerului în țesuturile sensibile.
În timp ce unele studii au abordat transmiterea riscului de cancer de sân și de prostată (13, 22), s-a făcut puține lucrări pentru a evalua mecanismele prin care obezitatea maternă crește riscul altor forme de cancer. Toate datele actuale sugerează că obezitatea maternă este legată de alte rezultate ale cancerului prin mecanisme secundare. De exemplu, o recenzie recentă a propus că obezitatea maternă influențează obezitatea și creșterea în greutate la descendenți și, prin urmare, predispune descendenții la cancer colorectal (30). Aceasta se bazează pe observația că obezitatea pacientului la diagnostic și creșterea în greutate în viața adultă sunt factori de risc pentru cancerul colorectal (30). Aceiași autori au sugerat, de asemenea, un mecanism similar pentru carcinomul hepatic. În cele din urmă, Walker și colegii săi au demonstrat că șoarecii ale căror mame au consumat o dietă bogată în grăsimi au un risc crescut de a dezvolta tumori de reproducere și hipofiză (31), dar nu a fost încă stabilit un mecanism.
OBEZITATEA ȘI REZULTATELE COPILĂRII ȘI ADOLESCENTE
OBEZITATE ÎN TIMPUL ANILOR DE REPRODUCERE
În general, se acceptă faptul că adipozitatea mai mare la începutul adulților și premenopauzei este legată de un risc mai mic de cancer de sân premenopauzal (38). Cu toate acestea, studii recente mai detaliate (39-41) privind schimbarea greutății pe parcursul vieții indică interacțiunea protecției prin adipozitatea copilăriei și efectul advers al creșterii în greutate a adulților. Datele prospective europene au arătat că creșterea în greutate în timpul vârstei de 40 până la 50 de ani a fost asociată cu un risc ulterior de cancer de sân după vârsta de 50 de ani (39). Alte studii pe femei în vârstă de 40 de ani au legat creșterea în greutate de riscul de cancer de sân pre și postmenopauză (40). În studiul de sănătate al asistenților medicali, creșterea în greutate recentă de peste 4 ani a fost asociată cu un risc crescut de cancer mamar premenopauzal, iar riscul a fost mai mare pentru boala ER - receptor negativ pentru progesteron (PR -) și ER + PR - decât pentru ER + PR + boală (41). Mai mult, obezitatea crește factorul 1 de creștere asemănător insulinei (IGF1) atât la femeile cu greutate normală, cât și la femeile supraponderale și este asociată cu un risc crescut de cancer mamar premenopauzal și postmenopauzal (42).
OBEZITATEA DUPĂ MENOPAUZĂ
Riscul de cancer mamar se acumulează pe parcursul vieții, rezumat aici prin perioade de timp etichetate ca viață fetală, copilărie și copilărie, adolescență, premenopauză și postmenopauză, deoarece delimitarea acestor perioade variază modest între femei. Relația adipozității cu viitorul risc de cancer mamar este prezentată în raport cu riscul de cancer la femeile cu IMC în intervalul normal.
CREDIT: H. MCDONALD/MEDICINA TRANSLAȚIONALĂ ȘTIINȚĂ
Obezitatea este, de asemenea, legată de recurența cancerului de sân și de moartea după cancerul de sân (47). O meta-analiză a 82 de studii arată că obezitatea se corelează cu recurența (creșterea riscului cu creșterea IMC) (47). Această revizuire sistematică și meta-analiză a inclus peste 200.000 de femei cu cancer de sân și peste 40.000 de decese. Pentru femeile obeze comparativ cu femeile cu greutate normală, riscul relativ de deces prin cancer de sân a fost de 1,75 pentru femeile cu premenopauză și 1,34 pentru cancerul de sân postmenopauză. Important, nu a existat niciun efect protector al obezității asupra supraviețuirii la femeile aflate în premenopauză. Creșterea mortalității poate fi mediată prin concentrații mai mari de estrogen și concentrații mai mari de insulină în rândul femeilor obeze, deoarece ambii hormoni au fost corelați cu un prognostic slab la femeile cu cancer de sân (48).
PIERDERE ÎN GREUTATE
Dovezile dacă pierderea în greutate susținută reduce incidența cancerului sunt limitate, în mare parte din cauza succesului scăzut pe termen lung al intervențiilor de slăbire. Cu toate acestea, pierderea în greutate după intervenția chirurgicală bariatrică este mai susținută decât după alte intervenții și este protectoare împotriva cancerului endometrial (49). În plus, pierderea în greutate după menopauză a fost legată de riscul redus de cancer de sân postmenopauză (50) și un studiu a sugerat că scăderea în greutate de peste 5 kg după vârsta de 18 ani a redus riscul de cancer de sân premenopauzal (51). Numeroase studii care examinează efectele intervențiilor de scădere în greutate au evaluat markeri intermediari, cum ar fi concentrațiile hormonale (52, 53), dar până în prezent nu s-au efectuat studii care să investigheze efectele intervențiilor de scădere în greutate susținută asupra incidenței cancerului.
La șoareci de tip sălbatic, greutatea și fenotipul metabolic se normalizează odată cu exercițiile fizice și/sau pierderea în greutate, dar până în prezent, niciun studiu nu a analizat în mod direct inversarea progresiei tumorii (54). Într-un studiu recent, investigatorii au hrănit o dietă obezogenă la un model de șoarece predispus la dezvoltarea cancerului de sân bazal și au constatat că creșterea tumorii a fost prevenită atunci când șoarecii obezi au fost induși să piardă în greutate trecând la o dietă de control cu conținut scăzut de grăsimi înainte de debutul tumorii ( 55).
IMPLICAȚII TRANSLAȚIONALE
Aportul excesiv de energie în raport cu cheltuielile are ca rezultat un echilibru energetic pozitiv, creșterea în greutate în exces și numeroase afecțiuni cronice. Desfășurarea momentului expunerii la excesul de adipozitate în raport cu transmiterea riscului de cancer între generații este o sarcină dificilă și, prin urmare, acest subiect rămâne sub studiat. Cu toate acestea, această problemă este importantă pentru generațiile viitoare, deoarece creșterea globală a obezității are ca rezultat mai multe sarcini și nașteri în rândul mamelor supraponderale și obeze. Dovezile actuale indică faptul că, cu excepția adipozității copiilor și adolescenților, reducând riscul de cancer mamar, obezitatea crește în general riscul de cancer. Deoarece studiile umane pe termen lung sunt atât de provocatoare, studiile viitoare care fac legătura între modelele animale și oamenii ne vor accelera înțelegerea acestor conexiuni. Prioritățile pentru studiu includ o mai bună înțelegere a momentului adipozității în raport cu concepția și riscul de cancer; mecanismele prin care adipozitatea copilariei, viteza de creștere și densitatea sânului afectează riscul de cancer mamar; și mecanismele care stau la baza conexiunilor dintre greutatea la naștere și cancerul de sân.
- Șobolanii grași arată de ce cancerul mamar poate fi mai agresiv la pacienții cu obezitate - ScienceDaily
- Modele dietetice și riscul apariției adenoamelor colorectale cancerul studiului sănătății femeilor negre
- Articolul complet Acizii grași omega-3 reduc riscul de cancer mamar la femeile obeze aflate în postmenopauză
- Efectul obezității și al diabetului de tip 2 asupra răspunsului anabolic al proteinelor la insulină la femeile în vârstă -
- Efectele obezității și distribuției grăsimilor asupra funcției ventilatorii studiul privind îmbătrânirea normativă - PubMed