Sumida Y 1 *, Yoneda M 1, Tokushige K 2, Kawanaka M 3, Fujii H 4, Yoneda M 5, Imajo K 5, Takahashi H 6, Ono M 7, Nozaki Y 8, Hyogo H 9, Koseki M 10, Yoshida Y 11, Kawaguchi T 12, Kamada Y 13, Eguchi Y 14, Okanoue T 15, Nakajima A 5; Grupul de studiu japonez al NAFLD (JSG-NAFLD) 16
1 Divizia de Hepatologie și Pancreatologie, Departamentul de Medicină Internă, Universitatea de Medicină Aichi, Japonia
2 Departamentul de Medicină Internă, Institutul de Gastroenterologie, Tokyo Women’s Medical University, Tokyo, Japonia
3 Departamentul de Medicină Internă Generală2, Școala de Medicină Kawasaki, Okayama 700-8505, Japonia
4 Departamentul de Hepatologie, Școala de Medicină, Universitatea din Osaka, Osaka, Japonia
5 Divizia de Gastroenterologie și Hepatologie, Școala de Medicină a Universității din Yokohama City, Yokohama, Japonia
6 Departamentul de Metabolism și Endocrinologie, Facultatea de Medicină, Universitatea Saga, Saga, Japonia
7 Division of Gastroenterology and Hepatology, Department of Internal Medicine, Tokyo Women’s Medical University Medical Center East, Tokyo, Japan
8 Departamentul de Gastroenterologie, Centrul Național pentru Sănătate și Medicină Globală, Tokyo, Japonia
9 Departamentul de Gastroenterologie, Spitalul General JA Hiroshima, Japonia
10 Departamentul de Medicină Cardiovasculară, Departamentul de Medicină, Școala de Medicină a Universității din Osaka
11 Departamentul de Gastroenterologie și Hepatologie, Spitalul Municipal Suita, Osaka, Japonia
12 Divizia de Gastroenterologie, Departamentul de Medicină, Școala de Medicină a Universității Kurume, Kurume, Japonia
13 Departamentul de Biochimie Moleculară și Investigații Clinice, Universitatea din Osaka Școala de Medicină, Suite, Osaka, Japonia
14 Liver Center, Spitalul Universitar Saga, Saga, Japonia
15 Centrul de Hepatologie, Spitalul Saiseikai Suita, Osaka, Japonia
16 Centrul de cercetare în domeniul administrării medicale strategice din Japonia, Nagoya, Aichi, Japonia
Autorul corespunzator: Yoshio Sumida
Abordare: Divizia de Hepatologie și Pancreatologie, Departamentul de Medicină Internă, Universitatea de Medicină Aichi, Nagakute, Aichi 480-1195, Japonia; Tel: + 81-561-62-3311; Fax: + 81-561-62-1508; E-mail: [email protected]
Data primiriiStk #: 04 februarie 2020; Data acceptatăStk #: 26 februarie 2020; Data publicării: 05 martie 2020
Citare: Sumida Y, Yoneda M, Tokushige K, Kawanaka M, Fujii H, Yoneda M, Imajo K, Takahashi H, Ono M, Nozaki Y, Hyogo H, Koseki M, Yoshida Y, Kawaguchi T, Kamada Y, Eguchi Y, Okanoue T, Nakajima A; Grupul de studiu japonez al NAFLD (JSG-NAFLD). Efectul hepatoprotector al inhibitorului SGLT2 asupra bolilor hepatice grase nealcoolice. Acces deschis Diab Res. 2020 05 mar; 2 (S1): 17-25.
Cuvinte cheie: Boală hepatică grasă nealcoolică; Cotransporter de sodiu-glucoză 2; Glucagon ca Peptida-1; Fibroza hepatică; Hepatocarcinogeneza
Introducere
Boala hepatică grasă nealcoolică (NAFLD) include 10-20% din steatohepatita nealcoolică (NASH), care prezintă un risc ridicat de a muri din cauza bolii hepatice. Deși nu există o farmacoterapie stabilită pentru NASH, există o mare așteptare pentru medicamentele diabetice noi care au un efect de scădere în greutate. În special, se așteaptă ca inhibitorii SGLT2 să aibă efecte multiple, cum ar fi pierderea în greutate, reducerea grăsimii viscerale și reducerea tensiunii arteriale, în plus față de efectele de scădere a glicemiei, iar studiile clinice la scară largă au demonstrat efectele protectoare asupra organelor precum inima și rinichii. (Rezultatul EMPA-REG, studiu CVD-REAL, program CANVAS, studiu CREDENCE [1], proces DECLARE, studiu DAPA-HF [2]). În ultimii ani, s-a raportat că inhibitorii SGLT2 îmbunătățesc steatoza hepatică și nivelul ALT, iar efectele hepatoprotectoare ale inhibitorilor SGLT2 au atras atenția.
Diabet și boli hepatice
Conform studiului cauzei decesului la pacienții diabetici la nivel național (2001-1010, n = 45.708), 9,3% au murit din cauza bolilor hepatice (6,0% cancer hepatic, 3,3% ciroză), clasându-se pe locul trei după boli de inimă și pneumonie Met. Potrivit grupului de cercetare NASH al Ministerului Sănătății, Muncii și Bunăstării, în rândul diabeticilor, riscul de deces cauzat de carcinomul hepatocelular a fost cel mai mare dintre tumorile maligne [3]. Când FibroScan a fost efectuat la 1.918 pacienți diabetici din Hong Kong, steatoza hepatică a fost detectată la 73%, iar fibroza hepatică avansată (≥9,6 kPa) a fost detectată la 18%. În mod similar, studiul de la Rotterdam din Olanda a constatat o rigiditate hepatică crescută la una din șase persoane cu diabet. Pe de altă parte, în studiul a 1.365 de cazuri de NAFLD diagnosticate prin biopsie hepatică ale Grupului de studiu japonez al NAFLD (JSG-NAFLD), prezența diabetului a fost un factor de risc pentru fibroza avansată a NASH [4]. În studiul JSG-NAFLD, un indice HOMA-IR ridicat, un indicator al rezistenței la insulină, a fost un factor de risc independent pentru fibroza avansată la pacienții non-diabetici [5]. Astfel, se sugerează că diabetul și rezistența la insulină nu numai că provoacă NAFLD, ci și promovează progresia fibrozei hepatice.
Starea actuală a tratamentului pentru diabetul cu NASH/NAFLD
Eficacitatea inhibitorului SGLT2 pentru disfuncția hepatică asociată cu diabetul de tip 2
Pentru a investiga efectele inhibitorilor SGLT2 asupra funcției hepatice la pacienții japonezi cu diabet zaharat de tip 2, a fost efectuată o subanaliză a canagliflozinei într-un studiu clinic japonez [8]. Într-o sub-analiză a studiului de fază 2, nivelurile de ALT au fost semnificativ mai mici în grupul tratat cu canagliflozin de 12 săptămâni (n = 47) decât în placebo (n = 59) la pacienții cu ALT anormală. Într-o sub-analiză a studiului de fază 3, canagliflozin la 52 de săptămâni a redus nivelul ALT în 89% din cazurile ALT anormale (n = 195), cu o reducere medie de 16 UI/L. Scăderea ALT a fost invers corelată cu Valoarea ALT înainte de tratament și s-au obținut efecte mai bune la pacienții cu ALT anormală. În mod similar, o sub-analiză a unui studiu de fază 2 a canagliflozinei din Canada a raportat că enzimele hepatobiliare s-au îmbunătățit față de placebo și inhibitorii DPP-4 și că îmbunătățirea ALT a fost corelată cu HbA1c și îmbunătățirea greutății corporale. Conform studiului clinic de fază 3 cu luseogliflozină, grupul tratat cu luseogliflozină (n = 79) a îmbunătățit semnificativ AST, ALT și GGT comparativ cu placebo [9]. Aceste rezultate au sugerat că efectul hepatoprotector al inhibitorilor SGLT2 la pacienții cu diabet zaharat de tip 2.
Utilitatea inhibitorului SGLT2 pentru diabet cu NASH/NAFLD
Prin urmare, se așteaptă ca inhibitorii SGLT2 să fie eficienți pentru NAFLD/NASH. Am efectuat o analiză comparativă retrospectivă a 24 NAFLD tratați cu inhibitori SGLT2 timp de 24 de săptămâni și 21 NAFLD tratați cu inhibitori DPP-4 timp de 24 săptămâni și am constatat că inhibitorii SGLT2 au avut efecte asupra pierderii în greutate, nivelului ALT și reducerii grăsimii corporale. Conform examinării histologice a ficatului de către Akuta și colab., Toate cazurile (n = 9) au arătat o ameliorare a steatozei, iar trei cazuri au prezentat o ameliorare a fibrozei hepatice [10]. Două studii controlate randomizate (ECA) au fost recent raportate din Japonia. O comparație a 32 de cazuri de diabet cu NAFLD împărțită în grupul MTF și grupul luseogliflozin a arătat că luseogliflozina la 6 luni a arătat o greutate corporală mai mare, HbA1c, zona de grăsime viscerală și steatoza hepatică a fost semnificativ îmbunătățită [11]. În plus, în ECA deschisă de ipragliflozin 50 mg și PIO 15-30 mg, administrarea de ipragliflozin timp de 24 de săptămâni a îmbunătățit grăsimea hepatică și funcția hepatică similar cu PIO, dar a redus semnificativ greutatea corporală și grăsimea corporală în comparație cu PIO [12]. Așa cum s-a descris mai sus, inhibitorii SGLT2 pot fi superiori altor medicamente pentru diabet în tratamentul NAFLD/NASH. Un studiu clinic de fază 3 cu dapagliflozin (studiu DEAN) este în curs de desfășurare.
Mecanismul de acțiune al inhibitorului SGLT2 și îmbunătățirea ficatului gras
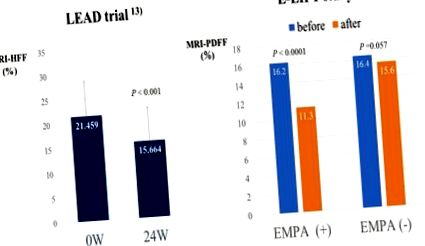
Fig-1: Efectul inhibitorilor SGLT2 asupra conținutului de grăsime hepatică evaluat prin rezonanță magnetică: două studii prospective
Studiu LEAD : Lusepgliflozin 2,5 mg/zi pentru 24 de săptămâni a redus semnificativ conținutul de grăsime hepatică evaluat de RMN-HFF (fracțiune de grăsime hepatică) la 39 de pacienți NAFLD cu diabet de tip 2.
E-LIFT patients Pacienții cu NAFLD (n = 22) au redus semnificativ conținutul de grăsime hepatică prin RMN-PDFF (fracțiune de grăsime cu densitate de protoni) comparativ cu cei fără tratament cu inhibitori SGLT2.
Fig-2: Mecanisme de acțiune plauzibile ale inhibitorului SGLT2 în hepatoprotecție
Care sunt cele mai bune indicații pentru inhibitorii SGLT2? (Tabelul 1)
Tabelul 1: Indicații ale inhibitorilor SGLT2 pentru NAFLD/NASH
Provocările inhibitorilor SGLT2 în tratamentul NASH
Cea mai mare preocupare cu administrarea inhibitorului SGLT2 sunt efectele secundare. În plus față de polakiurie, deshidratare și infecții ale tractului urinar, există raportări grave de cetoacidoză diabetică și amputare a membrelor inferioare. În cazul nostru, cazurile NAFLD/NASH sunt obeze și există multe cazuri de diabet timpuriu înainte de introducerea agentului SU sau a insulinei și nu apar efecte secundare grave, deoarece secreția de insulină este relativ menținută. Cu toate acestea, infecțiile genitale și ale tractului urinar, cum ar fi pruritul genital și cistita, apar frecvent și folosesc adesea unguente antifungice și antibiotice orale. În plus, ca contramăsură împotriva inhibitorului SGLT2 cazuri ineficiente și cazuri cu apetit crescut, utilizați cu MTF, agonist al receptorului GLP-1 etc. ar trebui luat în considerare. În Europa și Statele Unite, este raportat că este eficient pentru pacienții non-obezi și pacienții fără diabet, dar este necesar să se ia în considerare beneficiile pe baza beneficiilor economice medicale.
Inhibitor SGLT2 și efect de suprimare a cancerului
Perspectiva viitoare a inhibitorilor SGLT
Inhibitori dual SGLT1/2, cum ar fi sotagliflozin (LX4211, Lexicon) și licogliflozin (Novartis) sunt acum în curs de dezvoltare. Sotagliflozin a fost stabilit pentru a fi eficient la pacienții T1DM necontrolați cu insulină. Deși studiile de fază 3 și 2 sunt în curs de desfășurare pentru tratamentul pacienților cu diabet de tip 2 și respectiv cu insuficiență cardiacă, studiile NASH nu au fost niciodată luate în considerare. Licogliflozina este un compus oral, o dată pe zi, cu inhibitor dual SGLT1/2. Studiul de fază 2a la 110 pacienți obezi cu NASH stadiul 1-3 a fost finalizat (NCT03205150). Rezultatul primar se modifică față de valoarea inițială în ALT în săptămâna 12. Pacienții înscriși au fost împărțiți în mod aleatoriu în trei grupuri, inclusiv licogliflozină 30 mg/zi (n = 44), licoglifolzină 150 mg/zi (n = 44) și placebo (n = 22) (NCT03205150 ) (Fig-3). În cadrul Liver Meeting 2019 ®, Harrison și colegii săi au demonstrat o îmbunătățire dependentă de doză a enzimelor hepatice și a PDFF asociate cu pierderea în greutate. Cu toate acestea, 76,5% dintre pacienții din grupul cu doze mai mari au prezentat diaree vs.
- Rezistența la insulină poate prezice boli hepatice grase nealcoolice în psoriazis, artrită psoriazică
- Formularea pe bază de plante MIT ameliorează boala hepatică grasă nealcoolică indusă de dietă bogată în grăsimi -
- Expunerea intermitentă la rece ameliorează boala ficatului gras SFEBES2019 Society for Endocrinology BES
- Cum 6 exerciții de antrenament de rezistență luptă împotriva bolilor hepatice grase 1MD
- Ciroza hepatică Dietă Alimente pentru a mânca și a evita bolile hepatice grase