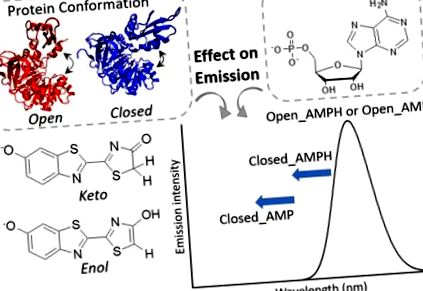
Reprezentarea formelor chimice de oxiluciferină, a conformațiilor proteice și a stărilor de protonație AMP luate în considerare în acest studiu.
Reprezentarea grafică a celor două tipare de legături de hidrogen găsite de-a lungul simulărilor (keto-4G36-AMPH ca caz reprezentativ) între fragmentul fenolat (O1) cu (a) molecule de apă (model 1) sau (b) ARG377 și model de molecule de apă 2). (c) Spectre de emisie simulate pentru două simulări MD: simularea MD A a keto-4G36-AMPH (linia roșie) este caracterizată prin modelul 1 al legăturii de hidrogen și simularea MD B a keto-4G36-AMPH (linia neagră) este caracterizată prin hidrogen - modelul de legătură 2.
Reprezentarea grafică a modelelor legăturilor de hidrogen găsite de-a lungul simulărilor de (a) keto-4G36-AMPH și (b) keto-4G37-AMPH. (c) Histogramă care arată numărul de molecule de apă în cadrul a 3 angstromi de O2 în timpul simulării. (d) Spectre de emisie simulate pentru keto-4G36-AMPH și keto-4G37-AMPH.
Reprezentarea grafică a modelelor legăturilor de hidrogen găsite de-a lungul simulărilor (a) keto-4G36-AMP și (b) keto-4G37-AMP. (c) Spectre de emisie simulate pentru keto-4G36-AMP și keto-4G37-AMP.
Reprezentarea grafică a modelelor legăturilor de hidrogen găsite de-a lungul simulărilor de (a) enol-4G36-AMPH care implică GLY341 și AMPH - (model 1), (b) enol-4G36-AMPH care implică doar AMPH - (model 2) și (c )) enol-4G37-AMPH (modelul 2). (d) Spectre de emisie simulate pentru enol-4G36-AMPH (roșu) și enol-4G37-AMPH (negru).
Reprezentarea grafică a modelelor legăturilor de hidrogen găsite de-a lungul simulărilor de (a) enol-4G36-AMP și (b) enol-4G37-AMP. (c) Histogramă care arată numărul de molecule de apă în cadrul a 3 angstromi de O2 în timpul simulării. (d) Spectre de emisie simulate pentru enol-4G36-AMP și enol-4G37-AMP.
Spectre de emisie simulate, a căror intensitate a fost normalizată având în vedere spectrul cel mai intens (enol-4G37-AMP) ca valoare de referință a 1, schimbând conformația proteinelor și starea de protonație a AMP pentru (a) fenolat-ceto și (b) fenolat- forme chimice enol ale oxiluciferinei.
Reprezentarea schematică a reacției bioluminescente a licuricii care prezintă prima (1) și a doua (2) reacții catalitice.
Abstract
Reprezentarea formelor chimice de oxiluciferină, a conformațiilor proteice și a stărilor de protonație AMP luate în considerare în acest studiu.
Reprezentarea grafică a celor două tipare de legături de hidrogen găsite de-a lungul simulărilor (keto-4G36-AMPH ca caz reprezentativ) între fragmentul fenolat (O1) cu (a) molecule de apă (model 1) sau (b) ARG377 și model de molecule de apă 2). (c) Spectre de emisie simulate pentru două simulări MD: simularea MD A a keto-4G36-AMPH (linia roșie) este caracterizată prin modelul 1 al legăturii de hidrogen și simularea MD B a keto-4G36-AMPH (linia neagră) este caracterizată prin hidrogen - modelul de legătură 2.
Reprezentarea grafică a modelelor legăturilor de hidrogen găsite de-a lungul simulărilor de (a) keto-4G36-AMPH și (b) keto-4G37-AMPH. (c) Histogramă care arată numărul de molecule de apă în cadrul a 3 angstromi de O2 în timpul simulării. (d) Spectre de emisie simulate pentru keto-4G36-AMPH și keto-4G37-AMPH.
Reprezentarea grafică a modelelor legăturilor de hidrogen găsite de-a lungul simulărilor (a) keto-4G36-AMP și (b) keto-4G37-AMP. (c) Spectre de emisie simulate pentru keto-4G36-AMP și keto-4G37-AMP.
Reprezentarea grafică a modelelor legăturilor de hidrogen găsite de-a lungul simulărilor de (a) enol-4G36-AMPH care implică GLY341 și AMPH - (model 1), (b) enol-4G36-AMPH care implică doar AMPH - (model 2) și (c )) enol-4G37-AMPH (modelul 2). (d) Spectre de emisie simulate pentru enol-4G36-AMPH (roșu) și enol-4G37-AMPH (negru).
Reprezentarea grafică a modelelor legăturilor de hidrogen găsite de-a lungul simulărilor de (a) enol-4G36-AMP și (b) enol-4G37-AMP. (c) Histogramă care arată numărul de molecule de apă în cadrul a 3 angstromi de O2 în timpul simulării. (d) Spectre de emisie simulate pentru enol-4G36-AMP și enol-4G37-AMP.
Spectre de emisie simulate, a căror intensitate a fost normalizată având în vedere spectrul cel mai intens (enol-4G37-AMP) ca valoare de referință a 1, schimbând conformația proteinelor și starea de protonație a AMP pentru (a) fenolat-ceto și (b) fenolat- forme chimice enol ale oxiluciferinei.
Reprezentarea schematică a reacției bioluminescente a licuricii care prezintă prima (1) și a doua (2) reacții catalitice.
- Comparație fără text integral a conținutului de zinc, cupru și seleniu în materie brută, afumată și murată
- Tratament full-text fără molecule cu inhibitor de kinază 12 asemănător Ste-20 de mamifere (MST12) XMU-MP-1
- Investigații numerice fără text complet, cu molecule, ale sintezei ultra-scurte laser-ablative a metalului
- Stare termică, grosime și compoziție a textului complet cu minerale fără text Minerals, mantaua litosferică
- Stiinte medicale Stare imuna gratuita cu text integral al pacientilor cu cancer pancreatic care primesc criochirurgie