Lone V. Nielsen
1 Departamentul de Nutriție, Exerciții și Sport, Facultatea de Științe, Universitatea din Copenhaga, Danemarca
Mette S. Nielsen
1 Departamentul de Nutriție, Exerciții și Sport, Facultatea de Științe, Universitatea din Copenhaga, Danemarca
Julie B. Schmidt
1 Departamentul de Nutriție, Exerciții și Sport, Facultatea de Științe, Universitatea din Copenhaga, Danemarca
Sue D. Pedersen
1 Departamentul de Nutriție, Exerciții și Sport, Facultatea de Științe, Universitatea din Copenhaga, Danemarca
2 Clinica de endocrinologie C-ENDO, Calgary, AB, Canada
Anders Sjödin
1 Departamentul de Nutriție, Exerciții și Sport, Facultatea de Științe, Universitatea din Copenhaga, Danemarca
Abstract
O pierdere în greutate preoperatorie de 8% este o condiție prealabilă pentru a fi supus unei intervenții chirurgicale bariatrice (BS) în Danemarca. Scopul prezentului studiu a fost de a evalua eficacitatea unei diete cu consum redus de energie (LCD) de 7 sau 11 săptămâni pentru atingerea greutății țintă preoperatorii înainte de BS. Un total de treizeci de pacienți obezi (IMC 46 · 0 (sd 4 · 4) kg/m 2) au urmat un LCD (Cambridge Weight Plan ®, 4184 kJ/d (1000 kcal/d)) timp de 7 sau 11 săptămâni ca pregătire pentru BS. Măsurătorile antropometrice, inclusiv compoziția corpului (absorptiometria cu raze X cu energie dublă), parametrii sanguini și tensiunea arterială au fost evaluate în săptămânile 0, 7 și 11. În săptămâna 7, majoritatea pacienților (77%) și-au atins greutatea țintă, iar acest lucru a fost atinsă după 5 · 4 (sem 0 · 3) săptămâni. Pierderea medie în greutate a fost de 9,3 (sem 0 · 5)% (P sem 2 · 3) și, respectiv, de 7 · 3 (sem 1 · 8) mmHg, respectiv, toate scăderea P sem 1 · 8)% a glucozei în post (P sem 6 · 4)% scăderea insulinei de post (P sem 2 · 2)% scăderea LDL (P sem 4 · 7)% scăderea TAG (P Cuvinte cheie: Dietele cu consum redus de energie, Dietele cu formule lichide, Pierderea în greutate preoperatorie, Chirurgia bariatrică
Singurul tratament eficient pe termen lung dovedit în prezent pentru a depăși obezitatea severă este chirurgia bariatrică (BS) (, 1). Studiile au arătat că complexitatea procedurii chirurgicale și riscul de complicații perioperatorii și postoperatorii sunt asociate cu gradul de obezitate (, 2, 3) .
Beneficiile pierderii în greutate preoperatorie includ o reducere a riscului de complicații perioperatorii prin reducerea țesutului adipos visceral și a conținutului de grăsime intrahepatică, reducând astfel riscul de a face conversia în operație deschisă (, 2, 4 - 6), scurtarea timpului de operare (, 7 - 10), precum și durata spitalizării (, 10, 11). În plus, o pierdere în greutate preoperatorie poate fi chiar asociată cu o scădere în greutate postoperatorie îmbunătățită (, 7, 10, 11), potențial prin reflectarea motivației pacienților, dar și prin obișnuirea pacienților cu un stil de viață de restricție alimentară după operație. Prin urmare, pentru a optimiza siguranța și eficacitatea BS la pacienții cu obezitate severă, este preferabilă pierderea în greutate preoperatorie.
Majoritatea chirurgilor recomandă pacienților să piardă în greutate înainte de BS. Ministerul danez al Sănătății solicită o scădere în greutate de 8% pentru pacienții programați pentru BS (, 12); cu toate acestea, în prezent nu există un program de dietă standard prescris pentru a obține greutatea țintă preoperatorie. O scădere în greutate obținută prin dieta convențională și modificările stilului de viață poate fi foarte dificil de obținut pentru unii pacienți, mai ales într-un timp prestabilit. În astfel de cazuri, o dietă cu formulă cu consum redus de energie (LCD) cu conținut ridicat de proteine poate fi o opțiune eficientă. Aceste formule limitează de obicei aportul de energie la 3347–6276 kJ/zi (800–1500 kcal/zi), dar conțin toți nutrienții esențiali. Formulele cu conținut scăzut de energie, cu conținut ridicat de proteine, sunt capabile să inducă pierderea rapidă în greutate, de multe ori asigură o sațietate relativ adecvată după câteva zile și încearcă să minimizeze pierderea de masă fără grăsimi (FFM) (, 13, 14). Întrucât peste 300.000 de proceduri BS sunt efectuate anual în întreaga lume (, 15), acest lucru intensifică necesitatea cercetării cu accent pe îmbunătățirea strategiilor preoperatorii de slăbire.
În acest studiu am urmărit să determinăm eficacitatea unui LCD pentru a obține o pierdere în greutate de 8% la pacienții cu obezitate severă înainte de BS. În al doilea rând, au fost evaluate potențialele beneficii pentru sănătate și efectele secundare ale LCD.
Metode
Acest studiu a făcut parte dintr-un studiu mai amplu; o descriere detaliată a metodelor a fost recent publicată în altă parte (, 16) .
Populația de studiu
Un total de treizeci de caucazieni, cu vârste cuprinse între 18 și 65 de ani, cu IMC ≥ 40 sau IMC ≥ 35 kg/m 2 combinat cu apnee de somn obstructivă sau hipertensiune aprobată pentru by-passul gastric Roux-en-Y au fost recrutați din noiembrie 2009 până în august 2011. Excludere criteriile au fost fie legate de obiectivele finale din studiul principal și au inclus diabet zaharat, disfuncție tiroidiană, etiologie hipotalamică sau genetică a obezității (, 16), fie contraindicații legate de utilizarea LCD: caz anterior de diverticulită, istoric trecut de aritmii ventriculare, disfuncție renală (clearance-ul creatininei 3 × limita normală superioară), alergie la proteine din lapte sau intoleranță la lactoză, porfirie sau fenilcetonurie, antecedente de gută, alăptare, utilizare concomitentă de inhibitori de monoaminooxidază sau diuretice care nu economisesc potasiu sau incapacitate sau lipsă de dorință cu ecranul LCD.
Acest studiu a fost realizat în conformitate cu liniile directoare stabilite în Declarația de la Helsinki și toate procedurile care implică subiecți umani au fost aprobate de Comitetul etic municipal din Copenhaga/Comitetul de etică științifică din regiunile metropolitane din Danemarca (jurnal nr. H-2-2009- 091), Agenția Daneză pentru Protecția Datelor (jurnal nr. 2007-54-0296) și a fost înregistrată la clinictrials.gov (ID ClinicalTrials.gov> NCT00939679). Consimțământul informat scris a fost obținut de la toți subiecții.
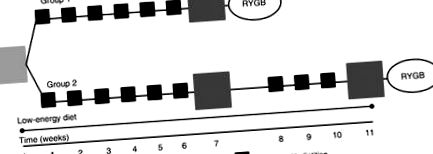
Studiul a inclus o vizită de bază (săptămâna 0) și două vizite de urmărire la săptămânile 7 și 11. Pentru a investiga efectele asupra obiectivului primar al studiului principal (cheltuieli de energie) (, 16), subiecții au fost randomizați la una dintre două grupuri: grupul 1 programat pentru operația de by-pass gastric Roux-en-Y în săptămâna 8 (n 15), sau grupul 2 programat pentru operația de by-pass gastric Roux-en-Y în săptămâna 12 (n 15). Toți participanții au primit un LCD timp de 11 săptămâni. În lucrarea de față vor fi examinate numai perioadele pre-chirurgicale: adică perioada de la săptămâna 0 la 7 (inclusiv ambele grupuri 1 și 2, n 30) și perioada de la săptămâna 7 la 11 (numai grupa 2, n 15) (Fig. 1). Subiecții au primit săptămânal consiliere nutrițională de la un dietetician.
Prezentare generală a proiectului studiului. Deoarece proiectarea studiului principal a fost un studiu controlat, participanții au fost randomizați la operația de by-pass gastric Roux-en-Y (RYGB) în săptămâna 8 (grupul 1) sau săptămâna 12 (grupul 2). Participanții au urmat o dietă cu formulă cu conținut scăzut de energie din săptămâna 0 până în săptămâna 11.
Screening
Pacienții eligibili pentru studiu au fost identificați de endocrinologi la Spitalul Hvidovre, Copenhaga, Danemarca și au făcut referire la o vizită de screening la Departamentul de Nutriție, Exerciții și Sport, Universitatea din Copenhaga, unde au fost explicate detaliile protocolului și a fost programată o vizită de bază pentru subiecții eligibili.
Linia de bază (săptămâna 0) și vizitele de urmărire (săptămânile 7 și 11)
La vizita inițială au fost obținute date demografice și istoricul medical, iar pacienții au fost randomizați la intervenție chirurgicală fie la săptămâna 8, fie la 12. Au fost colectate date antropometrice, a fost prelevată o probă de sânge în repaus alimentar, iar ritmul cardiac și tensiunea arterială au fost măsurate cu poziția în decubit dorsal. LCD-ul a fost inițiat cu prima lor vizită la dietetician.
Vizita de bază și cele două vizite de urmărire au fost identice.
Dieta cu consum redus de energie
Ecranul LCD a constat din patru mese pe bază de pulbere (Cambridge Weight Plan ®), 1 litru de lapte degresat, 295 g de legume și 100 g iaurt cu conținut scăzut de grăsimi pe zi, oferind 4310 kJ/zi (1030 kcal/zi) (48% energie E %) din carbohidrați, 39 E% din proteine, 13 E% din grăsimi și ≥100% doza zilnică recomandată pentru toate vitaminele și mineralele). Efectele secundare autoevaluate și respectarea LCD au fost înregistrate la întâlnirea săptămânală cu dieteticianul. Conformitatea a fost evaluată pe o scară de la 1 la 5, 5 indicând „o conformitate foarte bună”.
Măsurători antropometrice
Subiecții au fost informați să poarte îmbrăcăminte ușoară, fără pantofi, să aibă vezica golită și să fie postite pentru evaluarea lor antropometrică. Greutatea corporală a fost măsurată la cel mai apropiat 0,1 kg. Circumferințele de talie și șold au fost măsurate de două ori până la cel mai apropiat 0,5 cm și s-a utilizat media. Înălțimea a fost măsurată la cel mai apropiat 0,5 cm folosind un stadiometru digital montat pe perete. Compoziția corpului a fost determinată prin absorptiometrie cu raze X cu energie duală (DXA). Măsurătorile DXA au fost făcute folosind scanări pe jumătate de corp (, 17). Același scaner DXA (Lunar Prodigy, versiunea software Encore 12.3) a fost utilizat pe tot parcursul studiului pentru a evita variații în analiza rezultatelor scanării. Cu toate acestea, din cauza limitărilor de greutate, trei subiecți au fost scanați într-un scaner DXA cu dimensiunea și capacitatea de greutate a mesei mai mari (Lunar iDXA, versiunea software Encore 12.3).
Măsuri biochimice
Probele de sânge au fost colectate după un post peste noapte (10-12 ore) și au fost analizate pentru glucoză, insulină, peptidă C, TAG, colesterol total, HDL, LDL și proteină C-reactivă cu sensibilitate ridicată. Pregătirea și analiza probelor de sânge au fost descrise în detaliu în altă parte (, 16). CV-urile în cadrul și între analize au fost sub 3-5%, respectiv 6,5%, pentru toate măsurile biochimice.
analize statistice
Toate analizele statistice au fost făcute în versiunea R 2.14.0 (www.r-project.org).
Rezumate descriptive ale datelor (vârstă, greutate corporală, IMC) sunt prezentate ca valori medii și abateri standard. Eficacitatea LCD-ului pentru toate punctele finale a fost modelată într-un model liniar mixt cu săptămâna ca efect fix și subiectul ca efect aleatoriu. Toate analizele s-au bazat pe intenția de a trata cu observațiile de bază reportate pentru datele lipsă (n 2), cu excepția greutății corporale în care ultima observație (măsurată la întâlnirea săptămânală cu dieteticianul) a fost reportată pentru datele lipsă. Subanalizele au fost modelate într-un model liniar mixt incluzând o interacțiune săptămânală × de grup și cu subiectul ca efect aleatoriu. Datele sunt prezentate ca valori medii cu erorile lor standard.
Valorile P corespund testelor de probabilitate și valorile P (, 16). Cu toate acestea, un calcul al mărimii eșantionului, bazat pe datele dintr-un studiu anterior, utilizând un LCD de 3347-4184 kJ (800-1000 kcal) timp de 8 săptămâni (, 18), a arătat că odată cu dimensiunea eșantionului am fost alimentați pentru a detecta o greutate de 8% pierderea la subiecții obezi (corespunzătoare unei pierderi medii în greutate de 11,1 kg, o sd de 3,3 kg și o diferență minimă relevantă de 8 kg (8% pierdere în greutate); α = 0,05, β = 0,8 ).
Rezultate
Date descriptive
În total, opt bărbați și douăzeci și două de femei au fost incluși în studiu. Vârsta medie a fost de 38,8 (sd 10,4) ani, cu o greutate corporală medie la momentul inițial de 135,1 (sd 19,2) kg și IMC de 46,0 (sd 4,4) kg/m 2. Doi subiecți au renunțat înainte de prima vizită de urmărire (săptămâna 7), din cauza problemelor personale și a incapacității de a se conforma LCD-ului.
Pierdere în greutate
Pierderea medie în greutate în săptămâna 7 a fost de 9,3 (sem 0,5), ceea ce corespunde unei pierderi în greutate de 12,7 (sem 0,8) kg (Fig. 2).
Pierderea în greutate săptămânală (%) măsurată de la săptămâna 0 la 7 (n 30; grupurile 1 și 2; ○) și de la săptămâna 0 până la 11 numai în grupa 2 (n 15; X). Grupa 1 a fost operată în săptămâna 8; grupa 2 a fost operată în săptămâna 12. Valorile sunt mijloace, cu erori standard reprezentate de bare verticale.
Dintre pacienții incluși, 77% și-au atins greutatea țintă preoperatorie, iar acest lucru a fost realizat în medie în săptămâna 5,4 (sem 0,3). Pierderea în greutate în grupul care a atins greutatea țintă înainte de săptămâna 7 (n 23) a fost de 10,2 (sem 0,3%), ceea ce corespunde unei reduceri în greutate de 14,1 (sem 0,7) kg, în timp ce pierderea medie în greutate pentru subiecții rămași în săptămâna 7 (n 7) a fost de 6 · 1 (sem 0 · 9)%, ceea ce corespunde unei reduceri de greutate de 7 · 9 (sem 1 · 2) kg. Pierderea în greutate procentuală în săptămâna 7 nu a prezis pierderea în greutate procentuală la 18 luni postoperator (r -0 · 40; P = 0 · 07).
O altă reducere a greutății corporale de 3,9% (sem 0,5%) a fost observată în săptămâna 7-11 în cei cincisprezece pacienți programați pentru BS în săptămâna 12 (P sem 0,1) din săptămâna 0-7, și a rămas neschimbată până la săptămâna 11 (4 · 1 (sem 0 · 2); P = 0 · 16). Conformitatea a fost asociată pozitiv cu pierderea în greutate procentuală din săptămâna 0 până la 7 (r 0 59; P sem 0 · 8) și respectiv 2 · 3 (sem 0 · 7)%) a fost observată în săptămâna 7 până la 11 (ambele P sem 0 · 5) c. 8,7 (cu excepția 0,7)%; P sem 1 · 0) și 3 · 5 (sem 0 · 7) kg, respectiv, Fig. 3).
FFM, masă fără grăsimi; FM, masă grasă; hs-CRP, o proteină C reactivă foarte sensibilă; TA, tensiune arterială; HR, ritm cardiac.
Valoarea medie a modificării de la săptămâna 0 la 7 a fost semnificativă: * P sem 1 · 3) bătăi/min, 7 · 1 (sem 2 · 3) și 7 · 3 (sem 1 · 8) mmHg, respectiv (toate P 140/90 mmHg) și doar unul dintre acești pacienți a fost tratat farmacologic pentru aceasta. Tensiunea arterială s-a normalizat la cinci dintre acești șase pacienți în săptămâna 7. Alți cinci pacienți au fost tratați cu medicamente antihipertensive cu tensiune arterială în intervalul normal la momentul inițial. Medicamentul a fost retras la unul dintre acești pacienți în săptămâna 7.
Efecte secundare
Cele mai frecvent raportate reacții adverse au fost cefaleea, oboseala, constipația, amețelile și infecțiile respiratorii superioare (raportate de 57, 50, 43, 33 și respectiv 30%). Alte reacții adverse mai puțin raportate au inclus intoleranță la frig, foame, dureri abdominale, iritabilitate, piele uscată, diaree, flatulență și respirație urât mirositoare. Nu au fost raportate evenimente adverse severe.
Discuţie
Deoarece consilierea nutrițională este un aspect important în tratamentul obezității (, 35, 36), o limitare a prezentului studiu este că rezultatele ar putea să nu fie direct aplicabile candidaților la BS care nu primesc consiliere nutrițională săptămânală și încurajări de la un experimentat profesionist în sănătate. În plus, excluderea pacienților diabetici și a subiecților care nu erau dispuși să respecte LCD-ul ar fi putut afecta rezultatele noastre, deoarece acest grup poate fi mai puțin predispus la pierderea în greutate (, 37). O altă limitare este DXA, care nu a fost evaluat pe deplin ca instrument de evaluare a compoziției corpului la pacienții cu obezitate severă și a fost raportat că nu furnizează date valabile în cazul pierderii dinamice în greutate din cauza ipotezelor inexacte ale unei hidratări constante a FFM .
În concluzie, rezultatele noastre sugerează că este posibil să se obțină o pierdere în greutate preoperatorie de 8% cu un LCD în termen de 7 săptămâni. Pierderea în greutate în săptămâna 7 a fost însoțită de un profil metabolic îmbunătățit și o reducere a tensiunii arteriale, fără alte îmbunătățiri după o pierdere în greutate suplimentară de 3,9% în săptămâna 11. Mecanismele din spatele reducerii excesive a FFM la subiecții cu obezitate ridicată după LCD are nevoie de investigații suplimentare, inclusiv potențialul de optimizare a formulelor LCD utilizate pentru a limita pierderea țesutului activ din punct de vedere metabolic.
Mulțumiri
Autorii îi mulțumesc lui Luise Gunvald MSc, John Gargul Lind BSc, Lene Stevner MSc, Jane Jørgensen BSc, Søren Andresen BSc, Marianne Juul BSc, Ulla Skovbæch Pedersen BSc, Departamentul de Nutriție, Exerciții și Sport, Danemarca.
Studiul a fost realizat ca parte a UNIK: Food, Fitness and Pharma for Health and Disease la Universitatea din Copenhaga. Proiectul UNIK a fost finanțat de Ministerul Danez al Științei, Tehnologiei și Inovării, numărul de subvenție 09-065308. Produsele cu consum redus de energie au fost furnizate de Cambridge Weight Plan ® (Corby, Northants, Marea Britanie). UNIK și Cambridge Weight Plan ® nu au avut niciun rol în proiectarea, analiza sau redactarea acestui articol.
Cercetare proiectată: A. S. și S. D. P.; colectarea coordonată a datelor: J. B. S., L. V. N. și M. S. N.; date analizate: L. V. N. și M. S. N.; a discutat analiza și interpretarea datelor: L. V. N., M. S. N., J. B. S., S. D. P. și A. S.; a scris lucrarea: L. V. N. și M. S. N.; a avut responsabilitatea principală pentru conținutul final: A. S.; toți autorii au analizat manuscrisul în mod critic și au aprobat manuscrisul final.
J. B. S., M. S. N. și L. V. N. au primit subvenții de călătorie de la Cambridge Weight Plan ®. Produsele cu consum redus de energie au fost furnizate de Cambridge Weight Plan ®. UNIK și Cambridge Weight Plan ® nu au avut niciun rol în proiectarea, analiza sau redactarea acestui articol.
- Dan Stevens Pierderea în greutate, dieta și fotografiile
- Efectul de a permite alegerea dietei asupra pierderii în greutate Un studiu randomizat - PubMed
- Alegeți alimente dietetice pentru slăbit, sucuri sănătoase, miere organică - ZOE
- Daniel s dieta de 10 zile - Jordan Rubin s (legume, kilograme, antrenament, sare) - Dieta și Pierdere în Greutate
- FDA aprobă un nou gel de pierdere în greutate Revizuiește pierderea medie în greutate în dieta Keto de 30 de zile