Abstract
Scopul revizuirii
Pentru a înțelege mai bine impactul obezității și al bolilor cardiovasculare asupra infecției cu gripa A.
Descoperiri recente
Această infecție ar putea avea rezultate dăunătoare la pacienții obezi cu boli cardiovasculare, cum ar fi un risc crescut, durata spitalizării, severitatea bolii, morbiditatea și mortalitatea. Cu toate acestea, ar putea exista și unele beneficii cardioprotectoare asociate cu vaccinarea antigripală, cum ar fi o mortalitate redusă, spitalizare și sindroame coronariene acute, la pacienții cu boli coronariene și/sau insuficiență cardiacă.
rezumat
Obezitatea are un impact negativ asupra funcției imune și apărării gazdei. Studii recente arată că obezitatea este un factor de risc independent pentru creșterea morbidității și mortalității după infecție. Pacienții obezi ar putea avea nevoie de considerații speciale în tratament; cu toate acestea, nu există suficiente dovezi pentru a înțelege pe deplin mecanismele din spatele imunocompetenței reduse atunci când apare infecția cu gripa A. Studiile viitoare ar trebui să se concentreze pe tratamente speciale, atunci când pacienții nu au fost vaccinați și au boli cardiovasculare.
Introducere
Această revizuire se concentrează asupra modului în care obezitatea și bolile cardiovasculare influențează răspunsul gripal. Studiile retrospective demonstrează că în timpul pandemiei H1N1 din 2009, obezitatea a fost identificată ca un factor de risc pentru spitalizare, ventilație mecanică și mortalitate la infecție. Aceste date trebuie evidențiate, deoarece se preconizează că aproape 50% din populația mondială va fi obeză până în 2050. Mai multe studii de caz au identificat posibilele efecte ale obezității asupra replicării virale în plămânul profund, progresia spre pneumonie virală și vărsarea virală prelungită [1]. Prin urmare, gestionarea infecției gripale la această populație cu risc trebuie să aibă o atenție specială, având în vedere că este posibil să nu răspundă optim la vaccinare [2].
Obezitatea și impactul acesteia asupra infecției gripale
Acumularea excesivă de grăsimi care duce la obezitate afectează sănătatea adulților [3]. Starea sa cronică indusă de inflamație cronică are un impact negativ asupra funcției imune și apărării gazdei [2], după cum se arată în timpul pandemiei H1N1 a virusului gripal A din 2009, în care obezitatea a fost un factor de risc independent pentru boli severe, spitalizare, ventilație mecanică mortalitate la infecție [1].
Este bine cunoscut faptul că infecția cu virusul gripal A se caracterizează prin febră, mialgie, rinoree, dureri în gât și strănut. Aceste simptome au un maxim de 3-5 zile după infecție, cu vărsarea virală maximă în zilele 2-3. De obicei, este limitat la căile respiratorii superioare; cu toate acestea, în cazuri severe, tractul respirator inferior, inclusiv plămânii, poate fi afectat și necesită adesea spitalizare. Această progresie este mai frecventă la pacienții obezi, ducând la diminuarea rezoluției infecției în comparație cu pacienții non-obezi [1]. Obezitatea joacă, de asemenea, un rol în rezultatul complicațiilor critice ale infecției cu gripa A/pdmH1N1 și este asociată cu o ventilație mecanică mai lungă pentru sindromul de detresă respiratorie acută severă și șoc [4].
Un indice mai mare de masă corporală (IMC) și sindromul metabolic la pacienții cu gripă au arătat un risc crescut și durata de spitalizare [4,5,6], creșterea severității bolii, morbidității și mortalității în timpul infecțiilor tractului respirator inferior. Acest lucru s-ar putea explica parțial prin permeabilitatea pulmonară crescută în timpul infecției, constatată în studiile la șoareci. Șoarecii obezi au o scurgere crescută de proteine din plămâni în lichidul de lavaj bronhoalveolar în comparație cu șoarecii slabi. În plus, edemul pulmonar și stresul oxidativ sunt, de asemenea, crescute, ceea ce subliniază etiologiile multiple ale patologiei pulmonare crescute la gazda obeză și afectarea reparării plăgilor [1, 4].
Starea obezogenă poate afecta, de asemenea, evoluția virusului gripal A. Este bine cunoscut faptul că indivizii obezi sunt subnutriți în afară de excesul lor de grăsime; ar putea prezenta, de asemenea, deficiențe de nutrienți, cum ar fi vitaminele [7], mineralele și oligoelementele [8]. Există o varietate de mecanisme prin care dezechilibrele nutriționale ar putea modifica evoluția virală din interiorul gazdei [8]. Studiile au arătat că astfel de dezechilibre prelungesc infecțiile, întârzie eliminarea și cresc vărsarea (cu 42% mai mult decât ne-obezii) [9], toate acestea putând crește transmisia virală [1].
În plus față de scăderea mecanismelor de imunocompetență, alți factori potențiali ar putea contribui la susceptibilitatea crescută a acesteia la infecții în spital. Unele exemple, care sunt boli subiacente care afectează mobilitatea, pot crește, de asemenea, riscul apariției problemelor pielii, vizitelor prelungite la spitale și infecțiilor nosocomiale, modificarea farmacocineticii unor medicamente și o susceptibilitate crescută la infecțiile postoperatorii [2]. Astfel, este o problemă complexă care necesită dovezi suplimentare pentru a dezvolta tratamente mai bune pentru această populație în creștere.
Importanța vaccinării împotriva gripei
Obezitatea provoacă o stare cronică de inflamație într-un mod generalizat și constant, cu efecte negative asupra imunității. Persoanele obeze au întârziat răspunsurile imune la infecția cu virusul gripal și au o recuperare mai lentă după boală. În plus, eficacitatea tratamentului și a vaccinului este redusă la această populație provocând o alterare a ciclului de viață viral și, împreună cu un răspuns imun deja slăbit și întârziat, ducând la o afecțiune mai gravă. Răspunsurile inițiale și adaptative slabe la infecție și vaccinare creează o capacitate afectată de a răspunde corespunzător la infecție. Eficacitatea vaccinului poate scădea la oamenii obezi; cu toate acestea, sunt necesare mai multe studii pentru a înțelege mai bine modul în care starea obeză afectează controlul infecției [1].
Studiile anterioare sugerează că severitatea infecției cu virus gripal este multifactorială și poate fi legată de răspândirea și repararea plămânilor, formarea de concentrate extracelulare de neutrofile la nivel pulmonar; cu toate acestea, acest mecanism la indivizi este necunoscut [10].
Eficacitatea vaccinului la grupurile umane a arătat că ratele inițiale de seroconversie sunt ridicate în populația obeză, dar că în timp există o scădere mai mare a eficacității decât cea observată la populațiile neobeze [11]. Vaccinul antigripal ca metodă de prevenire este formulat în fiecare an, conținând în mod obișnuit atât gripa A, cât și B. Un studiu realizat în 2013-2015 a avut ca scop evaluarea dacă obezitatea a fost asociată cu un risc crescut de gripă pentru gripă și boli asemănătoare gripei în rândul obezilor vaccinați și adulții non-obezi, constatând că, printre obezi, 9,8% au confirmat gripa sau boala asemănătoare gripei, comparativ cu 5,1% dintre participanții la greutate sănătoasă. În comparație cu greutatea sănătoasă vaccinată, participanții obezi au avut dublu riscul de a dezvolta gripa sau boala asemănătoare gripei (risc relativ = 2,01, IÎ 95% 1,12, 3,60, p = 0,020); prin urmare, în acest grup de risc, în același mod, vaccinarea este foarte importantă [12]. Deși se pare că în grupurile cu risc crescut, cum ar fi populația obeză și supraponderală, vaccinarea poate să nu ofere o protecție optimă și, din cauza tendinței în creștere a obezității la nivel mondial, eficacitatea vaccinului ar trebui îmbunătățită [10].
La pacienții cu boli cardiovasculare, există dovezi convingătoare care arată un risc mai mic de evenimente cardiovasculare adverse majore, spitalizare redusă și mortalitate [13,14,15], fiind cel mai mare efect de tratament s-a observat la pacienții cu risc crescut cu boală coronariană mai activă [15].
Recenta recomandare susține prioritatea vaccinării împotriva gripei la pacienții obezi; un program de vaccinare trebuie evaluat pe deplin la adulții obezi. Vaccinurile cu doze mari concepute pentru vaccinarea persoanelor peste 65 de ani pot fi utilizate și la populația obeză [9, 10].
Risc cardiovascular și infecție gripală
În secolul al XX-lea, în timpul epidemiilor de gripă, a existat un exces de mortalitate din cauza bolilor cardiovasculare [16]. Un studiu recent care a inclus 364 spitalizări pentru infarct miocardic acut a demonstrat un risc crescut de infarct miocardic acut în decurs de o săptămână după infecția cu virusul gripal, până la un risc care a fost de șase ori mai mare decât riscul din anul anterior sau după debutul infecției [17]. . Complicațiile cardiovasculare asociate cu infecția gripală includ miocardită, revărsat pericardic, miopericardită, disfuncție ventriculară dreaptă și stângă, infarct miocardic, insuficiență cardiacă, accident vascular cerebral și insuficiență circulatorie datorată șocului septic [13, 18,19,20]. Riscul de infarct miocardic după o infecție respiratorie ușoară revine la valoarea inițială în aproximativ 5 săptămâni, dar în cazul pneumoniei complicate de sepsis, riscul persistă până la 10 ani după infecție [16] [21].
Agenții infecțioși (inclusiv virusul gripal) au fost implicați în etiologia aterosclerozei [22]. Au fost descrise mai multe mecanisme prin care gripa crește riscul de evenimente cardiovasculare; pot fi legate de mediatori proinflamatori, stimulare simpatică și activarea cascadei de coagulare [19].
Infarct miocardic
Conform celei de-a patra definiții universale a infarctului miocardic, există 5 tipuri de infarct miocardic pe baza evaluării clinice, electrocardiografice și de laborator [23]. Infecția gripală poate declanșa infarctele miocardice de tip 1 și 2 [16].
Infarctul miocardic de tip 1 este definit ca ischemie miocardică cauzată de boala arteria coronariană aterotrombotică și este de obicei precipitată prin întreruperea plăcii aterosclerotice care poate fi ruptură sau eroziune [23]. Este important să ne amintim că plăcile aterosclerotice conțin, de asemenea, celule inflamatorii și citokine pro-inflamatorii, cum ar fi interleukinele 1, 6 și 8, și factorul de necroză tumorală α sunt generate ca răspuns al infecției. Aceste citokine inflamatorii pot activa celulele inflamatorii în plăcile aterosclerotice [16] [24].
Infecția acută cu gripă este asociată cu o stare procoagulantă care crește riscul de tromboză coronariană în locurile de întrerupere a plăcii [16] [25, 26]. Infecția cu virusul gripal este asociată cu expresia genelor care au fost legate de activarea trombocitelor: expunerea la H1N1 crește semnătura expresiei genelor plachetare, care este asociată cu infarctul miocardic [25].
Infarctul miocardic de tip 2 ar putea fi luat în considerare cu o creștere și/sau scădere a valorilor troponinei cardiace și dovezi ale unui dezechilibru între aportul de oxigen miocardic și cererea care nu au legătură cu tromboza coronariană. [23]. Infecția gripală produce un răspuns inflamator sistemic, cu o creștere a frecvenței cardiace care rezultă și scurtează timpul de umplere în timpul diastolei, compromitând astfel aportul sanguin coronarian. Dacă apare șocul septic, acesta poate avea un efect advers substanțial asupra perfuziei coronare. La pacienții mai în vârstă cu plăci coronariene cronice, inflamația sistemică determină nepotrivire metabolică cardiacă, crescând riscul de infarct miocardic [16, 18].
Insuficienta cardiaca
Infecția gripală este, de asemenea, asociată cu creșterea mortalității la pacienții cu insuficiență cardiacă [27] și este vulnerabilă la complicațiile asociate gripei [28] [29]. Acest tip de pacienți are rezerve cardiace și respiratorii limitate și este posibil să nu tolereze cererea metabolică și hipoxemia, exacerbând boala cardiacă subiacentă probabil datorită unei activități crescute a sistemului nervos simpatic, hipoxemiei și disfuncției renale care poate duce la supraîncărcare de volum [28].
Într-o inimă sănătoasă, infecția acută severă cu gripă produce creșteri proinflamatorii ale nivelului de citokine care pot provoca miocardită acută [28] [18], caracterizată printr-un spectru larg de simptome care merg de la cursuri asimptomatice la semne de infarct miocardic până la boli devastatoare cu cardiogen șoc [30] [31]. Miocardita rezultă adesea din infecții virale obișnuite și răspunsuri post-virale mediate de imunitate [30]. În miocardita acută, există o incidență ridicată a anomaliilor mișcării peretelui. În timpul epidemiilor de gripă, 15% dintre pacienții internați la un spital militar cu infecție gripală prezentau anomalii ale mișcării pereților pe ecocardiogramă [18]. Acest lucru devine important, datorită faptului că boala inflamatorie a miocardului este considerată un precursor al cardiomiopatiei dilatate [30] [32]. Constatările electrocardiografice la pacienții cu miocardită variază de la modificările nespecifice ale undelor T și ale segmentului ST la creșterea segmentului ST asemănătoare unui infarct miocardic acut; pot fi prezente și aritmii supraventriculare și ventriculare. Rezultatele electrocardiografice care sunt legate de rezultatul clinic slab includ o prelungire a QTc la 440 ms, o axă QRS anormală și bătăi ectopice ventriculare [30].
Un studiu recent dezvoltat pentru a evalua incidența și consecințele hemodinamice ale disfuncției ventriculare drepte și ventriculare stângi la pacienții cu infecție cu H1N1 a demonstrat că la internare 72% aveau funcție ventriculară anormală (46% aveau anomalii ventriculare stângi izolate și 39% aveau disfuncție ventriculară dreaptă izolată) iar 14% au avut disfuncție biventriculară. La urmărire, funcția ventriculară dreaptă a avut tendința de a se agrava în timpul spitalizării, dar funcția ventriculară stângă a avut tendința de a se normaliza. Cu toate acestea, pacienții cu disfuncție ventriculară au nevoie de o terapie mai agresivă și de strategii ventilatorii de salvare, cum ar fi oxidul azotic inhalat, poziționarea predispusă și oxigenarea membranei extracorporale [18].
Accident vascular cerebral
În timpul epidemiilor de gripă, spitalizările pentru bolile cerebrovasculare cresc [33]. A fost sugerată o creștere a incidenței accidentului vascular cerebral ischemic în decurs de 2 săptămâni după infecția gripală [34, 35]. Calea proteinei C și fibrinoliza endogenă sunt mecanisme asociate cu ischemie cerebrovasculară și infecție gripală [19]. Infecția gripală dezvoltă o stare protrombotică prin creșterea expresiei factorului tisular și scade capacitatea fibrinolitică prin expresia crescută a inhibitorului activatorului plasminogen-1 (PAI-1). Acest lucru are ca rezultat un dezechilibru între coagulare și căile anticoagulante [36].
La fel ca în infarctul miocardic, relația dintre inflamația sistemică și fiziopatologia accidentului vascular cerebral a arătat că accidentul vascular cerebral apare adesea într-o stare preexistentă de inflamație datorită aterosclerozei, obezității sau infecției [37].
Posibile efecte cardioprotectoare ale vaccinării împotriva gripei
Al șaselea grup de lucru comun al Societății Europene de Cardiologie și alte societăți de prevenire a bolilor cardiovasculare în practica clinică recomandă ca vaccinarea anuală împotriva gripei să poată fi luată în considerare la pacienții cu boli cardiovasculare stabilite (clasa IIb, nivel C) [38], pe baza faptului că că riscul unui eveniment cardiovascular (infarct miocardic sau accident vascular cerebral) este de peste patru ori mai mare după o infecție a tractului respirator, cu cel mai mare risc în primele 3 zile după infecție [39]. Au fost dezvoltate mai multe studii care demonstrează că vaccinarea împotriva gripei reduce mortalitatea, spitalizarea și sindroamele coronariene acute la pacienții cu boli coronariene și/sau insuficiență cardiacă [13].
Mecanismele prin care inflamația acută afectează riscul de evenimente vasculare includ următoarele: disfuncție endotelială, stare procoagulantă și modificări inflamatorii în plăcile aterosclerotice [39, 40]. Se știe, de asemenea, că activitatea inflamatorie sistemică persistentă este un factor de risc pentru bolile cardiovasculare, iar nivelurile mai mari de interleukină-6 din sânge cresc mortalitatea cardiovasculară la un an după infectarea cu pneumonie [41]. Acest răspuns inflamator sistemic poate fi redus prin vaccinare [13]. Atunci când se estimează costul și beneficiul intervențiilor pentru prevenirea pneumoniei, ar trebui luată în considerare și asocierea pneumoniei cu riscul bolilor cardiovasculare [40].
Pacienții cu insuficiență cardiacă cronică sunt vulnerabili la complicațiile legate de gripă (inclusiv infecții secundare, cum ar fi pneumonia și exacerbările acute ale insuficienței cardiace). Recent, Procesul PARADIGM-HF a evaluat asocierile dintre primirea vaccinului antigripal și spitalizări cu deces cardiovascular sau insuficiență cardiacă, spitalizări pentru toate cauzele și spitalizări cardiopulmonare sau legate de gripă, concluzionând că vaccinarea a fost asociată cu un risc redus de deces [42].
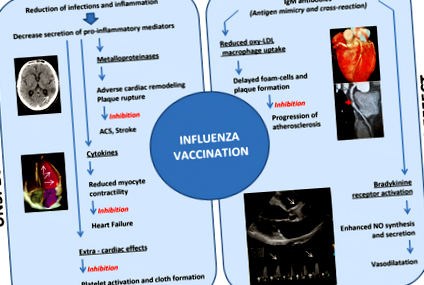
Au fost descrise două mecanisme posibile prin care vaccinarea antigripală poate reduce evenimentele cardiovasculare: efecte nespecifice și specifice [13]. mecanism nespecific se bazează pe faptul că infecția gripală determină un răspuns inflamator sistemic, disfuncție endotelială și o stare procoagulantă. Acești factori au efecte negative asupra pacienților cu boli cardiovasculare anterioare, cum ar fi bolile cardiace ischemice și insuficiența cardiacă, cauzând insuficiență cardiacă acută, edem pulmonar sau destabilizarea bolii cardiace ischemice cronice, ducând la infarct miocardic sau moarte subită cardiacă [13] [15]. ]. Vaccinarea antigripală reduce riscul de infecție și inflamație prin scăderea secreției mediatorilor proinflamatori, cum ar fi citokinele (care determină reducerea contractilității miocardice) și metaloproteinazele (care provoacă remodelare cardiacă adversă și ruperea plăcii); vaccinarea împotriva gripei determină, de asemenea, inhibarea activării trombocitelor și a formării pânzelor [13] [43].
mecanism specific ia în considerare proprietățile imunologice ale vaccinului. Efectul protector al vaccinului antigripal a fost demonstrat în mai multe studii. Pentru a explica efectul pleiotrop al vaccinului antigripal, a fost propusă „mimica antigenică” între placa aterotrombotică și virusul gripal [22]. S-a propus, de asemenea, că există o „reacție încrucișată” autoimună între gripă și ateroscleroză [13] [44].
Figura 1 rezumă posibilul mecanism cardioprotector al vaccinării împotriva gripei [13].
Posibile mecanisme cardioprotectoare ale vaccinării împotriva gripei
- Obezitate, hipertensiune și boli vasculare SpringerLink
- Obezitatea și excesul de greutate conduc la mortalitatea prematură a bolilor cardiovasculare, descoperă cercetările
- Asocierea prospectivă a dietei mediteraneene cu incidența bolilor cardiovasculare și
- Obezitatea și riscul cardiovascular după renunțarea la fumat Cele mai recente dovezi
- Obezitatea și Crohn; boala care este primul, oul sau puiul