Abstract
rezumat
Boala celiacă a adulților a devenit din ce în ce mai recunoscută în America de Nord (1), chiar și în mediile de îngrijire primară (2). Detectarea poate fi simplă, dar mai multe capcane contribuie la sub-diagnostic, precum și la supra-diagnostic. Boala celiacă la adulți necesită diferențierea de alte tulburări, unele frecvente, dar nu sensibile la gluten, deoarece unele imită aspectul său clinic și histologic. Rar, boala celiacă poate deveni refractară sau, de la bun început, rezistentă la tratament. În aceste cazuri, se pot dezvolta sau pot fi deja prezente tulburări mai sinistre, cum ar fi limfomul.
Pacienții recomandați au adesea diaree cronică mai mult de o lună, cu studii fecale negative pentru agenții patogeni bacterieni și paraziți. Textele medicale furnizează algoritmi pentru testele de diagnostic costisitoare și consumatoare de timp. Unele sunt dependente de pacient, necesită colectări temporizate și sunt dificil de făcut cu precizie de laborator. Adesea, acestea pot fi eludate cu biopsii endoscopice precoce ale intestinului subțire. Unii pot să nu aibă diaree sau să slăbească. În schimb, apar deficiența de fier sau valorile chimice modificate (de exemplu, niveluri scăzute de folat seric sau albumină). Alternativ, poate fi diagnosticată inițial o tulburare strâns legată de boala celiacă (de exemplu, boala tiroidiană autoimună, diabetul insulino-dependent și dermatita herpetiformă). În cele din urmă, testele de sânge pozitive de screening (de exemplu, anticorpi împotriva transglutaminazei tisulare) pot duce la suspiciunea bolii celiace. Modificările patologice găsite în boala celiacă au fost detaliate în detaliu și ilustrate în altă parte cu fotomicrografii reprezentative (3,4).
Un diagnostic definitiv este uneori dificil, deoarece există multe capcane. Deoarece diagnosticul se bazează patologic, medicul poate beneficia de o experiență de instruire „practică” în interpretarea biopsiei intestinale și de o interacțiune continuă cu patologi experți. Imperativul critic este comunicarea problemei clinice către patologi și transmiterea de biopsii de calitate cu site-urile lor notate cu precizie pentru a optimiza evaluarea. Un raport clinic relevant de patologie bazat pe severitatea perturbărilor arhitecturale poate fi deosebit de valoros.
MODIFICĂRI ENDOSCOPICE ÎN BOLIA CELIACĂ
Modificările endoscopice ale bolii celiace reflectă dispariția tiparelor normale de mucoasă. A fost raportată o suprafață tubulară netedă, cu pliuri „festonate” sau „crestate” (5). Modificări similare au fost descrise cu endoscopia fără capsule (6). Acestea nu sunt specifice bolii celiace și apar în alte tulburări cu afectare duodenală (de exemplu, boala Crohn) (7,8). Deși modificările macroscopice pot direcționa locul biopsiei (7), acestea pot fi limitate și se corelează slab cu modificările biopsiei, inclusiv cele severe. Endoscopiștii cu experiență estimează că aproximativ 10% din cazuri au fost diagnosticați deoarece biopsiile duodenale de screening au fost efectuate în timpul evaluărilor endoscopice, nu pentru că s-au găsit markeri endoscopici (9). În schimb, un aspect endoscopic „normal” nu este suficient pentru a exclude boala celiacă. Metodele mai noi ale intestinului subțire se pot dovedi utile. Studiile pe capsule pot ajuta la definirea gradului macroscopic al bolii și complicațiile pot fi mai bine apreciate (10,11). Enteroscopia cu balon dublu poate apărea ca un instrument și mai eficient în situații selectate, deoarece este posibilă biopsia dirijată de-a lungul lungimii intestinului subțire (12) și pot fi identificate modificări patologice care au fost omise anterior de studiile cu capsule (13).
În scopuri clinice, biopsiile au fost clasificate pe baza gradului de arhitectură perturbată, împreună cu caracteristici diagnostice specifice (3). Sunt disponibile mai multe metode de clasificare. Unii (de exemplu, clasificarea Marsh) și-au găsit drumul în domeniul clinic (14), dar acordul intraobserver a fost redus (15). Multiple biopsii din locuri separate sunt utile deoarece unele tulburări relevă doar modificări focale la nivelul intestinului subțire (de exemplu, boala Crohn) (16), în timp ce altele prezintă modificări severe difuze, dar variabile (de exemplu, giardioză). Eșantionarea mucoasei cu apariție normală și anormală este, de asemenea, importantă, mai ales dacă sunt prezente eroziuni sau ulcere, deoarece unele modificări microscopice sunt cel mai bine apreciate în mucoasa mai puțin inflamată sau reactivă (de exemplu, celulele limfoide maligne).
PREGĂTIREA ȘI MANIPULAREA BIOPSIEI
Biopsiile duodenale endoscopice trebuie interpretate cu prudență din cauza dimensiunii mai mici (în comparație cu biopsiile de aspirație) și a localizării lor proximale. Materialul acceptabil pentru biopsie poate fi obținut pentru evaluarea diagnosticului, dar biopsiile mai mari sunt mai bune (17,18). Biopsiile din bulbul duodenal pot avea vilozități mai scurte, cu mucoasă „pseudoflatată” deasupra glandelor Brunner (adică așa-numitul „artefact al glandei Brunner”), dar hiperplazia celulei epiteliale a criptelor, care este tipică bolii celiace adulte, nu este prezentă. De asemenea, biopsiile care prezintă „duodenită cronică” sau „inflamație nespecifică” în bulbul duodenal ar putea fi cauzate de boala celiacă, dar acestea reflectă de obicei boala peptică sau leziunea indusă de medicamente (de exemplu, antiinflamatoare nesteroidiene). Într-adevăr, ar trebui luate în considerare o serie de alte boli (de exemplu, boala Crohn), mai ales dacă se constată modificări în intestinul subțire distal.
Artefactele rezultă din manipularea eșantionului în suita de endoscopie sau cu prelucrarea în laborator. Trauma tehnică se poate datora procedurii de biopsie (de exemplu, așa-numitul „artefact de zdrobire a biopsiei”). Acestea sunt mai frecvente dacă se obțin specimene mici, dacă se obțin mai multe biopsii cu o singură trecere pentru a accelera viteza procedurii și dacă biopsiile „țesut lacrimal” cu forceps plictisitoare sau traumatizate. Specimenele tachinate din cupa forcepsului cu un ac sau o scobitoare cu ecartament îngust ar trebui transferate ușor pentru a filtra hârtia sau plasa monofilament cu o orientare „mucoasă cu fața în sus” înainte de imersiunea într-un fixativ. Eșantioanele trebuie prezentate întotdeauna în recipiente separate, fiecare cu locul precis al intestinului subțire definit, nu ca un amestec de biopsii multiple din diferite locuri într-un singur recipient.
O orientare deficitară a eșantionului poate apărea și în timpul pregătirii blocului de parafină pentru secționarea în serie. Rezultatele „artefactului tangențial” pot apărea dacă secțiunile sunt luate în afara nucleului biopsiei. Acest artefact este, de asemenea, mai predispus să apară dacă mai multe biopsii sunt încorporate într-un singur bloc, deoarece biopsiile individuale sunt dificil de orientat din punct de vedere tehnic în același plan, chiar și de către un tehnician expert. Deși doar o singură biopsie poate fi suficientă, mai multe biopsii din diferite locuri sunt optime. În circumstanțe speciale (de exemplu, simptome recurente în boala celiacă stabilită), pot fi necesare biopsii din mai multe locuri de-a lungul lungimii intestinului subțire, folosind un instrument mai lung (de exemplu, un tub hidraulic, colonoscop sau enteroscop cu balon dublu). Într-un studiu (19) cu pacienți cu boală celiacă împreună cu limfoame, doar una din 88 de biopsii avea celule maligne (19).
BOALĂ CELIACĂ CLASICĂ
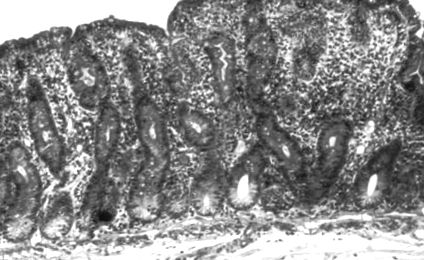
Diareea, scăderea în greutate și malabsorbția apar frecvent în boala celiacă clasică. Modificările patologice sunt de obicei prezente în intestinul subțire proximal (Tabelul 1). De obicei, se constată o leziune mucoasă „severă („ plană ”) (figurile 1 și 2). 2). Într-adevăr, cea mai frecventă cauză a unei leziuni mucoase severe în țările occidentale este boala celiacă (3). Modificări similare au fost etichetate drept „distructive plate” sau „leziuni de tip 3 de mlaștină” (14). Vilele sunt absente sau rudimentare. Se observă elemente crescute ale celulelor limfoide ale laminei proprii (în special celule plasmatice și limfocite) și limfocite intraepiteliale crescute. Suprafața epitelială este mai cuboidală (mai degrabă decât coloană). Hiperplazia celulelor epiteliale criptare apare împreună cu un indice mitotic crescut. Pot apărea modificări subcelulare (de exemplu, vacuolizare epitelială crescută) și glicocalix modificat (adică, prezentat cu lectine) (20). Cu o dietă strictă fără gluten, aceste modificări revin la normal (Figura 3). Site-urile proximale comparabile ale intestinului subțire vor prezenta în cele din urmă îmbunătățiri histologice, deși pot fi necesare perioade prelungite, în special la adulții în vârstă (21). Vor reapărea și indicii mitotici de criptare se normalizează. Celularitatea laminei proprii și numărul de limfocite intraepiteliale se reduc la normal.
Leziune mucoasă „plană” severă prezentată într-o secțiune de biopsie din regiunea ligamentului Trietz. Vilele sunt rudimentare și atrofice, cu cripte hiperplazice alungite. Celularitatea laminei proprii este crescută și se văd numeroase cifre mitotice. Aceste modificări sunt caracteristice, dar nu specifice bolii celiace adulte (pata de hematoxilină și eozină; mărire originală × 75)
Vedere cu o putere mai mare a aceleiași biopsii prezentată în Figura 1. Se observă un număr crescut de limfocite intraepiteliale (colorare hematoxilină și eozină; mărire originală × 250)
Secțiunea de biopsie a intestinului subțire post-tratament dintr-un site similar de biopsie prezentat în Figurile 1 și 2, 2, obținut la opt săptămâni după inițierea unei diete stricte fără gluten. Există normalizarea modificărilor arhitecturale anormale. Vilele sunt alungite cu cripte mai scurte. Se văd mai puține figuri mitotice. Celularitatea laminei proprii este semnificativ redusă. Celulele epiteliale sunt mai coloane și numărul limfocitelor intraepiteliale este redus. Acest răspuns fără dietă fără gluten este caracteristic bolii celiace definite de biopsie (pata de hematoxilină și eozină; mărire originală × 75)
TABELUL 1
Modificări ale biopsiei bolii celiace adulte
| Villi absente sau rudimentare, hiperplazie epitelială a criptelor (nu hipoplazie), indicele mitotic crescut al celulei epiteliale a criptei, conținut crescut de celule limfoide ale laminei proprii, limfocitoză intraepitelială, celule epiteliale cuboidale (mai degrabă decât coloane) |
| Alți termeni includ criptă hiperplazică (nu hipoplazică) atrofie viloasă |
| Similar cu leziunea „distructivă plană” sau „leziunea Marsh type 3” |
| Leziune moderată |
| Anomalii similare, dar modificările nu sunt la fel de pronunțate, cu modificări limitate, dar definite, în arhitectura vilă |
| O formă de perturbare arhitecturală severă variabilă |
| Similar cu leziunea „hiperplastică infiltrativă” sau „Marsh type 2” |
| Leziune ușoară |
| Villi rămân nealterate sau doar modificate minim în dimensiune, cu o pierdere a polarității celulelor epiteliale și o creștere marcată a limfocitelor intraepiteliale |
| Celularitatea laminei proprii poate fi mărită marginal |
| O formă de perturbare arhitecturală severă variabilă |
| Similar cu leziunea „infiltrativă” sau „Marsh type 1” |
În unele, apar grade mai mici de arhitectură viloasă modificată (3). Datorită utilizării crescute a testelor de screening serologic, acestea sunt frecvent apreciate (adică așa-numitul „aisberg celiac”). Cu „leziunea ușoară”, vilozitățile rămân în mare parte neschimbate sau minim modificate. Epiteliul anormal poate fi observat cu pierderea polarității și creșterea limfocitelor intraepiteliale. Modificările sunt similare cu leziunea „infiltrativă” sau „leziunea Marsh 1” (14). Pentru „leziunea moderată”, apar modificări arhitecturale definite. Acestea pot fi clasificate ca leziuni „hiperplastice infiltrative” sau „Marsh 2” (14). Modificări variabile severe pot fi prezente în boala celiacă, dermatita herpetiformă (22,23) și limfomul intestinal (24,25). Rezultate similare sunt raportate la rudele asimptomatice de gradul I (26).
Modificările arhitecturale mai puțin severe ar trebui să determine investigarea unei cauze nonceliace, inclusiv infecții (de exemplu, giardioză și criptosporidioză). Limfocitoza epitelială singură, cu arhitectură normală a intestinului subțire, poate prezenta un răspuns clinic favorabil la o dietă fără gluten (aproximativ 10%), sugerând că numărul crescut de limfocite intraepiteliale poate indica boala celiacă la adulți (27). Unii au raportat că diagnosticul poate fi posibil chiar și fără aceste modificări, folosind doar markeri imunohistochimici pentru a eticheta limfocitele intraepiteliale (28-30).
Modificările intestinului subțire în boala celiacă la adulți apar și într-o altă dimensiune - de-a lungul lungimii intestinului subțire. Anterior, acestea au fost detectate folosind instrumente de aspirație pentru a procura biopsii în intestinul subțire mai distal (de exemplu, un tub multifuncțional pentru mai multe biopsii în același loc și un tub hidraulic Quinton pentru diferite locuri). Tehnologiile mai noi permit acum vizualizarea suplimentară pe lungimea intestinului subțire, inclusiv unele metode emergente (de exemplu, studii enteroscopice cu capsulă și balon dublu).
CRITERII PENTRU DIAGNOSTICUL BOLII CELIACE
BOALA OCULTĂ ȘI LATENTĂ CELIACĂ
O altă formă adultă este boala celiacă latentă, raportată inițial în dermatita herpetiformă (60) și mai târziu, în limfomul intestinului subțire (25). În boala latentă, arhitectura intestinului subțire a fost normală. Cu toate acestea, o dietă bogată în gluten a provocat modificări patologice de severitate variabilă, indicând faptul că mucoasa intestinului subțire a fost sensibilă la gluten. Aceste modificări nu au fost detectate la voluntarii normali hrăniți cu diete similare care conțin gluten. Mai mult, aceste modificări ale intestinului subțire induse de gluten în boala celiacă latentă s-au dovedit, de asemenea, că răspund la tratament cu o dietă fără gluten.
ALTE CAUZE ALE LEZIUNILOR GRAVE SAU ‘VARIABLE GRAVE
Alte cauze ale leziunilor grave sau variabile ale biopsiei intestinului subțire pot fi asociate cu diaree sau malabsorbție (tabelele 2 și 3). 3). Cu toate acestea, numai boala celiacă răspunde la o dietă fără gluten. Ovăzul poate fi consumat în siguranță (63), dar poate fi contaminat și de alte boabe. În plus, ovăzul singur poate provoca anomalii în arhitectura vilozitară (64).
- Gestionarea minim invazivă a obezității Perle, capcane și experiență în Caraibe -
- TENDINȚE MODERNE ÎN DIAGNOSTIC ȘI TRATAMENTUL BOLII FICATULUI GRAS NALCOOLIC ÎN SUPRAPONDERE
- PRIME PubMed Dieta fără gluten este un factor de risc nutrițional pentru adolescenții cu boală celiacă
- Asocierea rară a bolii celiace cu miastenia gravis la un pacient cu alte tulburări imune
- Siguranța GFD la femeile gravide fără boală celiacă care investighează obiceiurile deteriorate - PubMed