Abstract
Recâștigarea greutății, creșterea țesutului adipos și rezistența la insulină pot apărea în câteva zile după încetarea dietei regulate și a exercițiilor fizice. Acest fenomen a fost atribuit, în parte, acțiunilor hormonilor de stres, precum și inflamației locale și sistemice. Am investigat efectul curcuminei, un polifenol natural cunoscut pentru proprietățile sale antiinflamatorii și acțiunea inhibitorie asupra activității 11β-HSD1, asupra păstrării sănătății metabolice și limitării creșterii țesutului adipos ca urmare a încetării exercițiului zilnic și a restricției calorice (CR). Șobolanii Sprague-Dawley (în vârstă de 6-7 săptămâni) au fost supuși unui protocol de „antrenament” de acces voluntar de 24 de ore pe roată și CR (15-20 g/zi;
50-65% din aportul ad libitum) pentru 3 săptămâni („Toți instruiți”) sau au fost sedentari și au fost hrăniți ad libitum („Sed”). După 3 săptămâni, All Trained au fost împărțiți în mod aleatoriu într-un grup care a fost terminat imediat („Antrenat”) și două grupuri reținute care aveau roțile blocate și au fost reintroduse în hrana ad libitum timp de 1 săptămână. Grupurile blocate pe roți au primit fie un gavaj zilnic al unui placebo („Detrained + Placebo”), fie curcumină (200 mg/kg) („Detrained + Curcumin”). Încetarea RC zilnică și a exercițiilor fizice a determinat o creștere a masei corporale, precum și o creștere de 9 până la 14 ori a masei țesutului adipos epididimal, perirenal și inghinal, toate acestea fiind atenuate de curcumină (P Cuvinte cheie: recâștigarea greutății, detrenare, curcumină, inflamație, țesut adipos
activitatea fizică și restricția calorică (CR) sunt modificări ale stilului de viață pentru a induce pierderea în greutate și a combate bolile cronice. Cu toate acestea, mulți indivizi întâmpină adesea dificultăți în susținerea pierderii în greutate cu succes (54). Mecanismele biologice care stau la baza recuperării greutății rămân incomplet înțelese, dar au fost atribuite unor caracteristici metabolice modificate în mușchiul scheletic, ficatul, țesutul adipos, creierul, intestinul și sistemul neuroendocrin. Mai mult, aceste modificări biologice pot apărea rapid odată cu întreruperea nivelurilor mai ridicate de activitate fizică zilnică și CR. De exemplu, reducerea numărului zilnic de pași la oameni (23, 32, 36) și încetarea rulării roților la rozătoare (24, 25, 28) induce rezistența la insulină a mușchilor scheletici, intoleranța la glucoză și o creștere substanțială a masei adipoase în câteva zile. Important, dacă aceste efecte dăunătoare ar putea fi contracarate cu modificări suplimentare ale stilului de viață sau cu strategii farmacologice, atunci volumul biologic pentru greutate recâștigă, chiar și după încetarea activității fizice zilnice, poate fi atenuat.
Folosind acest model de antrenare-detenție, scopul general al acestui studiu a fost de a caracteriza în continuare mecanismele timpurii care duc la recâștigarea greutății inițiale, la rezistența la insulină și la creșterea țesutului adipos. Pe baza varietății proprietăților biologice ale curcuminei, care culminează cu inflamația redusă, inhibarea semnalelor de creștere a țesutului adipos și producția redusă de GC activă, am emis ipoteza că administrarea curcuminei în perioada de detrenare ar atenua recuperarea greutății și disregularea metabolică asociată cu detrenarea (adică rezistență la insulină, intoleranță la glucoză).
MATERIALE ȘI METODE
Declarație de etică.
Acest studiu a fost aprobat de Comitetul pentru îngrijirea animalelor de la Universitatea York, în conformitate cu liniile directoare ale Consiliului canadian pentru îngrijirea animalelor.
Tratamentul rozătoarelor și proiectarea experimentală.
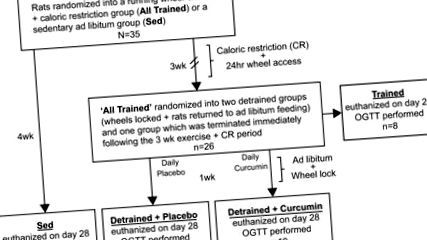
Modelul voluntar de rulare utilizat în acest studiu a implicat asigurarea accesului 24 de ore la roțile rulante plus CR zilnic timp de 3 săptămâni urmat de blocarea roților și reintroducerea la hrănirea ad libitum cu sau fără gavaj curcumină zilnic. Pentru aceasta, 35 de șobolani Sprague-Dawley masculi (Laboratoarele Charles River, 50-75 g la sosire) au fost adăpostiți individual într-un mediu controlat de umiditate și temperatură (50% umiditate relativă, 22-23 ° C) cu un 12:12 -h ciclu lumină-întuneric (0800-2000). O imagine de ansamblu a proiectului experimental este prezentată în Fig. 1. Pe scurt, șobolanii au fost împărțiți în mod aleatoriu în două grupuri, un grup sedentar alimentat ad libitum (Sed) (n = 9) și un grup de alergare voluntară (All Trained, n = 26) alimentat cu o dietă CR de 15-20 g/zi
50-65% din consumul de hrană ad libitum) al rozătorilor standard (Purina Labdiet, nr. 5012, St. Louis, MO). În scopuri practice, peletele au fost cântărite într-o barcă de cântărit până când masa brută a fost de 15-20 g/zi pentru fiecare șobolan restricționat caloric. După 3 săptămâni, grupul All Trained a fost în continuare împărțit în următoarele grupuri: „Antrenat”, „Detrained + Placebo” și „Detrained + Curcumin” (n = 8-10 pe grup, vezi Fig. 1). Grupul instruit a fost eutanasiat la sfârșitul celei de-a treia săptămâni și folosit ca o comparație de blocare pre-roată. Grupurile reținute au avut roțile de rulare blocate, au fost reintroduse la hrănirea ad libitum și li s-a administrat zilnic un placebo (Detrained + Placebo) sau curcumină (200 mg/kg) (Detrained + Curcumină) timp de 1 săptămână. Toate grupurile au avut un test oral de toleranță la glucoză (OGTT) administrat în ziua recoltării.
Cronologie experimentală. Șobolanii Sprague-Dawley au fost inițial împărțiți în 2 grupe: Sed și Toți instruiți. Grupul All Trained a avut acces la roți de rulare voluntare 24 de ore pe zi timp de 3 săptămâni și a fost plasat pe o dietă CR de 15-20 g/zi (
50-65% din aportul ad libitum) de chow standard pentru rozătoare. Grupul Sed nu a avut acces la roți și a fost hrănit ad libitum pe tot parcursul studiului. După 3 săptămâni, grupul All Trained a fost împărțit în următoarele grupuri: Antrenat, Detrained + Placebo și Detrained + Curcumin. În ziua 21, grupurile placebo și curcumina au avut roțile blocate, au fost reintroduse la hrănirea ad libitum și li s-a administrat zilnic o bucată orală fie de curcumină, fie de un placebo. Grupul instruit a fost recoltat în ziua 21 și folosit ca comparații înainte de blocare. Grupurile placebo și curcumină au fost recoltate în ziua 28, 1 săptămână după încetarea exercițiului zilnic și CR. Grupul Sed a fost, de asemenea, recoltat în ziua 28. Toate grupurile au avut un test oral de toleranță la glucoză (OGTT) administrat în zilele de recoltare.
Administrarea curcuminei.
Curcumina (nr. C1386, Sigma, Oakville, ON, Canada) a fost dizolvată în dimetil sulfoxid (DMSO, 100% în greutate/vol) la o concentrație de 200 mg/ml, iar un gavaj oral a fost administrat în doză de 1 ml/kg pentru o doză finală de 200 mg/kg pe zi. Grupul placebo a primit doar DMSO la o doză de 1 ml/kg. Această doză a fost selectată pe baza unui studiu în care această doză a atenuat creșterea în greutate și a îmbunătățit profilul lipidelor din sânge la șobolanii obezi cu conținut ridicat de grăsimi (19). Foarte important, mai multe studii nu au raportat nicio toxicitate legată de tratament cu hrănirea curcuminei atât la om (27), cât și la rozătoare (40), chiar și la doze foarte mari (3.000-12.000 mg/kg). În consecință, am avut un nivel ridicat de încredere că doza din acest studiu va fi bine tolerată. Pe de altă parte, această doză ar fi egală cu 14 g zilnic pentru un adult de 70 kg și poate să nu fie o strategie fezabilă de suplimentare pe termen lung. De remarcat, curcumina este cunoscută ca având o biodisponibilitate slabă, iar strategiile recente pentru a depăși acest lucru includ utilizarea de nanoparticule, lipozomi, complexe fosfolipidice și micele (39) care pot reduce doza de curcumină necesară pentru a observa efectele clinice.
Test de toleranță orală la glucoză.
Un test oral de toleranță la glucoză (OGTT) a fost administrat (1,5 g/kg masă corporală, soluție de dextroză 50%) la animale postite peste noapte prin gavaj oral, după cum s-a descris anterior (47), la sfârșitul celei de-a treia săptămâni pentru grupul instruit sau la sfârșitul celei de-a 4-a săptămâni pentru grupul Sed și pentru ambele grupuri detenite (a se vedea Fig. 1 pentru o cronologie). Concentrațiile de glucoză din sânge au fost măsurate cu ajutorul unui glucometru portabil (Bayer, Contour, NY). Plasma a fost, de asemenea, izolată din recoltarea de sânge safen în toată OGTT pentru analiza ulterioară a concentrațiilor de insulină (vezi mai jos). Zona de glucoză de sub curbă (ASC) a fost calculată în raport cu nivelurile de glucoză la jeun ale fiecărui șobolan. Toți șobolanii au fost eutanasiați imediat după finalizarea OGTT.
Analiza plasmatică.
Aproximativ 125 µl de sânge integral au fost colectate de la fiecare animal prin puncția venei safene pentru a măsura nivelurile de insulină plasmatică (nr. 90060, Crystal Chem, Downer’s Grove, IL) și de corticosteron (nr. 07120102, MP Biomedicals, Solon, OH). Pentru aceasta, o mică zonă de păr pe membrele posterioare superioare laterale a fost rasă cu un aparat de ras electric și ștearsă cu un strat subțire de vaselină. Odată localizată vena safenă, s-a folosit un ac steril cu calibru 25 pentru puncția venei și sângele integral a fost colectat în tuburi capilare cu microvetă acoperite cu litiu-heparină (nr. 16,443,100, Sarstedt, Canada) și centrifugat la 14,500 g Spin Plus, Brinkman Instruments) timp de 5 minute, transferate în tuburi din polietilenă și stocate la -80 ° C până la o analiză ulterioară. Acizii grași neesterificați (NEFA) (nr. 999-34691, 995-34791, 991-34891, 993-35191, Wako Diagnostics, Richmond, VA) și CRP (nr. RAB0097, Sigma-Aldrich) au fost măsurați din sângele colectat în timpul decapitării în urma OGTT.
Măsuri de rezistență la insulină și funcția celulelor β.
Evaluarea modelului homeostaziei (HOMA) a fost descrisă în detaliu anterior (31). Pe scurt, rezistența la insulină (HOMA-IR) a fost calculată după cum urmează: [glucoză post (mM) × insulină post (mU/l) /22,5]. Evaluarea modelului de homeostazie pentru celulele β (HOMA-β) a fost calculată după cum urmează: [20 × insulină la post [mU/l]/[glucoză la post (mM) - 3,5].
Western blot.
analize statistice.
10-12 km/noapte în ultimele 10 zile de acces la roți de rulare voluntare (Fig. 2F).
Masa corporală, consumul de alimente și datele de funcționare. A: masa corporală în timp în toate grupurile. B: masa corporală finală la data recoltării. C: consumul de alimente în timpul perioadelor CR (prima până la a treia săptămână) și ad libitum (a 4-a săptămână). Grupul instruit a fost recoltat la sfârșitul celei de-a treia săptămâni. Grupurile Sed, placebo și curcumină au fost recoltate la sfârșitul celei de-a 4-a săptămâni. D și E: aportul total de alimente în g și, respectiv, kcal, în perioada de detrenare (ultima săptămână). F: distanța de rulare zilnică pe întregul protocol în toate cele 3 grupuri de rulare („Toți instruiți”). * Sed vs. Toate antrenate (P Fig. 3, A - F). După 1 săptămână de consum alimentar ad libitum și blocarea roților, grupul placebo a avut o creștere semnificativă a masei țesutului adipos absolut și relativ în depozitele epididimale, perirenale și inghinale, comparativ cu grupul instruit (P Fig. 3, A - F) . Grupul tratat cu curcumină a avut, de asemenea, o creștere semnificativă a masei țesutului adipos față de grupul instruit; cu toate acestea, au câștigat înapoi semnificativ mai puțin țesut adipos vs. grupul placebo (P Fig. 3, A - F). Grupul placebo a avut o creștere de două ori a masei hepatice absolute vs. grupul instruit și această creștere a fost semnificativ redusă la șobolanii tratați cu curcumină (Tabelul 1). Un rezumat al greutăților relative și absolute ale țesutului pentru mușchiul scheletic și ficat este prezentat în tabelul 1 .
Toate datele sunt mijloace ± SE; n = 8-10. Relative (g/kg masă corporală) și absolute (g) mase tisulare, respectiv, pentru mușchiul scheletic și ficat. O diferență semnificativă este prezentă atunci când grupurile nu împărtășesc o literă (P Fig. 4). În grupul placebo, 1 săptămână de blocare a roții și aportul nelimitat de alimente au deteriorat atât toleranța la glucoză, cât și sensibilitatea la insulină la valori similare sau mai mari decât cele observate în grupul sedentar ad libitum (Fig. 4). Mai precis, grupul placebo a avut o creștere de două și de șase ori a ASC a glucozei și a insulinei, respectiv, în timpul unui OGTT, vs. grupul instruit (P Fig. 4, B și E). După blocarea roților și CR, grupul placebo a avut, de asemenea, o creștere de nouă și de trei ori a HOMA-IR și, respectiv, HOMA-β vs. grupul instruit (P Fig. 4, C și F). Comparativ cu grupul placebo, grupul cu curcumină a menținut glicemia și ASC ale insulinei plasmatice la nivelurile observate în grupul instruit (Fig. 4). Mai mult, HOMA-IR în grupul cu curcumină, deși încă mai mare decât în grupul instruit, a fost mai mic decât cel observat în grupul Placebo, sugerând un rol al curcuminei în păstrarea toleranței îmbunătățite la glucoză și a sensibilității la insulină.
- Serios nu se poate îngrășa (culturisti, carne, alergare, pierde în greutate) - Exerciții fizice și fitness
- Deteriorarea țesutului adipos perivascular legat de obezitate este inversată prin pierderea în greutate susținută la șobolan
- Planul de slăbire Shayne Ward pentru scăderea în greutate Steaua Coronation Street a folosit exerciții fizice pentru a slăbi
- Steaua lui Pretty Little Liars, Sasha Pieterse, dezvăluie o afecțiune care a cauzat o creștere extremă în greutate
- Sport Fitness Tânără Fată Alergare Element gratuit, Exercițiu, Slăbire, Pierdere în greutate PNG transparent