Subiecte
Abstract
Restricția calorică (CR) îmbunătățește sănătatea, reduce incidența cancerului și extinde durata de viață în mai multe organisme, inclusiv șoareci. S-a arătat că CR îmbunătățește reparația exciziei de bază și căile de reparare a exciziei de nucleotide ale reparării ADN-ului, totuși, dacă CR îmbunătățește repararea rupturilor de ADN dublu catenar nu a fost examinat într-un sistem in vivo. Aici utilizăm șoareci reporteri non-omologi de îmbinare finală (NHEJ) pentru a arăta că CR pe termen scurt îmbunătățește puternic repararea ADN-ului de către NHEJ, care este asociat cu niveluri ridicate de ADN-PK și SIRT6.
Am generat un șoarece reporter knock-in care permite măsurarea cantitativă a eficienței NHEJ in vivo folosind endonucleaza I-SceI pentru a induce pauze ADN-ADN specifice site-ului în caseta reporter NHEJ integrată în ROSA26 locus 19 (Fig. 1a). Caseta reporter NHEJ 19 constă din gena GFP întreruptă de intronul Pem1 de șobolan, care nu are omologie cu genomul șoarecelui și un exon „ucigaș” flancat de situsuri I-SceI. GFP este inactivat de prezența exonului ucigaș într-o construcție neamenajată. Tăierile I-SceI duc la eliberarea exonului ucigaș, în timp ce repararea cu succes a NHEJ re-ligează intronul ducând la reactivarea genei GFP. Evenimentele de reparare NHEJ care apar în cadrul intronului tolerează ștergerile (până la 1 kb pe fiecare parte a tăieturii) și inserțiile fără a interfera cu activitatea GFP.
Modelul de șoarece reporter NHEJ oferă un nou instrument pentru a studia efectul CR asupra eficienței NHEJ in vivo. Rapoartele anterioare nu au examinat efectul CR pe termen scurt asupra NHEJ. În special, s-a raportat că 4 săptămâni de CR sunt suficiente pentru ameliorarea modificărilor legate de vârstă ale metilomului ADN 20, sugerând că CR pe termen scurt poate fi suficient pentru a spori eficiența reparării ADN-ului. În acest raport, am folosit șoareci reporteri NHEJ pentru a examina efectul pe termen scurt de 40% CR asupra eficienței NHEJ. Am constatat că eficiența NHEJ a fost mult îmbunătățită prin CR pe termen scurt.
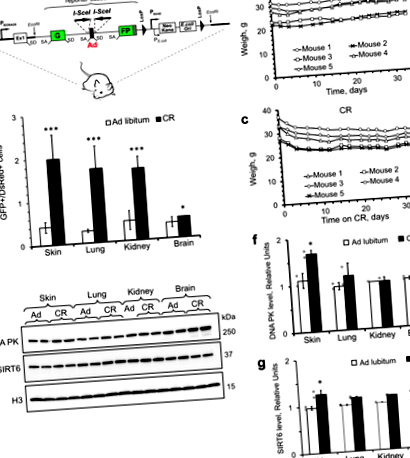
Pentru a calcula consumul zilnic de calorii la șoarecii reporteri NHEJ, am hrănit șoareci ad libitum cu o dietă de pelete de precizie fără praf și am numărat numărul de pelete consumate. Șoarecii au consumat în medie 14,3 ± 1,3 kcal pe zi sub hrănire ad libitum și și-au menținut greutatea corporală (Fig. 1b). În grupul CR, șoarecii au fost hrăniți cu 8,4 kcal/zi, ceea ce a fost egal cu 60% din consumul mediu zilnic de calorii. Șoarecii CR au pierdut greutatea corporală în primele două săptămâni de hrănire și apoi și-au menținut greutatea corporală (Fig. 1c). Toți șoarecii erau găzduiți singuri pentru a asigura un consum egal de alimente. Șoarecii au fost sacrificați la 4 săptămâni de la începutul dietei. NHEJ a fost măsurat în celule primare izolate de piele proaspătă, plămâni, rinichi și creier de șoareci. Testul NHEJ a fost efectuat așa cum s-a descris anterior 19. Pe scurt, celulele au fost co-transfectate cu o plasmidă care codifică enzima I-SceI pentru a induce DSB-urile și o plasmidă DsRed pentru a se normaliza pentru eficiența transfecției și au fost analizate prin citometrie în flux. Eficiența NHEJ a fost calculată ca un raport dintre celulele GFP + și celulele DsRed +. SceI, NHEJ-GFP și DsRed sunt exprimate de la un promotor CMV. Important, CR nu a modificat intensitatea fluorescenței DsRed (suplimentar Fig. 1c), sugerând că expresia I-SceI nu a fost afectată de CR.
Am constatat că CR pe termen scurt a crescut semnificativ eficiența NHEJ la nivelul pielii, plămânilor, rinichilor și țesuturilor cerebrale, comparativ cu șoarecii hrăniți ad libitum din piele, plămâni, rinichi și creier (Fig. 1d). Această creștere a fost asociată cu niveluri crescute de ADN PK (Fig. 1e, f) și SIRT6 (Fig. 1e, g). Aceste rezultate indică faptul că CR pe termen scurt este suficient pentru a spori NHEJ.
Ștergerile foarte mari se pot extinde în regiunea de codificare GFP și pot duce la pierderea semnalului. Deși, teoretic, un tratament CR poate modifica fidelitatea reparării, din studiile noastre anterioare de secvențiere la animale AL din aceeași tulpină, delețiile se extind foarte rar în regiunea codificatoare a genei GFP 19. Prin urmare, modificarea observată a eficienței NHEJ nu poate fi explicată prin fidelitatea modificată a NHEJ.
Studiile anterioare au arătat că CR a împiedicat scăderea legată de vârstă a capacității de reparare 17.18, în timp ce aici arătăm că CR pe termen scurt îmbunătățește NHEJ la animalele tinere. Acest CR pe termen scurt, sau poate postul intermitent, poate oferi un plus de beneficii. Stresul de mediu conferit de CR poate declanșa răspunsul hormetic prin activarea căilor de răspuns la stres, cum ar fi SIRT6 și reglarea în sus a mașinilor de reparare a ADN-ului. Eficiența îmbunătățită a NHEJ va avea ca rezultat niveluri mai scăzute de deteriorare persistentă a ADN-ului, reducerea morții celulare, îmbunătățirea stabilității genomului și reducerea sarcinii mutaționale. Această stabilitate îmbunătățită a genomului va contribui probabil la scăderea incidenței cancerului și la o durată de viață mai lungă conferită de CR. Constatarea noastră că chiar și un CR pe termen scurt este suficient pentru a declanșa aceste efecte benefice este important pentru aplicațiile practice ale CR la om, unde CR pe termen lung este dificil de realizat, în timp ce CR pe termen scurt sau postul intermitent este mai fezabil.
Metode
Animale
Toate experimentele la șoarece au fost efectuate în conformitate cu liniile directoare stabilite de Comitetul pentru Resurse Animale al Universității din Rochester. Șoarecii masculi au fost utilizați în acest studiu și au fost toți într-o singură carcasă pentru a efectua experimente de hrănire controlată de calorii. Experimentele au fost efectuate pe șoareci C57BL/6 în vârstă de 3-5 luni care adăposteau caseta reporter NHEJ în locusul ROSA26 generat de Vaidya și colab. 19 .
Administrarea CR
Șoarecii au fost hrăniți cu dietă de pelete de precizie Dustless (BioServ, Cat # F0074). Cantitatea calculată de hrană de precizie pentru pelete a fost plasată pe podeaua cuștii în fiecare dimineață, resturile de pelete de alimente au fost numărate și îndepărtate zilnic înainte de furnizarea de alimente noi. Un șoarece a devenit moribund și a fost întrerupt din experimentele CR și exclus pentru analiza NHEJ.
Test NHEJ
Culturile de celule primare au fost izolate din piele, plămâni, rinichi și creier de la șoareci așa cum s-a descris anterior 19. Un milion de celule primare cultivate au fost transfectate cu 5 pg de plasmidă pCMV-I-SceI pentru a induce ADN DSB și 0,1 pg de plasmidă pCMV-DsRed pentru a normaliza eficiența transfecției, utilizând programul T-020 Amaxa Nucleofector II. Celulele mouse-ului afișează un nivel ridicat de auto-fluorescență care trebuie exclus pentru a obține date fiabile. Pentru a evita problema autofluorescenței am folosit cantități foarte mici de plasmidă DsRed, astfel încât să nu coincidă cu semnalul GFP permițându-ne să excludem celulele autofluorescente (Fig. 1b suplimentară). La trei zile după transfecție, celulele au fost recoltate și numărul de celule GFP + și celule DsRed + a fost analizat prin citometrie în flux. Transfecțiile triplicate au fost efectuate pentru culturi primare individuale și eficiența NHEJ a fost calculată ca raport dintre celulele GFP + și celulele DsRed +.
Western blot
Celulele în creștere exponențială au fost recoltate cu tripsină, numărate și 106 celule au fost resuspendate în 100 pl de PBS care conțin inhibitori de protează. S-au adăugat 100 uL de 2 × tampon Laemmli (Bio-Rad) și probele au fost fierte la 95 ° C timp de 10 min. Probele au fost separate cu gradient 4-20% SDS - PAGE, transferate la membrana PVDF și blocate în lapte 5% TBST timp de 2 ore la temperatura camerei. Membranele au fost apoi incubate peste noapte la +4 ° C cu anticorpi monoclonali de iepure anti-ADN PKcs (Abcam, ab32566, 1: 1000), anticorpi monoclonali de iepure anti-Sirt6 (CST, # 12486, 1: 1000) sau anticorpi policlonali de iepure anti- Histona H3 (Abcam, ab1791, 1: 10.000) în 5% BSA-TBST. După trei spălări timp de 10 minute cu TBST, membranele au fost incubate timp de 1 oră la temperatura camerei cu IgG capră anti-iepure H&L (HRP) (Abcam, ab6721, 1: 5000). După trei spălări cu semnal TBST a fost dezvoltat cu substrat Clarity Western ECL (Bio-Rad). Imaginile au fost cuantificate cu Image Lab (Bio-Rad). Toate pete prezentate au fost derivate din același experiment și au fost procesate în paralel.
Rezumatul raportării
Mai multe informații despre proiectarea cercetării sunt disponibile în Rezumatul raportării cercetării naturii, legat de acest articol.
Disponibilitatea datelor
Toate datele generate sau analizate în timpul acestui studiu sunt incluse în acest articol publicat (și fișierele sale de informații suplimentare) sau sunt disponibile de la autori la o cerere rezonabilă.
Referințe
Fontana, L., Partridge, L. & Longo, V. D. Extinderea duratei de viață sănătoase - de la drojdie la oameni. Ştiinţă 328, 321-326 (2010).
Mattson, M. P. Aportul de energie, frecvența meselor și sănătatea: o perspectivă neurobiologică. Annu. Rev. Nutr. 25, 237–260 (2005).
Weindruch, R. și Walford, R. L. Restricție dietetică la șoareci începând cu vârsta de 1 an: efect asupra duratei de viață și a incidenței cancerului spontan. Ştiinţă 215, 1415–1418 (1982).
Anderson, R. M., Shanmuganayagam, D. & Weindruch, R. Restricție calorică și îmbătrânire: studii la șoareci și maimuțe. Toxicol. Pathol. 37, 47-51 (2009).
Yu, B. P. Îmbătrânirea și stresul oxidativ: modulare prin restricție dietetică. Radic liber. Biol. Med. 21, 651–668 (1996).
Zainal, T. A., Oberley, T. D., Allison, D. B., Szweda, L. I. & Weindruch, R. Restricția calorică a maimuțelor rhesus scade leziunile oxidative ale mușchilor scheletici. FASEB J. 14, 1825–1836 (2000).
Sohal, R. S., Agarwal, S., Candas, M., Forster, M. J. și Lal, H. Efectul vârstei și restricția calorică asupra deteriorării oxidative a ADN-ului în diferite țesuturi ale șoarecilor C57BL/6. Mech. Îmbătrânire Dev. 76, 215–224 (1994).
Feuers, R. J., Weindruch, R. & Hart, R. W. Restricție calorică, îmbătrânire și enzime antioxidante. Mutat. Rez. 295, 191-200 (1993).
Hyun, D. H., Emerson, S. S., Jo, D. G., Mattson, M. P. și de Cabo, R. Restricția caloriilor reglează sistemul redox al membranei plasmatice în celulele creierului și suprimă stresul oxidativ în timpul îmbătrânirii. Proc. Natl Acad. Știință. Statele Unite ale Americii 103, 19908-19912 (2006).
De Cabo, R. și colab. Restricția calorică atenuează modificările legate de vârstă ale sistemului antioxidant al membranei plasmatice la ficatul de șobolan. Exp. Gerontol. 39, 297–304 (2004).
Guo, Z. M., Yang, H., Hamilton, M. L., VanRemmen, H. & Richardson, A. Efectele restricției de vârstă și de hrană asupra deteriorării ADN-ului oxidativ și a activităților enzimei antioxidante în aorta șoarecelui. Mech. Îmbătrânire Dev. 122, 1771–1786 (2001).
Xia, E., Rao, G., Van Remmen, H., Heydari, A. R. și Richardson, A. Activitățile enzimelor antioxidante în diferite țesuturi ale șobolanilor Fischer 344 masculi sunt modificate de restricția alimentară. J. Nutr. 125, 195–201 (1995).
Guo, Z., Heydari, A. & Richardson, A. Repararea exciziei nucleotidice a ADN transcris activ versus non-transcris în hepatocitele de șobolan: efectul vârstei și restricția dietetică. Exp. Rez. Celulare. 245, 228–238 (1998).
Cabelof, D. C. și colab. Restricția calorică promovează stabilitatea genomică prin inducerea reparării exciziei de bază și inversarea declinului legat de vârstă. Repararea ADN-ului 2, 295–307 (2003).
Heydari, A. R., Unnikrishnan, A., Lucente, L. V. și Richardson, A. Restricție calorică și stabilitate genomică. Acizi nucleici Res. 35, 7485–7496 (2007).
White, R. R. și Vijg, J. Pauzele ADN-ului cu două fire sunt cele care îmbătrânesc? Mol. Celulă 63, 729–738 (2016).
Lee, J. E. și colab. Restricția calorică (CR) reduce declinul dependent de vârstă al activității de îmbinare finală neomologă (NHEJ) în țesuturile șobolanilor. Exp. Gerontol. 46, 891–896 (2011).
Um, J. H. și colab. Modificări specifice țesutului proteinei Ku de reparare a ADN-ului și mtHSP70 la șobolani îmbătrâniti și întârzierea lor prin restricție calorică. Mech. Îmbătrânire Dev. 124, 967–975 (2003).
Vaidya, A. și colab. Șoarecii reporteri knock-in demonstrează că repararea ADN prin îmbinarea finală neomologă scade odată cu vârsta. PLoS Genet. 10, e1004511 (2014).
Kim, C. H. și colab. Restricția calorică pe termen scurt ameliorează modificările genomului, legate de vârstă, în metilarea ADN-ului. Celula de îmbătrânire 15, 1074–1081 (2016).
Mulțumiri
Această lucrare a fost susținută de subvenții de la Institutele Naționale de Sănătate către V.G. si ca.
Informatia autorului
Afilieri
Departamentul de Biologie, Universitatea din Rochester, Rochester, NY, 14627, SUA
Zhonghe Ke, Denis Firsanov, Brianna Spencer, Andrei Seluanov & Vera Gorbunova
Puteți căuta acest autor și în PubMed Google Scholar
Puteți căuta acest autor și în PubMed Google Scholar
Puteți căuta acest autor și în PubMed Google Scholar
Puteți căuta acest autor și în PubMed Google Scholar
Puteți căuta acest autor și în PubMed Google Scholar
Contribuții
Z.K., D.F., A.S. și V.G. cercetare proiectată; Z.K., D.F. și B.S. efectuat experimente; Z.K., A.S. și V.G. a analizat datele și a scris lucrarea cu contribuția tuturor autorilor.
Autori corespondenți
Declarații de etică
Interese concurente
Autorii nu declară interese concurente.
Informatii suplimentare
Nota editorului Springer Nature rămâne neutru în ceea ce privește revendicările jurisdicționale din hărțile publicate și afilierile instituționale.
- Tărâță de ovăz, Calculator brut de calorii
- Răspunsurile cititorilor la „Transferul de calorii o nouă abordare a crizei globale a nutriției”
- Obezitatea, o afecțiune care imită îmbătrânirea prematură - ScienceDirect
- Pocket Calorie Counter, ediția 2016 Ghid complet discret și portabil pentru gestionarea
- Salo - calorii, beneficii, daune