Abstract
Metformina este medicamentul cel mai frecvent prescris pentru diabetul de tip 2 (T2DM) din lume. Are prioritate în tratamentul acestei boli datorită istoricului de siguranță și, de asemenea, datorită dovezilor pentru reducerea riscului de evenimente cardiovasculare. S-au acumulat dovezi care indică faptul că metformina este sigură la persoanele cu boală renală cronică în stadiul 3 (CKD-3). Se estimează că aproximativ un sfert dintre persoanele cu CKD-3 și T2DM din Statele Unite (peste peste 1 milion) nu sunt eligibile pentru tratamentul cu metformină din cauza nivelurilor crescute de creatinină serică. Acest lucru ar putea fi depășit dacă ar putea fi dezvoltată o schemă, probabil bazată pe studii farmacocinetice, pentru a prescrie doze reduse de metformină la acești indivizi. Există, de asemenea, dovezi substanțiale din studiile epidemiologice care indică faptul că metformina nu numai că este sigură, ci poate aduce beneficii persoanelor cu insuficiență cardiacă (IC). Sunt necesare studii prospective, randomizate, privind utilizarea metforminei în IC pentru a investiga această posibilitate.
Introducere
Boala cardiovasculară (CV) este principala cauză de deces în SUA. Persoanele cu diabet zaharat de tip 2 (T2DM) au o creștere de 2 până la 4 ori a riscului CV mai mult decât explicat de factorii de risc convenționali (1). S-a estimat că până la 75% dintre persoanele cu T2DM vor muri de un eveniment CV (2). Legătura remarcabilă dintre T2DM și boala CV nu este pe deplin înțeleasă, dar rezistența la insulină joacă probabil un rol proeminent (3). Rezistența la insulină, bolile T2DM și CV cresc brusc odată cu vârsta (4; 5).
5000 de indivizi cu T2DM, pierderea intenționată în greutate de un grad modest a fost asociată cu o scădere cu 28% a mortalității prin CV (24). Efectul metforminei asupra motilității gastro-intestinale este în mare parte neexplorat.
Boli renale cronice
Rinichiul joacă un rol important în farmacocinetica metforminei. Absorbția unei doze orale de metformină este completă după
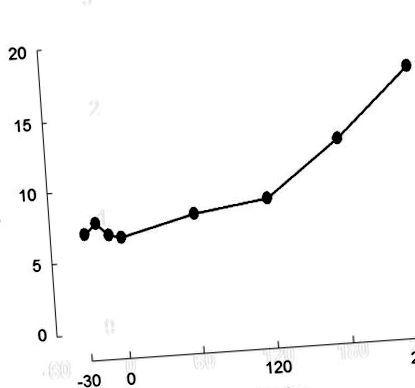
6 ore, dar o fracțiune semnificativă din doză este malabsorbită (16). Timpul de înjumătățire acută (t1/2) al metforminei în sânge este de 2–6 ore după o doză orală (16), dar cu terapia cronică, t1/2 este de 8–20 de ore din cauza unei cantități mari de medicamente intracelulare). Folosind o metodă bazată pe LC/MS/MS pentru măsurarea metforminei plasmatice, am efectuat recent studii preliminare privind farmacocinetica metforminei la persoanele cu T2DM. După cum se poate vedea în Figura 1, concentrațiile plasmatice de metformină cresc progresiv după o doză orală de preparat cu eliberare imediată timp de cel puțin 4 ore. Absorbția intestinală este facilitată de transportorii de cationi organici (OCT), care mediază și absorbția hepatică și renală (30). Absorbția intestinală este saturabilă (30); prin urmare, malabsorbția fracționată a medicamentului este mai mare la doze mai mari și redusă la doze mai mici (16). Metformina este excretată nemodificată de rinichi, iar clearance-ul său depinde de rata de filtrare glomerulară (GFR) (31). În plus față de excreția prin filtrare, există secreție tubulară activă de metformină (31).
Concentrațiile plasmatice ale metforminei înainte și timp de 4 ore după o doză de metformină dimineața (1000 mg) la un pacient care a luat în mod cronic 1000 mg de două ori pe zi (date nepublicate).
Boala renală cronică (CKD) este o afecțiune frecventă care crește dramatic odată cu vârsta. Există un declin universal sau aproape universal al GFR odată cu îmbătrânirea (32; 33); riscul de viață al stadiului 3 CKD (CKD-3, cu GFR 30-59 ml/min/1,73 m 2) este
60%, cu debutul apărut după vârsta de 70 de ani la jumătate din pacienți (34). Datele recente NHANES indică faptul că prevalența CKD-3 crește cu mai mult de un ordin de mărime după vârsta de 59 de ani (35). Trebuie subliniat faptul că senescența fiziologică a rinichiului apare chiar și cu îmbătrânirea sănătoasă (36). Într-un studiu realizat pe 1344 potențiali donatori de rinichi, volumul cortical a scăzut odată cu vârsta, atât la bărbați, cât și la femei, cu o rată accelerată de declin după vârsta de 50 de ani (37). Un studiu efectuat pe 1203 de donatori renali reali a constatat prevalența nefrosclerozei (glomeruloscleroză, atrofie tubulară, fibroză interstițială și arterioscleroză) asupra biopsiei renale pentru a crește liniar de la 2,7% la 18-29 de ani la 73% la 70 la 77 de ani (32 ).
CKD este asociat cu un risc cardiovascular crescut (38) și este o complicație frecventă a diabetului. Datele din Studiul Național de Examinare a Sănătății și Nutriției (NHANES) indică faptul că prevalența CKD-3 este
tabelul 1
Gama de concentrații serice de creatinină la persoanele cu CKD-3 (eGFR 30 până la 59 ml/min/1,73 m 2)
| 40 | 1.5–2.6 | 1.2–2.0 | 1.7-2.9 | 1.3–2.3 |
| 50 | 1.4–2.4 | 1.1–1.9 | 1.6–2.7 | 1.3–2.3 |
| 60 | 1.3–2.3 | 1.1–1.8 | 1.5–2.6 | 1.2–2.0 |
| 70 | 1.3–2.1 | 1.0-1.7 | 1.4–2.4 | 1.1–1.9 |
| 80 | 1.2–2.0 | 1.0-1.6 | 1.4–2.3 | 1.1–1.8 |
Pragurile de creatinină pentru utilizarea metforminei se bazează pe îngrijorarea cu privire la reținerea medicamentelor și rezultatul crescut al riscului de acidoză lactică, singurul risc potențial serios al tratamentului cu metformină. Majoritatea studiilor prospective, randomizate, au constatat o creștere a concentrațiilor de lactat din sânge la persoanele care iau metformină (48-50). Cu toate acestea, efectul este relativ modest (o creștere de 20-50%), cu concentrații medii de lactat în mod constant 100.000 pacienți-ani) meta-analiza a constatat că limita superioară pentru incidența acidozei lactice este de 4,3 și 5,4 cazuri la 100 000 pacienți-ani la pacienții T2DM tratați cu metformină și, respectiv, netratați (51). Mai mult, atunci când apare acidoză lactică la pacienții care iau metformină, aceasta tinde să fie de tipul A (hipoxemic), mai degrabă decât de tipul B (nehipoxemic) (52), sugerând că metformina nu este cauza acidozei lactice la acești indivizi. În pofida acestor dovezi liniștitoare, este bine cunoscută apariția acidozei lactice în cazul supradozajului cu metformină (53-57), confirmând că există un potențial de acidoză lactică atunci când există o acumulare marcată de metformină în timpul utilizării terapeutice.
Insuficienta cardiaca
Recent, a existat un interes considerabil asupra efectelor medicamentelor împotriva diabetului asupra riscului de IC. Un control glicemic slab este asociat cu riscul de spitalizare pentru IC (74), dar acest lucru nu indică neapărat o relație de cauzalitate. S-a exprimat o îngrijorare deosebită cu privire la utilizarea tiazolidindionelor din cauza retenției de sodiu care apare atunci când se administrează acești agenți (75). Terapia cu insulină este asociată cu o creștere de 140% a riscului relativ de a dezvolta IC (76). O creștere a riscului de IC cu terapia cu insulină ar putea fi cauzată de creșterea în greutate și creșterea corespunzătoare a tensiunii arteriale (77; 78) și/sau efectul antinatriuretic al insulinei (79).
S-a acumulat o literatură interesantă cu privire la relația dintre utilizarea metforminei și IC. Timp de mai mult de 10 ani după aprobarea sa în Statele Unite, HF a fost o contraindicație oficială pentru utilizarea metforminei. Utilizarea surprinzător de comună a metforminei la pacienții cu Medicare cu IC a fost atribuită lipsei de conștientizare a medicului cu privire la riscuri sau credinței că riscurile sunt supraevaluate (80); IC este considerat de mulți ca fiind cel puțin o contraindicație relativă la utilizarea metforminei (81; 82). Cu toate acestea, studiile concepute special pentru a investiga rezultatele la pacienții care iau metformină spun o poveste diferită. După cum sa menționat anterior, riscul de acidoză lactică nu pare a fi crescut prin utilizarea metforminei (51). Interesant este faptul că FDA, care a adăugat HF ca contraindicație la utilizarea metforminei la câțiva ani după ce a fost pusă la dispoziție pentru utilizare în Statele Unite (83), a concluzionat ulterior că metformina provoacă rareori, sau chiar vreodată, acidoză lactică (84). La sfârșitul anului 2006, din cauza datelor liniștitoare privind siguranța metforminei la pacienții cu IC, FDA a anulat contraindicația (85). Cu toate acestea, utilizarea acestuia este încă descurajată în prospect: (http://packageinserts.bms.com/pi/pi_glucophage.pdf).
Mai multe studii indică faptul că metformina poate fi de fapt benefică pentru pacienții cu IC. Noua incidență a IC este redusă la persoanele cu T2DM pe metformină (76; 86), iar atât decesul, cât și spitalizarea sunt mai scăzute la pacienții tratați cu metformină luată singură sau în asociere cu sulfoniluree comparativ cu cei aflați în tratament cu sulfoniluree (87). Un studiu retrospectiv de cohortă a 16.417 beneficiari Medicare cu diabet externat după spitalizare pentru IC a constatat o scădere cu 31% a mortalității la un an la persoanele tratate cu metformină comparativ cu cei care au fost tratați cu alți agenți (88). O analiză recentă a aproape 20.000 de persoane cu diabet în registrul REACH a demonstrat, de asemenea, o mortalitate cu IC cu 31% mai mică la persoanele care iau metformină în comparație cu cei care nu au luat-o (12). Astfel, 5 studii mari demonstrează în unanimitate o relație între tratamentul cu metformină și rezultatele îmbunătățite ale IC. Aceste observații epidemiologice sunt susținute de cercetări la animale. La șoarecii diabetici, protein kinaza miocardică activată AMP (AMPK) și funcția sistolică a VS sunt deprimate, iar terapia cronică cu metformină produce îmbunătățiri semnificative la ambele (89). Nu există studii prospective privind utilizarea metforminei în IC la om.
Mecanismul prin care metformina ar putea avea un efect favorabil asupra IC nu este cunoscut, dar poate fi legat de aportul redus de energie. Pierderea în greutate neintenționată, așa cum se întâmplă în cașexia cardiacă, are implicații prognostice adverse în IC de stadiu final (90). Cu toate acestea, am constatat într-o analiză suplimentară a datelor dintr-un studiu recent publicat (67) că pierderea în greutate este asociată cu o scădere a rigidității vasculare și abrogarea creșterii normale a rigidității LV legate de vârstă (B. Borlaug, rezultate nepublicate) . Într-adevăr, pierderea în greutate intenționată produsă de chirurgia bariatrică îmbunătățește de fapt funcția sistolică și diastolică, atât în prezența, cât și în absența IC (91). O pierdere în greutate mai modestă, similară cu cea produsă prin tratamentul cu metformină, poate avea, de asemenea, efecte favorabile. Într-un studiu realizat de anchetatori italieni, o intervenție de șase luni de viață a produs un
5% pierderea intenționată a greutății la 34 de persoane cu IC (30% dintre care au avut diabet) însoțită de o îmbunătățire semnificativă a clasei funcționale NYHA, EF ventricular stâng (VS) și calitatea vieții percepute (92).
Concluzii
Metformina este în prezent medicamentul ales pentru T2DM, iar supremația sa în tratamentul acestei afecțiuni nu se va schimba din cauza înregistrării sale excelente de siguranță și a beneficiilor CV unice. Îngrijorările cu privire la siguranța acestui agent din cauza riscului de acidoză lactică s-au dovedit a fi în mare parte nefondate; Aceste îngrijorări sunt probabil cauzate de anxietatea restantă legată de acidoză lactică cauzată de fenformină, care a fost utilizată în Statele Unite între 1959 și 1977. Ca urmare a unui risc perceput de acidoză lactică, a existat reticență în utilizarea metforminei la pacienții cu CKD. De fapt, există dovezi substanțiale că metformina ar putea fi utilizată în condiții de siguranță la persoanele cu valori CKD-3 și eGFR de până la 30 mL/min/1,73 m 2. Cu toate acestea, sunt necesare date farmacocinetice suplimentare pentru a dezvolta o schemă de dozare pentru persoanele cu CKD-3.
Există, de asemenea, dovezi considerabile că metformina poate fi utilizată în condiții de siguranță la pacienții cu IC. Studii epidemiologice mari demonstrează o asociere între tratamentul cu metformină și rezultatele îmbunătățite ale IC. Mecanismul pentru un efect salutar asupra metforminei asupra IC, dacă există, este necunoscut, dar posibilitățile includ îmbunătățirea funcției diastolice și scăderea muncii/cererii cardiace legate de scăderea activării simpatice. Sunt necesare studii prospective, randomizate, privind utilizarea metforminei la pacientul cu IC.
Mulțumiri
Sprijinit parțial de subvenții de la USPHS (RO1 HL67933 și UL1 RR 24150) și Fundația Mayo.
Barry A. Borlaug a fost consultant pentru Merck, Amgen, GlaxoSmithKline și Cardiokinetix. A primit sprijin de la Atcor Medical.
- Cum se evaluează activele pentru protecția pielii împotriva ruperii homeostaziei, poluării, îmbătrânirii, bolilor de piele ...?
- Beneficiile îmbătrânirii sănătoase
- Medicamentul pentru diabet de tip 2 Biguanidă Metformină Glucofag
- Greșeala de antrenament care cauzează îmbătrânirea
- Utilizarea terapeutică a metforminei în prevenirea diabetului și a diabetului