Clorura este secretată în lumenul intestinal prin acțiunea coordonată a cotransportorului basolateral Na +/2C1−/K + (NKCC1) și a regulatorului de conducere transmembranar al fibrozei chistice apicale (CFTR).
Termeni asociați:
- Bicarbonat de sodiu
- Ionii anorganici
- Secreție (proces)
- Proteină
- Mutaţie
- Ion de sodiu
- Potasiu
- Fibroză chistică
Descărcați în format PDF
Despre această pagină
Nutriție
Sherry M. Lewis,. Joseph J. Knapka, în The Laboratory Rat (Ediția a doua), 2006
CLORURĂ.
Clorura împreună cu sodiul și potasiul sunt responsabile pentru presiunea osmotică și echilibrul acido-bazic. Clorura este cel mai abundent anion din lichidul extracelular. Ca element electronegativ, Cl - este un agent oxidant. Pe lângă rolul său pasiv în echilibrul electrolitic, clorura este necesară pentru producerea acidului clorhidric gastric secretat din celulele parietale ale mucoasei gastrice din stomac (Groff și Gropper, 2000a). Această mucoasă eliberează și pepsinogen, care este activat de HC1 și este factorul intrinsec necesar pentru absorbția vitaminei B12 și producerea mucusului. Mucusul protejează organul de a fi digerat de HC1 și proteaze. HC1 acționează ca un bacteriocid care previne creșterea bacteriană a tractului gastro-intestinal (Berdanier, 1998). De asemenea, funcționează ca anion de schimb în celulele roșii din sânge pentru HCO-3, cunoscut sub numele de deplasarea clorurii. Acest proces permite transferul de CO2 derivat din țesuturi înapoi în plămâni (Groff și Gropper, 2000).
Necesarul estimat de clorură dietetică pentru șobolani este de 0,5 g/kg dietă NRC (1995). Deficitul de clorură la șobolani se dezvoltă lent datorită capacității lor de a conserva electrolitul prin reducerea semnificativă a excreției urinare în timpul epuizării. Semnele deficitului de clorură sunt creșterea slabă, eficiența scăzută a hranei, scăderea clorurii de sânge, reducerea excreției de clorură și creșterea nivelului de CO2 din sânge NRC (1995). Șobolanii hrăniți cu diete care conțin concentrații ridicate de clorură au crescut normal și au avut concentrații normale de clorură de mușchi și rinichi (Whitescarver și colab., 1986; Kaup și colab., 1991a, b). Cu toate acestea, șobolanii Sprague-Dawley hrăniți cu 15,6 g/kg de clorură dietetică aveau tensiune arterială crescută și rinichi măriți (Kaup și colab., 1991a, b). Kotchen și colab. (1983) au hrănit șobolani Dahl sensibili la sare 4,86 g/kg clorură dietetică, rezultând creșterea tensiunii arteriale.
Atmosfere naturale: coroziune
1.2 Cloruri
Clorurile sunt compuși corozivi în special pentru multe metale. Solubilitatea în apă a multor cloruri metalice este relativ mare și, deoarece clorura este monovalentă, tinde să stabilizeze solurile suspensoidale, împiedicând astfel dezvoltarea unui strat de produs de protecție împotriva coroziunii. Clorurile sunt prezente în apa de mare într-o concentrație ridicată și tind să fie antrenate în aer prin acțiunea vântului asupra apei, provocând surf și spray. Aceste cloruri încep ca picături de apă de mare, dar odată cu trecerea timpului, acestea se usucă până la particule solide fine. Ca urmare, regiunile apropiate de ocean tind să fie foarte corozive pentru majoritatea metalelor, iar corozivitatea este proporțională cu apropierea de surf. Oțelurile și, într-o măsură mai mică, aliajele de cupru, sunt afectate de clorură, în timp ce materialele de zinc și nichel sunt mai puțin afectate. Regiunile foarte apropiate de suprafață vor avea un timp de umezeală crescut, precum și rate de depunere ridicate de clorură.
Depunerea clorurii poate fi măsurată printr-o varietate de tehnici, dar metoda lumânării umede, ASTM G140, a fost adoptată ca standard. Această metodă utilizează un tub înfășurat cu tifon menținut umed cu apă pentru a captura clorurile ude sau uscate. După o expunere de 30 de zile, dispozitivul este recuperat și conținutul de clorură este măsurat prin analize chimice. Trebuie remarcat faptul că valorile obținute din lumânarea cu clorură nu corespund neapărat măsurătorilor obținute din alte geometrii de colectare.
Clorurile pot fi găsite și în expuneri la atmosferă lângă autostrăzi și drumuri unde clorura de sodiu și/sau calciu este folosită pentru a topi zăpada și gheața în timpul iernii. În aceste cazuri, metoda de transport este mai degrabă prin stropire decât depunere uscată. Depunerea de sare rutieră a contribuit major la coroziunea și defectarea componentelor auto de mulți ani.
ISO a adoptat o clasificare standard pentru depunerea clorurii. Aceste valori sunt prezentate în tabelul 2. Acestea se bazează pe măsurători de lumânări umede și sunt utile pentru evaluarea siturilor aflate la mai puțin de 1 km de o sursă de apă de mare.
Masa 2. Clase de depunere clorură ISO și dioxid de sulf, bazate pe ISO 9223.
| S0 | 300 | P3 | > 81 | > 91 |
Viteza de depunere a clorurilor pe baza ionului clorură; Rata de depunere a SO2 pe baza sulfului total ca SO2; Concentrația de SO2 bazată pe SO2 la 25 ° C în aer la 1atm.
Biologia moleculară și celulară a durerii
5 Reglarea concentrațiilor de anioni intracelulari
Reglarea clorurii depinde de coordonarea mai multor procese (Fig. 2). Anumite canale de scurgere de clorură au fost sugerate pentru a reduce concentrația de clorură intracelulară acționând ca supape unidirecționale. Această idee provine din observația că canalele de clorură precum ClC-2 (gena clcn2) sunt mai permeabile la clorura care iese din celulă decât la clorura care intră în celulă. 35 Indiferent de această permeabilitate diferențială, denumită rectificare, direcția fluxului de clorură depinde în continuare de forța motrice a clorurii. Aceasta înseamnă că clorura va avea rareori posibilitatea de a ieși din celulă prin intermediul ClC-2, deoarece forța motrice a clorurii este aproape întotdeauna în direcția opusă. Deoarece „supapa” este imperfectă, canalele ClC-2 lasă clorura să se scurgă în celulă. 36
Eșecul canalelor de a lăsa clorura să iasă din celulă evidențiază nevoia de diferite mecanisme de transport al ionilor care pot deplasa clorura împotriva gradientului său. 37 Cotransportatorii sau simporterii deplasează două sau mai multe specii de ioni în aceeași direcție de-a lungul membranei celulare; clorura se poate deplasa împotriva gradientului său prin salvarea unui alt ion care se deplasează în jos pe gradientul său. Schimbătoarele, sau antiporters, fac efectiv același lucru, dar prin cuplarea mișcării speciilor de ioni care curg în direcții opuse peste membrană. Principalul extruder de clorură din neuroni este cotransportorul 2 de clorură de potasiu (KCC2) (gena slc12a5). KCC2 permite ionilor de potasiu clorura piggyback care curg în jos gradientul lor și în afara celulei. Procesul este electroneutral datorită stoichiometriei 1: 1 a clorurii și potasiului. Procesul nu este activ în măsura în care nu implică direct hidroliza ATP (și, prin urmare, nu ar trebui denumit pompare); în schimb, procesul este activ în al doilea rând, deoarece KCC2 se bazează pe gradientul de potasiu menținut de ATPaza sodiu - potasiu, care pompează potasiu în celulă.
După cum sa menționat deja, bicarbonatul curge prin receptorii GABAA și glicină activi. Probabilitatea ca un eflux de bicarbonat să provoace acumularea extracelulară este scăzută, având în vedere difuzia relativ nerestricționată a bicarbonatului în spațiul extracelular, dar efluxul de bicarbonat poate epuiza nivelurile de bicarbonat intracelular și poate provoca o scădere a pH-ului. 49 Totuși, aceste tendințe nu apar în condiții normale, deoarece bicarbonatul intracelular este completat prin conversia dioxidului de carbon și a apei în bicarbonat și protoni de către enzima anhidrază carbonică; ca gaz, dioxidul de carbon se difuzează liber pe membrana celulară. Bicarbonatul intracelular poate fi epuizat (iar efluxul său astfel redus) prin blocarea anhidrazei carbonice de către acetazolamidă, 32 care poate avea de fapt efecte analgezice (Secțiunea 9). Reglarea pH-ului implică alte reacții chimice și mecanisme de transport, iar bicarbonatul în sine poate fi transportat pe membrana celulară în schimbul clorurii. 50
Roluri multiple ale KCC2 în creierul în curs de dezvoltare
53.2.1 Proteinele CCC sunt codificate de familia de gene SLC12
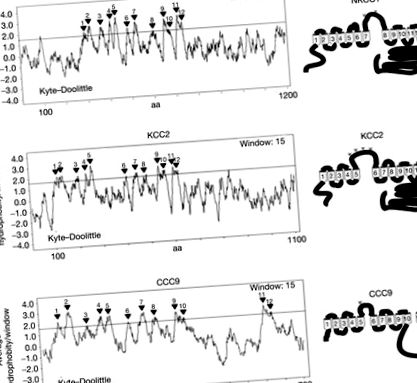
Proteinele CCC sunt codificate de gene corespunzătoare care constituie familia genei purtătorului solut 12 (SLC12) (Tabelul 53.1) cu nouă membri (Gamba, 2005). Se prevede că toți membrii CCC (cu excepția poate CCC9) vor avea 12 domenii transmembranare (TM) (Figura 53.3); acest lucru a fost confirmat experimental până acum numai pentru Na + –K + –2Cl - cotransporter 1 (NKCC1) (Gerelsaikhan și Turner, 2000; Gerelsaikhan și colab., 2006).
Tabelul 53.1. Membrii familiei CCC
| NKCC2 | SLC12A1 | Na +, K +, Cl - | 1099/178 | Gamba și colab. (1994) și Payne și Forbush (1994) |
| NKCC1 | SLC12A2 | Na +, K +, Cl - | 1191/262 | Delpire și colab. (1994) și Xu și colab. (1994) |
| NCC | SLC12A3 | Na +, Cl - | 1023/143 | Gamba și colab. (1993) |
| KCC1 | SLC12A4 | K +, Cl - | 1085/123 | Gillen și colab. (1996) |
| KCC2 | SLC12A5 | K + , Cl - | 1116/104 | Payne și colab. (1996) |
| KCC3 | SLC12A6 | K +, Cl - | 1150/190 | Hiki și colab. (1999), Mount și colab. (1999) și Race și colab. (1999) |
| KCC4 | SLC12A7 | K +, Cl - | 1083/123 | Muntele și colab. (1999) |
| CCC9 | SLC12A8 | Necunoscut | 714/44 | Hewett și colab. (2002) |
| CIP | SLC12A9 | Necunoscut | 915/44 | Caron și colab. (2000) |
Figura 53.3. Plante de hidropatie pentru proteinele NKCC1, KCC2 și CCC9. O analiză de hidropatie Kyte - Doolittle (în stânga, folosind o fereastră de 15 aa (Kyte și Doolittle, 1982)) sugerează domenii 12-TM pentru NKCC1 (a), KCC2 (b) și posibil și pentru CCC9 (c). Modele schematice ale proteinelor NKCC1 (a), KCC2 (b) și CCC9 (c) cu 12 segmente TM sunt prezentate în dreapta.
Familia CCC este subdivizată în trei ramuri (Figura 53.4). Prima ramură include Na + -dependent K + –Cl - cotransportatori NKCC1 și NKCC2, precum și un Na + -dependent Cl - cotransportator NCC. Aceste proteine mediază transportul electroneutral cu Na + Cl - transportat, indiferent de utilizarea lor a K +, și partajează
55% omologie în secvențe de aminoacizi. A doua ramură include patru K + dependenți de Cl - cotransportatori KCC1, KCC2, KCC3 și KCC4, care mediază Cl + cuplat electroneutral K + - transport și partajare
70% identitate de aminoacizi. În schimb, membrii acestor două ramuri CCC sunt doar aproximativ 25% omologi între ei. A treia ramură CCC este reprezentată de doi membri CCC orfani - cation - cotransportor clorură 9 (CCC9) și proteina 1 care interacționează CCC (CIP1), care demonstrează doar
20-25% identitate cu alte CCC (Gamba, 2005).
Figura 53.4. Arborele filogenetic al familiei CCC. Familia CCC (umbrită în verde) este în prezent împărțită în trei ramuri reprezentând membrii N (K) CC, KCC și orfani. Outgroup este reprezentat de trei membri ai familiei SLC7. Analiza arborelui filogenetic a fost efectuată folosind programul ClustalW Tree (Biology Workbench). Valorile bootstrap (un procent din frecvența cu care fiecare ramură este prezentată în toți copacii eșantionați) sunt indicate lângă ramuri. Lungimea ramurii corespunde unui număr mediu de substituții de aminoacizi per sit în secvențele aliniate. Bara de scară corespunde la 0,1 substituții pe site.
ANALIZA CLINICĂ | Electroliti în probe fiziologice
Semnificația și interpretarea rezultatelor
Măsurarea concentrației de clorură a serului (Tabelul 1) este semnificativă în cazul concentrației normale de apă a probei. În hiperlipemie sau hiperproteinemie, „grupat” apare deoarece o creștere de, de exemplu, 10% în compartimentul care conține macromolecule scade concentrația de cloruri cu 10%. O schimbare de 10% este deosebit de importantă atunci când intervalul de referință este relativ mic. În cazul clorurii, limita superioară a intervalului de referință diferă de limita inferioară cu 11% (vezi Sodiu de mai sus). Prin urmare, concentrația de clorură a serului trebuie reajustată (vezi Semnificația și interpretarea rezultatelor de mai sus) atunci când concentrația de apă este anormală pentru a fi comparabilă cu intervalul de referință.
Decalajul anionic (AG) (mmol l -1) se calculează ca
unde [Na +] este concentrația de sodiu în ser (mmol l -1), [Cl -] este concentrația de clorură în ser (mmol l -1) și [HCO3 -] este concentrația de carbonat de hidrogen în ser (mmol l −1).
Intervalul de referință al decalajului anionic este de +8 la +16 mmol l −1. Decalajul se datorează faptului că suma cationilor (de exemplu, K +, Ca 2+), care nu este luată în considerare, este mai mică decât suma anionilor, care sunt excluși din calcul (proteine, acizi organici) . Decalajul anionic este mărit în cazurile de cetoacidoză diabetică, lactatacidoză și anumite intoxicații cu salicilat, metanol (formiat), etanol (lactat) și etilen glicol (oxalat, glicolat, glioxilat). Decalajul anionic este redus sau chiar devine negativ în cazul concentrațiilor mari de bromură, mai ales dacă concentrația de clorură este determinată printr-o metodă care este mai sensibilă la bromură decât la clorură.
Concentrația de sodiu și concentrația de clorură se modifică în general în aceeași direcție și în aceeași măsură, în timp ce clorura și hidrogenocarbonatul se schimbă reciproc (Tabelul 4).
Tabelul 4. Tulburări ale echilibrului clorurii
| 1 | Hipocloremie | |
| 1.1 | Cauză: aport insuficient de clorură | |
| 1.2 | Cauză: Pierderea clorurii | |
| Exemple: | Vărsături | |
| Spălare gastrică | ||
| Alcaloza metabolică | ||
| Acidoza respiratorie | ||
| Diuretice | ||
| 1.3 | Cauză: Deshidratare hipotonică (vezi Sodiu) | |
| 1.4 | Cauză: Hiperhidratare hipotonică (vezi Sodiu) | |
| 2 | Hipercloremie | |
| 2.1 | Cauză: aport excesiv de clorură | |
| Exemple: | Infuzie de cantități mari de clorură | |
| Ureterosigmoidostomie | ||
| 2.2 | Cauză: Eliminarea scăzută a clorurii | |
| (datorită pierderii de carbonat de hidrogen) | ||
| Exemple: | Diaree | |
| Fistula pancreatică | ||
| Acidoza tubulară renală | ||
| Hipoaldosteronism cu acidoză | ||
| 2.3 | Cauză: Deshidratare hipertonică (vezi Sodiu) | |
| 2.4 | Cauză: Hiperhidratare hipertonică (vezi sodiu) | |
Modificat din Külpmann WR, Stummvoll HK și Lehmann P (1996) Electroliti: aspecte clinice și de laborator. New York: Springer.
Excreția urinară de clorură (Tabelul 3) seamănă de obicei cu excreția de sodiu. În cazul alcalozei metabolice datorate pierderii extrarenale de clorură, excreția de clorură este -1. Dacă alcaloza metabolică este cauzată de excesul de mineralocorticoizi, excreția de clorură nu este afectată și> 10 mmol d -1 .
Diversitatea și funcțiile receptorilor GABA: un omagiu adus lui Hanns Möhler, partea B.
3.2.2 Senzori de clorură codați genetic
Imagistica cu cloruri nu poate detecta nici inhibiția de manevrare, nici fluxul de bicarbonat și, prin urmare, permite doar afirmații indirecte asupra impactului unui semnal GABAergic asupra excitabilității neuronului postsinaptic.
Parametrii biochimici în studiile toxicologice în Africa
23.5.3 Clorură
Anatomia și fiziologia intestinului subțire și gros
Secreţie
În ileon și colon, schimbătorii NHE și Cl -/HCO3 - din membranele apicale produc absorbția netă electroneutrală de NaCl și secreția de H + HCO3 -. Acțiunea duală a proteinelor DRA (SLC26A3) și PAT1 (SLC26A6) produce o secreție electroneutrală de HCO3 - și absorbție de Cl -. Mecanismele independente de clorură ale secreției de bicarbonat includ secreția dependentă de AMPc și secreția de HCO3 asociată cu absorbția acizilor grași cu lanț scurt. 84
- Agent Antiobezitate - o prezentare generală Subiecte ScienceDirect
- Apiterapie - o prezentare generală a subiectelor ScienceDirect
- Beta-lactoglobulină - o prezentare generală a subiectelor ScienceDirect
- Boala tractului biliar - o prezentare generală Subiecte ScienceDirect
- Arginina - o prezentare generală Subiecte ScienceDirect