Abstract
Ratele de secreție de insulină sunt mai mari după glucoza orală decât după administrarea parenterală a unei încărcături echivalente de glucoză. Acest răspuns secretor al celulelor β crescute la o încărcare de glucoză pe cale orală rezultă din eliberarea în principal a doi hormoni intestinali: polipeptidă inhibitoare gastrică (GIP) și peptidă de tip glucagon-1, care potențează secreția de insulină indusă de glucoză. Datorită acțiunii lor insulinotrope, secreția lor anormală poate fi implicată în patogeneza hiperinsulinemiei obezității la copii. În acest studiu, am utilizat clema hiperglicemiantă cu o mică încărcătură orală de glucoză pentru a evalua efectul obezității infantile asupra răspunsului GIP la șapte copii slabi prepubertali și 11 copii obezi prepubertali și la 14 adolescenți slabi și 10 adolescenți obezi. Glucoza plasmatică a fost crescută acut la 11 mM prin infuzarea i.v. glucoză și menținută la această concentrație timp de 180 min. Fiecare subiect a ingerat glucoză orală (30 g) la 120 min, iar perfuzia de glucoză a fost ajustată pentru a menține platoul de glucoză plasmatică. Concentrațiile de insulină bazală și peptide C și ratele de secreție de insulină (calculate prin metoda deconvoluției) au fost semnificativ mai mari la copiii obezi comparativ cu copiii slabi (p
Este bine cunoscut faptul că ingestia de glucoză generează o creștere mai mare a concentrațiilor plasmatice de insulină în circulație în comparație cu i.v. sarcină de glucoză (1, 2). Această creștere a secreției de insulină este cauzată în principal de eliberarea de hormoni intestinali care acționează asupra celulelor β pentru a potența secreția de insulină indusă de glucoză (3). Acest efect, cunoscut sub numele de efect incretin, este atribuit în principal GIP produs de celulele K ale duodenului și jejunului (4-8) și GLP1 (7-36 amide) din celulele L ale ileonului 9 -15).
Semnificația efectului incretin decurge din importanța centrală a insulinei și a tulburărilor în metabolismul insulinei în stările patologice ale obezității și ale diabetului de tip 2. Hiperinsulinemia, cea mai frecventă alterare biochimică a obezității, este o consecință a secreției crescute de insulină, precum și a scăderii extracției hepatice fracționate a insulinei (16). Secreția crescută de insulină, în special după mese, a fost legată în mai multe modele animale de obezitate de o axă enteroinsulară hiperactivă (17, 18). De exemplu, șoarecele ob/ob mutant prezintă o hiperplazie generalizată a celulei endocrine a intestinului subțire (17), iar concentrațiile GIP intestinale și concentrațiile circulante ale hormonului sunt crescute (19). Aceste anomalii pot fi secundare pentru a crește aportul de energie, mai degrabă decât primare. Mai mult, șoarecele ob/ob pare a fi deosebit de sensibil la efectul insulinotrop al GIP (20). Rezultate similare s-au găsit la șoareci db/db (21), dar nu și la șobolani grași Zucker (fa/fa) (22).
Cu toate acestea, nu este sigur dacă astfel de modele obeze de rozătoare pot defini rolul axei entero-insulare în funcția dezordonată a celulelor β în obezitatea umană. Deși unele studii au observat concentrații crescute ale GIP la jeun la subiecți adulți obezi (3) și răspunsuri exagerate ale GIP la glucoza orală sau la o masă lichidă (23-26), alte studii nu au găsit o creștere a răspunsurilor GIP stimulate de nutrienți la adulți subiecți obezi (27, 28). Diferențele de glucoză sau mărimea și compoziția meselor ar fi putut contribui la variabilitatea răspunsurilor GIP în aceste studii. Este de remarcat faptul că integritatea răspunsului GIP nu a fost niciodată examinată la obezitatea infantilă, care este în mod clar asociată cu dereglarea funcției celulelor β la începutul dezvoltării sale.
În studiul actual, am folosit clema hiperglicemiantă cu o cantitate mică de glucoză orală pentru a studia contribuția GIP la secreția de insulină indusă de glucoză în obezitatea infantilă (2, 29). Această tehnică permite separarea efectelor hiperglicemiei și a factorilor insulinotropi intestinali asupra răspunsului celulelor β.
GIP stimulează secreția de insulină numai în prezența unei hiperglicemii ușoare până la moderate (29). Într-adevăr, GIP secretat ca răspuns doar la ingestia de grăsime nu stimulează secreția de insulină, servind drept protecție împotriva secreției de insulină și a hipoglicemiei inadecvate (22). Deoarece acțiunea insulinotropă GIP este dependentă de glucoză, cu efecte mai mari care apar la concentrații mai mari de glucoză, am ridicat glucoza plasmatică la concentrații hiperglicemiante (11 mM) pentru a putea studia efectele potențiale ale acesteia asupra secreției de insulină la copiii slabi și obezi.
METODE
Subiecte.
Au fost studiate patru grupuri de subiecți, iar caracteristicile lor clinice și biochimice sunt indicate în Tabelul 1. Copiii prepubertali au fost clinic Tanner stadiul I, fără dovezi biochimice de pubertate. Adolescenții au fost asortați pentru etapa Tanner și au variat între III și IV. Probele de plasmă pentru măsurarea estradiolului și testosteronului au fost, de asemenea, luate ca markeri biochimici ai dezvoltării pubertare (Tabelul 1).
Așa cum se arată în Tabelul 1, greutatea (în kilograme) și IMC (kilograme pe metru pătrat) au fost semnificativ mai mari la subiecții obezi. IGF-I a fost cel mai mare la adolescenții slabi comparativ cu toate celelalte grupuri (p 95 percentilă specifică vârstei și sexului (pe baza curbelor percentilale pentru fete și băieți albi, calculată din primul sondaj național de examinare a sănătății și nutriției din 1971-1974) (30). Procentul greutății ideale pentru înălțime a fost> 150% pentru copiii obezi și 6). Această analiză nu prezintă reactivitate la gastrină, glucagon, secretină, colecistochinină, pancreozimină, motilină sau VIP și nu are reactivitate încrucișată cu GLP1. Variabilitatea intra și interanaliză a fost de 6,2%, respectiv 7,8%.
Determinarea ISR.
ISR-urile au fost calculate prin deconvoluția concentrațiilor plasmatice ale peptidei C folosind un model cu două compartimente de cinetică a peptidei C așa cum s-a descris anterior (31). Am utilizat parametri cinetici standard care descriu clearance-ul peptidei C pe baza a 200 curbe individuale de descompunere a peptidei C biosintetice la adulți normali, obezi și diabetici (32). Acești parametri explică diferențele în funcție de vârstă, sex și suprafața corpului. Suprafața sub ratele de secreție de insulină și concentrațiile de insulină au fost calculate de la 0 la 120 de minute și de la 120 la 180 de minute a clemei hiperglicemice, care reprezintă atât glucoza, cât și efectele incretinei. Raportul dintre aceste două zone a furnizat o măsură indirectă a clearance-ului endogen al insulinei înainte și după încărcarea orală de glucoză (32, 33).
analize statistice.
Toate valorile sunt prezentate ca medie ± SEM. Analizele statistice au fost efectuate utilizând ANOVA bidirecțional, cu un design de măsură repetată și prin împerechere cu două cozi t Test. Coeficienții de corelație Pearson au fost calculați pentru a evalua gradul de asociere între variabile. ASC au fost determinate utilizând regula trapezoidală între 0 și 120 min și între 120 și 180 min din studiu. Diferențele au fost considerate semnificative statistic dacă corespund p ≤ 0,05. Toate analizele statistice au fost efectuate utilizând programul de analiză computerizată SAS (versiunea 6; Institutul SAS, Cary, NC).
REZULTATE
Concentrațiile bazale și stimulate de insulină și peptide C și ISR.
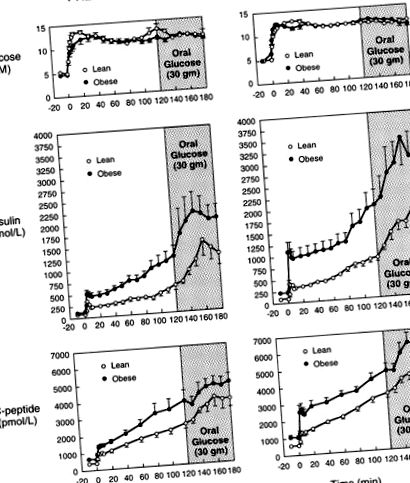
Figura 1 ilustrează concentrațiile plasmatice de glucoză, insulină și peptide C în timpul clemei hiperglicemice cu glucoză orală în preadolescenții și adolescenții slabi și obezi. În toate grupurile, glucoza plasmatică a fost crescută și menținută la 11 mM printr-o perfuzie variabilă de 20% glucoză. Acest platou hiperglicemic a fost menținut chiar și după ingestia a 30 g de glucoză orală la 120 de minute de clemă.
Concentrațiile plasmatice ale glucozei, insulinei și peptidelor C în timpul studiilor hiperglicemice și ale glucozei orale.
Concentrațiile plasmatice bazale de insulină și C-peptide au fost mai mari la grupurile obeze decât la copiii slabi (p Figura 2
Ratele de secreție de insulină în timpul studiilor hiperglicemice și de glucoză orală.
Zona sub curbele de secreție de insulină înainte și după încărcarea orală de glucoză la copii slabi și obezi.
Pentru a determina dacă clearance-ul insulinei a fost diferit între copiii slabi și obezi, am calculat raportul dintre ASC a secreției de insulină și ASC a concentrației periferice de insulină înainte și după încărcarea orală de glucoză. Acest raport, care oferă o măsură indirectă a clearance-ului insulinei endogene, a fost ușor, dar nu semnificativ mai mic la preadolescenții și adolescenții obezi (10,7 ± 1,1 și respectiv 10,4 ± 1,1 mL/min) decât la preadolescenții și adolescenții slabi (11,5 ± 0,7 și 12,9 ± 0,5 ml/min, respectiv). După ingestia unei mici cantități de glucoză, clearance-ul insulinei a scăzut semnificativ atât la copiii obezi (6,1 ± 0,8 și respectiv 6,8 ± 0,8 ml/min), cât și la copii slabi (6,6 ± 0,8 și 7,9 ± 0,7 ml/min, respectiv) copii, atingând valori care erau practic identice în toate cele patru grupuri.
Răspuns GIP.
Concentrațiile plasmatice GIP plasmatice circulante au fost similare la momentul inițial la copiii obezi și slabi și au rămas neschimbate în primele 120 de minute ale clemei hiperglicemiante (Fig. 4). În contrast, în toate cele patru grupuri, concentrațiile plasmatice de GIP au crescut brusc după ingestia de glucoză orală (p Figura 4
Modificări ale concentrațiilor plasmatice de GIP în timpul studiilor cu clemă hiperglicemică și glucoză orală.
DISCUŢIE
Efectele insulinotrope GIP și GLP1 sunt dependente de glucoză, cu efecte mai mari care apar la concentrații mai mari de glucoză (29). Prin urmare, starea hiperglicemiantă utilizată în prezentul studiu ne-a permis în mod clar să examinăm efectele potențiale ale acestui factor intestinal asupra secreției de insulină. La concentrații euglicemice, GIP nu are efect asupra celulei β și stimulează secreția de insulină atunci când concentrația plasmatică de glucoză depășește 110 mg/dL (6 mM) (22). De fapt, s-a sugerat că GIP ar trebui redenumit polipeptidă insulinotropă dependentă de glucoză (29). Deși în condițiile utilizate aici glucoza a fost blocată la concentrații mai mari, avem dovezi că unii copii obezi prezintă hiperglicemie ușoară postprandială, chiar dacă toleranța lor la carbohidrați nu este afectată (Sonia Caprio, comunicare personală).
Este clar că GIP singur nu poate explica efectul complet de incretină asociat în mod normal cu o masă mixtă și că efectele suplimentare sunt cauzate de efectele insulinotrope ale GLP1 (7-36) (29). Trebuie subliniat faptul că, pe o bază molară, creșterea GIP după încărcarea orală de glucoză (75 g) sau un mic dejun standard este de aproape 4 ori mai mare decât cea a GLP1 (36). Din concentrațiile plasmatice mai mari de GIP în stările bazale și postprandiale, s-a sugerat că fiziologic GIP este hormonul incretin mai important cantitativ (37).
Creșterea semnificativă a concentrațiilor GIP după doar ingestia a 30 g de glucoză (120 cal) a mediat fără îndoială stimularea acută a secreției de insulină observată atât la copiii slabi, cât și la cei obezi. Cu toate acestea, nu putem exclude faptul că alte incretine, în special GLP1, au fost eliberate și în condițiile actuale, făcând astfel sinergie cu GIP pentru a crește secreția de insulină. Această posibilitate rămâne de explorat.
În studiul de față, am folosit un model cu două compartimente pentru a estima ISR-urile din concentrațiile periferice de peptide C (31). Folosind această analiză cantitativă, am găsit concentrații crescute de insulină bazală și răspunsuri de insulină plasmatică în prima și a doua fază în pubertatea slabă contra copii prepubertali slabi care ar putea fi contabilizați de ISR crescut. Mai mult, ISR-urile în aceste condiții au fost mult exagerate de prezența și severitatea obezității. Într-adevăr, s-a găsit o relație liniară foarte semnificativă între bazală (r = 0,56, p 16). Spre deosebire de datele raportate la adulții obezi (16), clearance-ul insulinei a fost similar la copiii slabi și obezi și nu s-a găsit nicio relație între clearance-ul insulinei și IMC. Studiul nostru sugerează că secreția crescută de insulină este cel mai important factor în patogeneza obezității hiperesulinemice la copil, unde clearance-ul insulinei pare să fie mai puțin afectat. Trebuie remarcat faptul că factorii cinetici ai peptidei C utilizați pentru calcularea ISR s-au bazat pe date din populațiile adulte, iar datele bazate pe curbele de descompunere a peptidei C dintr-o populație pediatrică ar fi ideale. Din câte știm, însă, nu există astfel de date. Peptida C biosintetică nu este disponibilă în prezent pentru efectuarea acestor studii.
În concluzie, am constatat că sub condiția de hiperglicemie stabilă, ingestia unei cantități mici de glucoză a provocat răspunsuri GIP echivalente atât la adolescenții slabi, cât și la cei obezi. Cu toate acestea, în ciuda concentrațiilor similare de GIP, secreția de insulină a fost accentuată semnificativ la adolescenții obezi. Astfel, în obezitatea juvenilă, stimularea excesivă a celulelor β poate fi independentă de eliberarea crescută a hormonilor intestinali, cum ar fi GIP.
- Sângerarea a îmbunătățit secreția și sensibilitatea insulinei într-un studiu recent
- Sângerarea ameliorează sensibilitatea și secreția insulinei în paralel cu reducerea fierului hepatic în
- O recenzie a diverticulului gastric World Journal of Emergency Surgery Text integral
- Un extract de afine bogat în polifenoli protejează împotriva obezității induse de dietă, rezistenței la insulină și
- Benjamin Bikman - Valoarea consumului scăzut de carbohidrați; Glucagon în sus, insulină în jos