Editorii noștri vor examina ceea ce ați trimis și vor stabili dacă să revizuiți articolul.
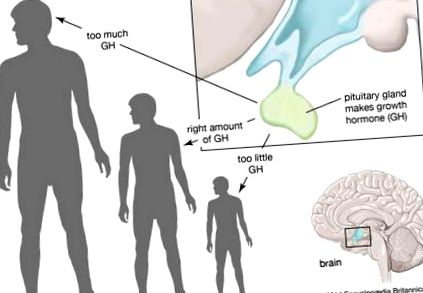
Hormonul de creștere (GH), numit si somatotropină sau hormon de creștere uman, hormon peptidic secretat de lobul anterior al hipofizei. Stimulează în esență toate țesuturile corpului, inclusiv osul. GH este sintetizat și secretat de celulele pituitare anterioare numite somatotrofe, care eliberează între unul și două miligrame de hormon în fiecare zi. GH este vital pentru creșterea fizică normală la copii; nivelurile sale cresc treptat în timpul copilăriei și vârf în timpul creșterii care apare în pubertate.
În termeni biochimici, GH stimulează sinteza proteinelor și crește descompunerea grăsimilor pentru a furniza energia necesară creșterii țesuturilor. De asemenea, antagonizează (se opune) acțiunii insulinei. GH poate acționa direct asupra țesuturilor, dar o mare parte din efectul său este mediat de stimularea ficatului și a altor țesuturi pentru a produce și elibera factori de creștere asemănători insulinei, în primul rând factorul de creștere asemănător insulinei 1 (IGF-1; numit anterior somatomedină). Termenul de factor de creștere asemănător insulinei este derivat din capacitatea concentrațiilor ridicate ale acestor factori de a imita acțiunea insulinei, deși acțiunea lor principală este de a stimula creșterea. Concentrațiile serice de IGF-1 cresc progresiv cu vârsta la copii, cu o creștere accelerată în momentul creșterii pubertare. După pubertate, concentrațiile de IGF-1 scad treptat odată cu vârsta, la fel și concentrațiile de GH.
Secreția de GH este stimulată de hormonul de eliberare a hormonului de creștere (GHRH) și este inhibată de somatostatină. În plus, secreția de GH este pulsabilă, cu creșteri ale secreției care apar după apariția somnului profund, care sunt deosebit de proeminente în momentul pubertății. La subiecții normali, secreția de GH crește ca răspuns la scăderea aportului de alimente și la stresuri fiziologice și scade ca răspuns la ingestia de alimente. Cu toate acestea, unii indivizi sunt afectați de anomalii ale secreției de GH, care implică fie deficiență, fie supraabundență a hormonului.
Deficitul hormonului de creștere
Deficitul de GH este una dintre numeroasele cauze ale staturii scurte și a nanismului. Rezultă în primul rând din afectarea hipotalamusului sau a glandei pituitare în timpul dezvoltării fetale (deficit congenital de GH) sau nașterea ulterioară (deficit de GH dobândit). Deficitul de GH poate fi, de asemenea, cauzat de mutații ale genelor care reglează sinteza și secreția acestuia. Genele afectate includ PIT-1 (factor de transcripție specific pituitar-1) și POUF-1 (profetul PIT-1). Mutațiile acestor gene pot provoca, de asemenea, scăderea sintezei și secreției altor hormoni hipofizari. În unele cazuri, deficitul de GH este rezultatul deficitului de GHRH, caz în care secreția de GH poate fi stimulată prin perfuzia de GHRH. În alte cazuri, somatotrofii înșiși sunt incapabili să producă GH sau hormonul în sine este anormal din punct de vedere structural și are puțină activitate de promovare a creșterii. În plus, statura scurtă și deficitul de GH se găsesc adesea la copiii diagnosticați cu nanism psihosocial, care rezultă din lipsa emoțională severă. Atunci când copiii cu această tulburare sunt eliminați din mediul stresant și neîngrijitor, funcția lor endocrină și rata de creștere se normalizează.
Copiii cu deficit de GH izolat au dimensiuni normale la naștere, dar întârzierea creșterii devine evidentă în primii doi ani de viață. Radiografiile (filmele cu raze X) ale epifizelor (capetele în creștere) ale oaselor prezintă o întârziere a creșterii în raport cu vârsta cronologică a pacientului. Deși pubertatea este adesea întârziată, fertilitatea și nașterea copiilor normali sunt posibile la femeile afectate.
Deficitul de GH este cel mai adesea tratat cu injecții de GH. Cu toate acestea, timp de decenii, disponibilitatea hormonului a fost limitată, deoarece a fost obținută exclusiv din pituitari umane de cadavru. În 1985, utilizarea GH naturală a fost oprită în Statele Unite și alte câteva țări din cauza posibilității ca hormonul să fie contaminat cu un tip de agent patogen cunoscut sub numele de prion, care provoacă o afecțiune fatală numită boala Creutzfeldt-Jakob. În același an, prin intermediul tehnologiei ADN recombinant, oamenii de știință au reușit să producă o formă umană biosintetică, pe care au numit-o somatrem, asigurând astfel o aprovizionare practic nelimitată a acestei substanțe odinioară prețioase.
Copiii cu deficit de GH răspund bine la injecțiile de GH recombinant, atingând adesea înălțimea aproape normală. Cu toate acestea, unii copii, în primul rând cei cu incapacitatea ereditară de a sintetiza GH, dezvoltă anticorpi ca răspuns la injecțiile cu hormon. Copiii cu statură scurtă care nu sunt asociați cu deficit de GH pot crește, de asemenea, ca răspuns la injecțiile hormonale, deși sunt deseori necesare doze mari.
O formă rară de statură scurtă este cauzată de o insensibilitate moștenită la acțiunea GH. Această tulburare este cunoscută sub numele de nanism Laron și se caracterizează prin receptori anormali ai GH, rezultând o producție scăzută de IGF-1 stimulată de GH și o creștere slabă. Concentrațiile serice de GH sunt mari din cauza absenței acțiunii inhibitoare a IGF-1 asupra secreției de GH. Dwarfismul poate fi, de asemenea, cauzat de insensibilitatea țesutului osos și a altor țesuturi la IGF-1, care rezultă din funcția scăzută a receptorilor IGF-1.
Deficitul de GH persistă adesea până la maturitate, deși unele persoane afectate în copilărie au secreție normală de GH la vârsta adultă. Deficitul de GH la adulți este asociat cu oboseala, scăderea energiei, starea de spirit deprimată, scăderea forței musculare, scăderea masei musculare, pielea subțire și uscată, creșterea țesutului adipos și scăderea densității osoase. Tratamentul cu GH inversează unele dintre aceste anomalii, dar poate provoca retenție de lichide, diabet zaharat și hipertensiune arterială (hipertensiune arterială).
Exces de hormon de creștere
Excesul de producție de GH este cel mai adesea cauzat de o tumoare benignă (adenom) a celulelor somatotrofe ale glandei pituitare. În unele cazuri, o tumoare a plămânului sau a insulelor pancreatice din Langerhans produce GHRH, care stimulează somatotrofii să producă cantități mari de GH. În cazuri rare, producția ectopică de GH (producerea de către celulele tumorale în țesuturile care nu sintetizează în mod obișnuit GH) provoacă un exces de hormon. Tumorile somatotrofe la copii sunt foarte rare și provoacă o creștere excesivă care poate duce la înălțime extremă (gigantism) și caracteristici ale acromegaliei.
Acromegalia se referă la mărirea părților distale (acrale) ale corpului, inclusiv mâinile, picioarele, bărbia și nasul. Mărirea se datorează creșterii excesive a cartilajului, a mușchilor, a țesutului subcutanat și a pielii. Astfel, pacienții cu acromegalie au o maxilară proeminentă, un nas mare și mâini și picioare mari, precum și o mărire a majorității celorlalte țesuturi, inclusiv limba, inima, ficatul și rinichii. În plus față de efectele excesului de GH, o tumoare hipofizară în sine poate provoca dureri de cap severe, iar presiunea tumorii asupra chiasmei optice poate provoca defecte vizuale.
Deoarece acțiunile metabolice ale GH sunt antagonice (opuse) celor ale insulinei, unii pacienți cu acromegalie dezvoltă diabet zaharat. Alte probleme asociate acromegaliei includ hipertensiunea arterială (hipertensiune arterială), bolile cardiovasculare și artrita. Pacienții cu acromegalie prezintă, de asemenea, un risc crescut de a dezvolta tumori maligne ale intestinului gros. Unele tumori somatotrofe produc, de asemenea, prolactină, care poate provoca lactație anormală (galactoree). Pacienții cu acromegalie sunt de obicei tratați prin rezecția chirurgicală a tumorii hipofizare. De asemenea, pot fi tratați cu radioterapie sau cu medicamente precum pegvisomant, care blochează legarea hormonului de creștere de receptorii săi și analogi sintetici cu acțiune îndelungată a somatostatinei, care inhibă secreția de GH.
- Consecințele deficienței sau excesului; Nutriția umană DEPRECATĂ
- Definiție euharistică, simboluri, semnificație, semnificație și fapte Britannica
- Cuvinte încrucișate Definiție, istorie și fapte Britannica
- Efectul terapiei hormonale de creștere de un an asupra factorilor de risc cardiometabolici la băieții cu obezitate
- Efectul aportului de proteine asupra controlului glicemic și a funcției renale la tipul 2 (non-dependent de insulină)