Zahra Faghihimani
1 Departamentul de Nutriție Clinică și Dietetică, Institutul Național de Cercetare în Nutriție și Tehnologie Alimentară, Universitatea Shahid Beheshti de Științe Medicale, Teheran, Iran
2 Centrul de cercetare endocrină și metabolică Isfahan, Universitatea de Științe Medicale Isfahan, Isfahan, Iran
Parvin Mirmiran
1 Departamentul de Nutriție Clinică și Dietetică, Institutul Național de Cercetare în Nutriție și Tehnologie Alimentară, Universitatea de Științe Medicale Shahid Beheshti, Teheran, Iran
Golbon Sohrab
1 Departamentul de Nutriție Clinică și Dietetică, Institutul Național de Cercetare în Nutriție și Tehnologie Alimentară, Universitatea Shahid Beheshti de Științe Medicale, Teheran, Iran
Bijan Iraj
2 Centrul de cercetare endocrină și metabolică Isfahan, Universitatea de Științe Medicale Isfahan, Isfahan, Iran
Elham Faghihimani
2 Centrul de cercetare endocrină și metabolică Isfahan, Universitatea de Științe Medicale Isfahan, Isfahan, Iran
Abstract
Fundal:
Prevalența rapidă în creștere a diabetului zaharat este o problemă serioasă de sănătate în lume. Noile date au stabilit că patogeneza diabetului zaharat este o inflamație cronică de grad scăzut, rezultând rezistență la insulină. Uleiul de semințe de rodie (PSO) are efecte antiinflamatoare; deși poate reduce rezistența la insulină și poate îmbunătăți glicemia în diabetul zaharat. Prezentul studiu a fost conceput pentru a investiga efectele PSO ca componentă dietetică naturală asupra stării metabolice a pacienților cu diabet zaharat de tip 2.
Metode:
Într-un studiu clinic randomizat dublu-orb, 80 de pacienți (28 de bărbați) cu diabet de tip 2 au fost repartizați aleatoriu în grupurile de intervenție și control. Grupul de intervenție a consumat capsule PSO, conținând 1000 mg PSO de două ori pe zi (2000 mg PSO), în timp ce controalele au loc placebo timp de 8 săptămâni. Participanții au urmat modelele dietetice anterioare și utilizarea medicamentelor. Factorii dietetici și factorii metabolici, inclusiv profilul lipidic, zahărul plasmatic în repaus și insulina și au fost analizați la momentul inițial și după 8 săptămâni.
Rezultate:
Participanții la două grupuri de intervenție și control au fost similari în ceea ce privește factorii antropometrici și dietetici la momentul inițial și după studiu (P> 0,05). Nivelurile medii de colesterol total, trigliceride, lipoproteine cu densitate scăzută-colesterol și lipoproteine cu densitate mare nu au fost semnificativ diferite între grupuri după studiu (P> 0,05). Consumul de PSO nu a afectat în mod semnificativ nivelurile de parametri precum zahărul din sânge în repaus alimentar (FBS), insulina, HbA1c, alanina transferază și evaluarea modelului homeostaziei - rezistența la insulină.
Concluzii:
Consumul de 2000 mg PSO pe zi timp de 8 săptămâni nu a avut niciun efect asupra FBS, rezistenței la insulină și profilul lipidic la pacienții diabetici.
INTRODUCERE
Diabetul zaharat a atins acum un nivel epidemic atât în țările în curs de dezvoltare, cât și în cele dezvoltate. Prevalența diabetului zaharat este estimată la aproximativ 387 de milioane de oameni în întreaga lume. [1,2] Ca urmare a nivelului de pandemie, pot apărea complicații macro și micro-vasculare cauzate de diabetul zaharat, care pot reprezenta o amenințare majoră pentru sănătate publică generală în întreaga lume cu costuri economice și sociale uriașe. [3,4] Dovezi recente au sugerat rolul posibil al inflamației de grad scăzut în patogeneza diabetului zaharat. Rezistența la insulină și diabetul zaharat se caracterizează de obicei printr-o creștere a stresului oxidativ și a citokinelor proinflamatorii. [5,6,7] Ca rezultat, majoritatea terapiilor s-au concentrat în principal pe potențialele efecte antioxidante sau antiinflamatorii. [8,9,10 ] În acest context, componentele dietetice naturale oferă o strategie terapeutică alternativă simplă, dar eficientă.
Dintre diferite componente dietetice naturale, sucul de rodie a primit recent multă atenție ca agent antiinflamator funcțional. [11,12] Conținutul ridicat de polifenoli din sucul de rodie ar putea explica efectul său antiinflamator. De-a lungul anilor, numeroase studii au fost dedicate extractului de rodie și potențialelor sale efecte antiinflamatoare. Cu toate acestea, uleiul de semințe de rodie (PSO) poate oferi, de asemenea, efecte antiinflamatorii și puține studii au examinat potențialele sale. [13,14]
PSO constă dintr-un conținut ridicat de acid linolenic conjugat (9-cis, 11-trans, 13-cis) acid octadecatrienoic sau acid punicic (principal ingredient bioactiv). [15,16]
Rezultatele diferitelor studii in vivo și in vitro privind eficacitatea PSO sunt controversate. Investigațiile actuale sugerează că PSO poate îmbunătăți diabetul de tip 2 prin ameliorarea rezistenței la insulină și a obezității la șobolanii cu o dietă bogată în grăsimi. [17] Într-un studiu in vitro, acidul punicic a îmbunătățit glicemia în plasmă (FPG) și profilurile lipidice în repaus alimentar [18]. Scopul nostru în acest studiu este de a prezenta o investigație aprofundată a PSO și a potențialelor sale ca posibilă componentă dietetică naturală pentru îmbunătățirea rezistenței la insulină, a glucozei plasmatice, a dislipidemiei și a tensiunii arteriale la pacienții diabetici.
METODE
Acest studiu a fost un studiu clinic randomizat, dublu-orb, controlat cu placebo. Optzeci de pacienți (28 de bărbați și 52 de femei), în vârstă de 52 ± 6,8 ani, cu diabet de tip 2, au fost înscriși prin eșantionarea convențională din dosarele medicale ale pacienților din centrul de cercetare endocrină și metabolică din Isfahan; toți pacienții au primit agenți hipoglicemianți pe cale orală. Criteriile de incluziune au fost după cum urmează: disponibilitatea la intrarea în studiu; Diabetul zaharat de tip 2 (timp de 5-10 ani); vârsta cuprinsă între 35 și 65 de ani; indicele de masă corporală cuprins între 20 și 30. Criteriile de excludere au fost următoarele: Fumatul, sarcina, orice altă boală cronică, administrarea de estrogeni, progesteron și corticosteroizi sau suplimente antioxidante sau insulină ca medicamente pentru diabet, orice dietă de slăbit în ultima lună; pacienți cu hiperglicemie severă (FPG> 250); insuficiență renală; boala de inima; și insuficiență hepatică.
Având în vedere formula sugerată, dată fiind eroarea de tip 1 de 5%, puterea de studiu de 80% și pe baza publicațiilor anterioare, aveam nevoie de 33 de persoane în fiecare grup. Deoarece am putea lipsi, am adăugat numărul fiecărui grup la 40 de persoane. La momentul inițial, participanții au fost stratificați în funcție de sex și repartizați aleator în două: grupuri de intervenție (PSO, n = 40) și control (placebo, n = 40), folosind recipiente numerotate secvențial. Un asistent a efectuat randomizarea. Atât investigatorul, cât și participanții au fost orbiți de randomizare.
Consimțământul informat scris a fost obținut de la fiecare dintre pacienții selectați. Comitetul etic al Institutului Național de Cercetare în Nutriție și Tehnologie Alimentară (Teheran, Iran) a aprobat protocolul acestui studiu. Studiul clinic a fost înregistrat în Registrul iranian de studii clinice (IRCT201409031640N15).
Toate datele demografice și istoricul medical la momentul inițial au fost documentate.
Grupul de intervenție a consumat capsule PSO, conținând 1000 mg PSO de două ori pe zi (2000 mg PSO), în timp ce martorii au luat capsule placebo timp de 8 săptămâni.
Subiecții au fost sfătuiți să urmeze tiparele anterioare de activitate fizică și dietetică și utilizarea medicamentelor.
Aporturile dietetice ale subiecților au fost înregistrate folosind o rechemare dietetică de 3 zile (2 zile săptămânale și 1 zi de weekend) la momentul inițial și la sfârșitul studiului. Dietele pacienților au fost analizate folosind software-ul Nutritionist IV (N-Squared Computing, San Bruno, CA, SUA).
Măsurători
Probele de sânge venos (10 ml) au fost obținute de la fiecare participant la momentul inițial și la sfârșitul intervenției de 8 săptămâni după un post de 12-14 ore peste noapte. Probele de sânge au fost centrifugate la 4000 rpm timp de 10 min și probele lor de plasmă au fost separate în alicote. Probele au fost congelate la -70 ° C pentru evaluări ulterioare.
Concentrația FPG determinată prin metoda colorimetriei folosind kituri Pars Azmoon (Teheran-Iran). Nivelurile de HbA1C au fost măsurate prin cromatografie cu schimb de ioni (LDN Germania). Nivelul de insulină a fost determinat prin metoda ELISA (Dia Plus, SUA). Trigliceridele plasmatice (TG), colesterolul total, lipoproteinele-colesterol cu densitate ridicată (HDL-C) și lipoproteinele-colesterolul cu densitate mică (LDL-C) au fost măsurate enzimatic de un autoanalizator folosind seturile Pars Azmoon (Teheran-Iran). Evaluarea modelului de homeostazie-rezistență la insulină (HOMA-IR) calculată ca: (Glucoză [mmol/L] × insulină [μU/mL] /22,5).
Greutatea corporală a participanților a fost măsurată la momentul inițial și la sfârșitul intervenției de 8 săptămâni.
Conformitate
Pentru a stabili conformitatea pacientului, am furnizat fiecărui pacient un număr fix de capsule PSO și am recomandat returnarea capsulelor neutilizate la sfârșitul studiului.
Respectarea tratamentului a fost determinată pe baza numărului de capsule returnate de fiecare pacient. Rata a fost de 90% pentru populația noastră studiată.
Ulei din semințe de rodie și capsule placebo
Compoziția PSO este prezentată în Tabelul 1. PSO și placebo au fost preparate de Zahravi Inc., Teheran, Iran. Capsulele placebo conțineau triacilglicerol cu lanț mediu.
tabelul 1
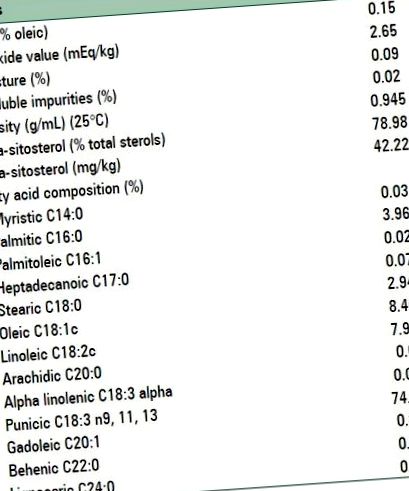
Compoziția uleiului de semințe de rodie
Pe baza analizei chimice, conținutul principal de acizi grași din PSO a fost după cum urmează; Acid punicic (PA) (18: 3) 74,48%; acid oleic (18: 2) 8,46%; acid palmitic (16: 0) 3,96%; acid stearic (18: 0) 2,94%; și urme (1%) de alți acizi grași. Conținutul de antioxidant în vitamina E al PSO brut a fost de 36 · 90 mg/100 g; care a fost păstrat la temperatura rece pentru a preveni oxidarea până la formularea în capsule.
analize statistice
Aceasta este o intenție de a trata un studiu clinic. Rezultatele sunt exprimate ca medie ± SD pentru variabilele cantitative și n (%) pentru variabilele calitative, iar diferențele au fost considerate semnificative la P ≤ 0,05.
Analiza statistică a datelor a fost efectuată utilizând software-ul SPSS versiunea 21.0 (Chicago, IL, SUA). Variabile calitative comparate între cele două grupuri studiate folosind testul Chi-pătrat. Normalitatea parametrilor cantitativi a fost determinată de testul Kolmogorov-Smirnov. Pentru a compara parametrii cantitativi în perioada pre- și post-intervenție, în cadrul și între grupuri a fost utilizat testul t asociat.
Pentru a compara mediile variabilelor după studiu și a determina efectul principal al tratamentului, modelul liniar general (ANCOVA) a fost utilizat cu valori de 8 săptămâni (durata procesului) ca variabile dependente, valorile de bază ca covariabile și grupul de tratament ca factor fix.
REZULTATE
Caracteristicile inițiale ale pacienților nu au diferit semnificativ între grupul tratat cu PSO și grupul placebo vârsta medie în grupul PSO a fost de 52 ± 6,8 (ani) și în grupul placebo a fost de 48 ± 85 (ani). În grupul PSO, 26% dintre persoanele din grupul placebo și 22% dintre persoanele din grupul placebo erau femei. Durata diabetului a fost de 7,8 ± 2,2 (ani) și 7,5 ± 2,3 (ani) în grupul PSO și, respectiv, placebo [Tabelul 2].
masa 2
Caracteristicile inițiale ale pacienților din grupurile de ulei de semințe de rodie și placebo
În comparație între grupuri, măsurătorile antropometrice și factorii dietetici au fost similare în două grupuri studiate înainte și după proces. În comparație de grup, variabilele studiate nu au avut modificări semnificative după studiu în cele două grupuri studiate [Tabelul 3].
Tabelul 3
Factori antropometrici și dietetici în grupurile de ulei de semințe de rodie și placebo
Concentrația medie a colesterolului total a fost semnificativ diferită între cele două grupuri la momentul inițial și la sfârșit; cu toate acestea, modificările medii nu au fost diferite între cele două grupuri la sfârșitul studiului.
Concentrația TG a fost semnificativ diferită între cele două grupuri la momentul inițial, dar nu a existat nicio diferență semnificativă între cele două grupuri la cele 8 săptămâni. De asemenea, concentrația medie de LDL-C a fost semnificativ diferită între două grupuri la momentul inițial; cu toate acestea, nu au existat diferențe semnificative între cele două grupuri în a 8-a săptămână și, de asemenea, în modificările medii. HDL-C s-a redus semnificativ la ambele grupuri la sfârșitul studiului comparativ cu valoarea inițială; cu toate acestea, nu au existat diferențe semnificative între cele două grupuri la sfârșitul studiului. Consumul de PSO nu a avut niciun efect semnificativ asupra nivelurilor de FPG, insulină, HbA1c, alanină transferază și HOMA-IR [Tabelul 3].
Tabelul 4
Concentrațiile plasmatice ale factorilor de măsurare în grupurile de ulei de semințe de rodie și placebo
După cum sa arătat sub formă de consoartă, patru persoane din grupul PSO nu au putut continua studiul. Două femei au avut erupții cutanate și mâncărime care au dispărut după întreruperea tratamentului. Un bărbat era supărat gastro-intestinal (GI). Un alt bărbat a avut sângerări GI superioare, ceea ce a cauzat internarea pacientului. După tratament, el a externat. Trei pacienți din grupul placebo au întrerupt tratamentul cu placebo din cauza cefaleei sau a unei ușoare tulburări abdominale [Figura 1].
Organigrama studiului
DISCUŢIE
În studiul de față, am constatat că consumul de 2000 mg PSO/zi timp de 8 săptămâni nu a avut niciun efect asupra glicemiei în post, a rezistenței la insulină și a profilului lipidic la pacienții diabetici. Din câte știm, acesta este primul studiu care a evaluat rezultatele consumului de PSO la pacienții diabetici. Studiile anterioare au arătat efectele PSO la modelele animale. [19] Într-un studiu realizat pe șoareci, Miranda și colab. au arătat că PA nu a scăzut acumularea de grăsimi în ficat și în alte organe ale șobolanilor hrăniți cu o dietă obezogenă și nu a dus la îmbunătățirea controlului glicemic. [20] Nekooeian și colab. a investigat impactul șobolanilor diabetici PSO tip 2. Au indicat că nivelul de insulină plasmatică a crescut fără nicio reducere a nivelului de glucoză plasmatică. Mecanismul acestui lucru este necunoscut, dar ar putea fi legat de reglarea în sus a genelor receptor-g (PPAR-g) activate de proliferatorul peroxizomului. [21]
Un studiu in vitro a arătat că disfuncția proteinelor induse de factorul de necroză tumorală a acidului punicic (TNF-α), prin urmare, absorbția glucozei și rezistența la insulină se pot îmbunătăți după administrarea acidului punicic. [22] Într-un alt studiu, consumul de PSO a dus la o reducere a nivelurilor plasmatice de TNF-α la șoareci. Cu toate acestea, tratamentul cu PSO la pacienții dislipidemici nu a avut niciun efect asupra TNF-α seric într-un studiu. [23]
Mai mult, studiile in vitro au documentat că acidul punicic este un agonist pentru PPAR, ținta moleculară pentru tiazolidindione, agenți antidiabetici. Cu toate acestea, agoniștii naturali ai PPAR sunt acidul punicic. PA poate crește expresia genică a PPAR și astfel poate îmbunătăți homeostazia glucozei și rezistența la insulină asociată inflamației. [24]
De asemenea, au arătat că PSO poate reduce stresul oxidativ, dar nu a avut efect asupra profilului lipidic seric. Studiile anterioare au documentat că „acidul gras polinesaturat n-3 este un agent hipolipidemic.] [25,26] Rezultatele studiilor recente privind efectul PSO asupra profilurilor lipidice sunt controversate. În studiul de față, nu a existat nicio diferență semnificativă în nivelurile serice de colesterol total, LDL, HDL-C și TAG la două grupuri de pacienți diabetici. Într-un studiu in vivo pe șobolani obezi, hiperlipidemici, s-a demonstrat că dieta suplimentată cu PSO nu a avut efect asupra țesutului adipos alb alb și asupra profilului lipidic seric, ci reduce acumularea de triacilglicerol hepatic similar grupului de control. [14] Un mecanism probabil a confirmat într-un studiu in vitro că în celulele HepG2 CLN 9-cis, 11-trans, 13-cis a suprimat sinteza TAG. [27] Mirmiran și colab. a constatat că consumul de 800 mg PSO nu a modificat colesterolul și LDL-C, dar a scăzut raportul TAG și TAG: HDL-C pe parcursul a 4 săptămâni de studiu la subiecții hiperlipidemici. [28]
Trebuie remarcat faptul că nu există o experiență anterioară cu PSO la pacienții diabetici, ceea ce ne-a limitat să administrăm doze în creștere de PSO.
Limitările acestui studiu sunt dimensiunea redusă a eșantionului din populația studiată și nu evaluarea nivelului seric de PSO.
Au fost necesare studii suplimentare pentru a evalua efectul suplimentării cu PSO la pacienții diabetici.
CONCLUZII
În prezentul studiu, am constatat că consumul de 2000 mg PSO/zi timp de 8 săptămâni nu a avut niciun efect asupra glicemiei în post, a rezistenței la insulină și a profilului lipidic la pacienții diabetici. Poate fi îngrijorat de dimensiunea redusă a eșantionului studiului nostru. Trebuie să investigăm efectul PSO în grupuri mai mari de oameni sau ar trebui să creștem durata studiului. După cum am arătat siguranța a 2000 mg/zi de PSO, studiile viitoare pot crește doza acestuia.
- Articolul complet Având în vedere microbiota intestinală în tratamentul diabetului zaharat de tip 2
- Cushing; Sindromul s-a prezentat cu scădere în greutate și diabet zaharat de tip II BES2002 21st Joint
- Beneficii ale extractului de semințe de țelină, efecte secundare; Dozare
- Întârzierea intervenției chirurgicale bariatrice și metabolice în timpul pandemiei COVID-19 pune pacienții la risc, experți
- Interviu exclusiv cu Jennifer Stone despre modul în care gestionează actorița, diabetul de tip 1 și mai mult dLife