Abstract
Obiectiv
Alimentele cu indice glicemic contrastant, atunci când sunt încorporate într-o masă, sunt capabile să modifice diferențial glicemia și insulinemia. Cu toate acestea, se știe puțin despre faptul că acest lucru depinde de mărimea mesei. Scopurile acestui studiu au fost: i) să se determine dacă impactul diferențiat asupra glicemiei și a răspunsurilor la insulină induse de alimentele GI contrastante este similar atunci când sunt furnizate în mese de diferite dimensiuni și; ii) pentru a determina relația dintre sarcina glicemică totală a mesei și răspunsurile observate la glucoză și insulină în ser.
Metode
Au fost recrutate 12 femei obeze (IMC 33,7 ± 2,4 kg/m 2). Subiecții au primit 4 mese diferite în ordine aleatorie. Două mese au avut un indice glicemic scăzut (40-43%) și două au avut un indice glicemic ridicat (86-91%). Ambele tipuri de mese au fost administrate ca două mărimi de masă, cu furnizarea de energie corespunzătoare a 23% și 49% din rata metabolică bazală prevăzută. Astfel, au fost administrate mese cu trei încărcături glicemice diferite (95, 45-48 și 22 g). Probele de sânge au fost prelevate înainte și după fiecare masă pentru a determina concentrațiile de glucoză, acizi grași liberi, insulină și glucagon pe o perioadă de 5 ore.
Rezultate
S-a observat o creștere a nivelului de glucoză și insulină serică de aproape 2 ori mai mare sub curbă (ASC) de peste 2 ore pentru mesele de aceeași dimensiune cu indice glicemic ridicat sau scăzut (p
fundal
Măsura răspunsului postprandial al glucozei serice rezultă în principal din efectul combinat al cantității și indicelui glicemic (GI) de carbohidrați conținut într-o porție alimentară [1, 2]. Sarcina glicemică (GL) corespunde produsului IG al fiecărui produs alimentar și cantității de carbohidrați dintr-o porție (g) împărțită la 100. Acest concept a fost recent validat folosind alimente izolate cu carbohidrați [3, 4]. S-a demonstrat că prin ajustarea cantității de alimente cu carbohidrați pentru a obține valori GL identice, se obține un răspuns similar al glicemiei [3]. În plus, creșterile treptate ale GL au produs creșteri proporționale ale glicemiei [3, 4].
Când se consumă mese mixte care conțin alimente cu carbohidrați cu indice glicemic contrastant, se știe că diferența în răspunsul glicemiei postprandiale se menține [5]. Cu toate acestea, amploarea acestui răspuns diferențiat al glicemiei poate depinde de mărimea mesei.
Conform rezultatelor studiilor care utilizează alimente izolate cu carbohidrați cu IG contrastante, se anticipează o diferență absolută mai mare în răspunsul la glucoză din sânge pe măsură ce mărimea mesei crește [6] și, în termeni proporționali, această diferență va fi similară la orice dimensiune a mesei. Această situație poate fi teoretic previzionată prin calcularea GL total al unei mese. Astfel, în mesele cu alimente GI-carbohidrați egali, diferența absolută în răspunsul la glucoză din sânge va crește odată cu creșterea cantității de carbohidrați.
Am urmărit să testăm aceste ipoteze în prezentul studiu prin evaluarea răspunsului la glucoză serică și a altor variabile sanguine relevante, după consumul meselor de dimensiuni mici și mari cu IG contrastant. Au fost, de asemenea, testate relațiile dintre masa GL și răspunsurile serice la glucoză și insulină. Acest studiu a arătat că mesele cu două IG-uri contrastante sunt la fel de capabile să afecteze diferențiat răspunsurile serice la insulină atunci când sunt furnizate într-o masă de dimensiuni mici sau mari. Mai mult, s-au observat asocieri directe între masa GL și răspunsurile serice la glucoză și insulină.
Metode
Subiecte
Au fost recrutați doisprezece femei obeze, dar altfel sănătoase (vârsta 33,2 ± 8,0 (medie și SD) ani, greutate 82,3 ± 10,6 kg, IMC 33,7 ± 2,4 kg/m 2). Criteriile de incluziune au fost absența semnelor clinice sau a simptomelor bolii cronice, determinate de examenul fizic și analizele de laborator, nedieta în ultimele 3 luni, stilul de viață sedentar, lipsa medicației, testul normal de toleranță la glucoză pe cale orală pentru a exclude diabetul și intoleranța la glucoză ] și profilul lipidic normal de post [8]. Toți subiecții și-au dat consimțământul informat în scris pentru a participa la studiu. Consiliul de etică al Institutului de nutriție și tehnologie alimentară (INTA) a aprobat protocolul experimental.
Proiectare experimentală
Subiecții au fost rugați să evite orice exercițiu fizic intens și să își mențină aportul alimentar obișnuit timp de 48 de ore înainte de zilele de testare. În 4 ocazii separate, subiecții au venit la INTA în seara dinaintea zilei de testare propriu-zisă. După sosire, au mâncat o cină standardizată conținând 34 kJ/kg de masă corporală, oferind 55% energie sub formă de carbohidrați, 25% sub formă de grăsimi și 20% sub formă de proteine. După un post peste noapte de 12 ore, o prelevare de sânge i.v. canula a fost introdusă în vena antecubitală. Probele de sânge au fost prelevate la -15, -10 și -5 min (analizate ca un bazin) înainte de masa experimentală, la fiecare 15 minute pentru prima oră și la fiecare 30 de minute după aceea pentru a finaliza o perioadă postprandială de 5 ore. Toate testele au fost efectuate în decurs de 10 zile de la debutul anticipat al menstruației.
Mese experimentale
Analize de probe de sânge
Probele de sânge venos pentru glucoză, insulină și FFA au fost colectate în tuburi de sticlă și lăsate să se coaguleze pe gheață timp de 10 minute; serul a fost apoi separat la temperatura camerei și depozitat imediat la -20 ° C până la analiză. Probele de glucagon din sânge au fost prelevate în Vacutainer-EDTA cu Trasylol® adăugat (50 μl/ml de sânge) și apoi s-a obținut plasmă și s-a păstrat așa cum s-a descris mai sus. Glucoza serică a fost testată prin metoda glucozei oxidazei (Instrument fotometric 4010, Roche, Basel, Elveția). Kit de testare Ser FFA by WAKO NEFA-C (Wako Chemicals, Richmond, VA, SUA) pe un analizor Hitachi-717 (Tokyo, Japonia). Insulina serică a fost măsurată utilizând RIA (DSL, Webster, TX, SUA). Glucagonul plasmatic a fost determinat de RIA (EURIA-Diagnostica, Malmö, Suedia).
Răspunsurile postprandiale ale glucozei și insulinei serice au fost evaluate utilizând aria incrementală (iAUC) și aria totală sub curbă (tAUC) la 2 h, 5 h și între 2-5 h. Răspunsurile postprandiale ale FFA serului și ale glucagonului plasmatic au fost evaluate utilizând tAUC la 2 h, 5 h și între 2-5 h. iAUC și tAUC au fost calculate geometric folosind metoda trapezoidală. Pentru primii, aria sub valorile bazale nu a fost luată în considerare [12].
Analize statistice
Rezultatele sunt exprimate ca mediană și interval intercuartilic, dacă nu se specifică altfel. Datele au arătat o distribuție non-parametrică și au fost tratate ca atare. Analiza Friedman a fost utilizată pentru a testa diferențele între grupuri [13]. Pentru a determina semnificația, post-hoc testarea a fost efectuată folosind testul Wilcoxon cu două cozi, pentru comparații perechi [13]. Au fost, de asemenea, evaluate interacțiunile dintre tipul de carbohidrați și conținutul de macronutrienți. Un alfa eroarea de 0,05 a fost considerată semnificativă statistic. Datele au fost prelucrate cu Analyze-It Software, Ltd. (Leeds, Marea Britanie).
Rezultate
Toți subiecții au finalizat protocolul experimental; mesele au fost complet consumate în toate cazurile. Nu s-au observat plângeri sau tulburări digestive. Greutatea corporală a fost stabilă pe tot parcursul studiului (-0,4 ± 1,4%, medie ± SD, p = NS).
Glucoza serică
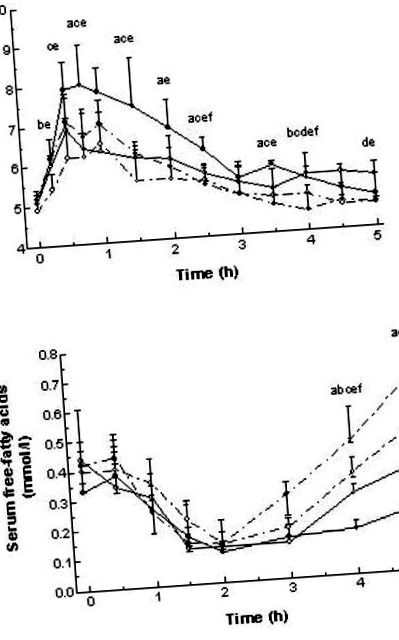
Profilul glucozei postprandiale serice a prezentat un model similar pentru toate mesele, cu un vârf înainte de 1 oră și revenind la valori aproape de post la aproximativ 3 ore (Figura 1). Indicele glicemic al meselor a modificat iAUC și tAUC ale glucozei serice numai la mesele mari, în timp ce nu s-a observat niciun efect după consumul meselor mici. Cu toate acestea, la compararea medianelor s-a observat o diferență proporțional similară în ambele cazuri, în special la evaluarea iAUC glucozei serice. Diferența de ASC a glucozei serice a fost observată în toate perioadele de timp (0-2 h, 0-5 h, 2-5 h), în timp ce, pentru tAUC glucozei serice, diferența a fost observată în perioada postprandială timpurie (0-2 h) numai.
În ceea ce privește relația dintre GL estimat și iAUC glucozei serice observate, s-a observat o asociere directă timp de 2 ore (r = 0,58, p Figura 2
Relația dintre încărcarea glicemică și răspunsurile serice la glucoză și insulină timp de 2 și 5 ore. Valorile sunt mediane și 25 și 75 percentile. (∘) indice glicemic scăzut/dimensiune mică a mesei; (∙) indice glicemic ridicat/dimensiune mică a mesei; (□) indice glicemic scăzut/dimensiune mare a mesei; (■) indicele glicemic ridicat/mărimea mare a mesei.
Acizi grași fără ser
De la post până la 2 ore, supresia post-prandială a FFA în ser a fost independentă atât de mărimea mesei, cât și de carbohidrații GI (Figura 1). În consecință, nu s-au găsit diferențe în tAUC seric al FFA peste 2 ore între mese (p = 0,82, Tabelul 2). Cu toate acestea, de la post la 5 ore, răspunsul seric FFA a diferit în funcție de mărimea mesei consumate; răspunsul a fost mai mic după mesele mari comparativ cu mesele mici (p Tabelul 2 Suprafață incrementală și/sau totală sub curbă pentru glucoză serică, acizi grași liberi, insulină și glucagon plasmatic după mese experimentale.
Insulina serică
După mese, profilul seric al insulinei a avut o formă similară cu un vârf înainte de 1 oră independent de IG sau de mărimea mesei și revenind la niveluri aproape de post la aproximativ 3 și 5 ore pentru mesele mici și, respectiv, pentru masa mare (Figura 3). IG a influențat răspunsurile de insulină serică postprandială integrate (iAUC și tAUC) timp de 2 și 5 ore în ambele dimensiuni de masă (p ≤ 0,016, Tabelul 2). Diferența în răspunsul insulinic seric pentru masa mare a fost observată pentru toate perioadele de timp (0-2 h, 0-5 h, 2-5 h) independent de metoda de analiză a răspunsului postprandial. Pe de altă parte, pentru masa mică, efectul diferențial al GI peste 5 ore a fost luat în considerare în perioada postprandială timpurie (0-2 ore), atunci când s-au observat atât insulina serică iAUC, cât și tAUC. După cum s-a observat pentru răspunsul glucozei serice, s-a găsit o relație strânsă între GL și insulina serică iAUC peste 2 ore (r = 0,60, p Figura 3
Glucagon plasmatic
Concentrațiile de glucagon din plasmă au fost relativ constante pe parcursul întregii perioade postprandiale (Figura 3). Mai mult, mărimea mesei și tipul de carbohidrați nu au afectat tAUC glucagonic plasmatic peste 2 ore (p = 0,11) și 5 ore (p = 0,10) (Tabelul 2).
Discuţie
Când se consumă mese mixte, vor fi prezente și alte alimente și macronutrienți. În acest studiu, rezultatele au fost similare cu cele observate în studiile care utilizează carbohidrați izolați [6] și implică faptul că alți macronutrienți au avut un efect negativ asupra răspunsurilor diferențiate la glucoză și insulină. De fapt, s-a raportat în altă parte că cantitatea și tipul de carbohidrați reprezintă aproximativ 90% din variabilitatea totală a răspunsului la glucoză din sânge, în timp ce proteinele și grăsimile din mesele mixte contribuie cu greu la variația glicemiei și a răspunsurilor la insulină [1], 2].
În raport cu alte răspunsuri metabolice ale sângelui, acest studiu și alții [14-17] au demonstrat că mesele mixte care conțin alimente GI contrastante nu afectează, sau afectează doar ușor, răspunsul FFA din sânge. Abia la sfârșitul perioadei postprandiale (4-5 ore), supresia serică a FFA a fost mai mare pentru mesele mari, comparativ cu cele mici. Aceasta este o constatare așteptată în funcție de concentrația mai mare de insulină serică observată în perioada postprandială timpurie. În ceea ce privește efectul IG, rezultatul a fost oarecum neașteptat, deoarece s-a găsit o concentrație crescută de FFA serică pentru masa mică cu IG ridicat. Relevanța biologică a acestor descoperiri necesită cercetări suplimentare, deoarece poate fi importantă pentru înțelegerea tulburărilor de rezistență la insulină, reglarea aportului alimentar și a metabolismului lipidelor. În ceea ce privește nivelurile periferice de glucagon în plasmă, așa cum s-a constatat în alte studii, nu s-a observat nicio influență a IG sau a mărimii mesei [14].
Un aspect al acestui studiu care ar trebui comentat este metoda (pentru care există multe alegeri [18]) aleasă pentru a analiza răspunsul postprandial integrat. Pentru a estima indicele glicemic alimentar la subiecții sănătoși, Organizația pentru Alimentație și Agricultură [19] recomandă utilizarea ASC incrementală, care a fost confirmată de Wolever [18] după compararea mai multor metode de analiză. Această recomandare a fost făcută pe baza faptului că rezultatul (adică IG) a fost independent de caracteristicile subiecților (de exemplu, diabetic, sănătos etc.). Pe de altă parte, când au fost folosite diferite metode pentru a estima modificarea răspunsului la glucoză din sânge înainte și după un program de exerciții de 9 luni la subiecții supraponderali, Potteiger și colab. [20] nu au găsit diferențe între ASC incrementale, incrementale pozitive sau totale. pentru glucoză din sânge. Toate metodele au fost la fel de eficiente în măsurarea impactului intervenției asupra glicemiei. În prezentul studiu, s-a obținut o concluzie practic identică utilizând ASC incrementală și totală atât pentru glucoza serică, cât și pentru insulină. Evaluarea critică a acestui număr merită cercetări suplimentare.
În concluzie, acest studiu a arătat că GI singur nu este în măsură să prezică impactul glicemic atunci când se consumă diferite cantități de carbohidrați. Mai mult, este susținută utilizarea GL pentru a diferenția impactul acut asupra glicemiei și a răspunsurilor la insulină induse de mesele mixte. Acest lucru este relevant pentru studiile epidemiologice care investighează rolul glucidelor în bolile cronice netransmisibile.
Referințe
Wolever T, Bolognesi C: Predicția răspunsurilor la glucoză și insulină ale subiecților normali după consumul meselor mixte, variind în energie, proteine, grăsimi, carbohidrați și indicele glicemic. J Nutr. 1996, 126: 2807-2812.
Sheard N, Clarke N, Brand-Miller J, Franz M, Pi-Sunyer F, Mayer-Davis E, Kulkarni K, Geil P: Glucide dietetice (cantitate și tip) în prevenirea și gestionarea diabetului: o declarație a americanului Asociația pentru diabet. Îngrijirea diabetului. 2004, 27: 2266-2271.
Brand-Miller J, Thomas M, Swan V, Ahmad Z, Petocz P, Colagiuri S: Validarea fiziologică a conceptului de încărcare glicemică la adulții tineri slabi. J Nutr. 2003, 133: 2728-2732.
Venn B, Wallace A, Monroe J, Perry T, Brown R, Frampton C, Green T: Sarcina glicemică estimată din indicele glicemic nu diferă foarte mult de cea măsurată folosind o curbă standard la voluntarii sănătoși. J Nutr. 2006, 136: 1377-1381.
Chew I, Brand J, Thorburn A, Truswell A: Aplicarea indicelui glicemic la mesele mixte. Sunt J Clin Nutr. 1988, 47 (1): 53-6.
Wolever T, Bolognesi C: Sursa și cantitatea de carbohidrați afectează glucoza și insulina postprandială la subiecții normali. J Nutr. 1996, 126: 2798-2806.
Raport al comitetului de experți privind diagnosticul și clasificarea diabetului zaharat. Îngrijirea diabetului. 2003, 26 (supl. 1): S5-S20.
Rezumatul celui de-al doilea raport al Panoului de experți al Programului Național de Educație pentru Colesterol (NCEP) privind detectarea, evaluarea și tratamentul colesterolului ridicat din sânge la adulți (Panoul II de tratament pentru adulți). JAMA. 1993, 269: 3015-3023. 10.1001/pit.269.23.3015.
Raportul unei consultări comune a experților FAO/OMS/UNU. Cerințe de energie umană. Seria de rapoarte tehnice privind alimentația și nutriția nr. 1. Roma: FAO/OMS/UNU. 2001
Schmidt-Hebbel H, Pennacchiotti I, Masson L, Mella MA: Tabel de compoziție a alimentelor chiliene. Editat de: Facultatea de Chimie și Farmacie. 1992, Universitatea din Chile., 8a
Foster-Powell K, Holt S, Brand-Miller J: Tabel internațional cu indicele glicemic și valorile sarcinii glicemice: 2002. Am J Clin Nutr. 2002, 76: 5-56.
Wolever T, Jenkins D: Utilizarea indicelui glicemic în prezicerea răspunsului glicemiei la mesele mixte. Sunt J Clin Nutr. 1986, 43: 167-172.
Sheskin D: Analiza bidirecțională Friedman a varianței pe grade. Manual de proceduri statistice parametrice și neparametrice. Editat de: Sheskin D. 2004, Boca Raton: Chapman & Hall/CRC Press, 845-865. 3
Ludwig D, Majzoub J, Al-Zahrani A, Dallal G, Blanco I, Roberts S: Alimente cu indice glicemic ridicat, supraalimentare și obezitate. Pediatrie. 1999, 103: 26-31. 10.1542/peds.103.3.e26.
Brynes A, Edwards M, Ghatei M, Dornhorst A, Morgan L, Bloom S, Frost G: Un studiu randomizat, cu patru intervenții, care investighează efectul glucidelor asupra profilurilor de zi ale insulinei, glucozei, acizilor grași neesterificați și triacilglicerolilor din mijloc bărbați în vârstă. Br J Nutr. 2003, 89: 207-218. 10.1079/BJN2002769.
Harbis A, Perdreau S, Vincent-Baudry S, Charbonnier M, Bernard MC, Raccah D, Senft M, Lorec AM, Defoort C, Portugal H, Vinoy S, Lang V, Lairon D: acumularea de lipoproteine intestinale la subiecții obezi, rezistenți la insulină. Sunt J Clin Nutr. 2004, 80: 896-902.
Korach-André M, Roth H, Barnoud MP, Peronnet F, Leverve X: Aspectul glucozei în circulația periferică și producția de glucoză hepatică la bărbați după o masă mare de amidon de 13C. Sunt J Clin Nutr. 2004, 80: 881-886.
Wolever T: Efectul programului de prelevare a sângelui și metoda de calcul al ariei de sub curbă asupra validității și preciziei valorilor indicelui glicemic. Br J Nutr. 2004, 91: 295-300. 10.1079/BJN20031054.
Raportul unei consultări a experților FAO/OMS privind carbohidrații în nutriția umană. Organizația pentru Alimentație și Agricultură Roma Italia Roma: FAO. 14-18 aprilie 1997.
Potteiger J, Jacobsen D, Donnelly J: o comparație a metodelor de analiză a glucozei și a insulinei sub curba după nouă luni de exerciții la adulții supraponderali. Int J Obezitate. 2002, 26: 87-89. 10.1038/sj.ijo.0801839.
Mulțumiri
Această lucrare a fost susținută de un grant de la Comisia Națională de Știință și Tehnologie, Chile (Fondecyt nr. 1010559). Suntem foarte recunoscători pentru asistența Sarah Wolf, BSc și Gail Goldberg, dr. Pentru traducerea în limba engleză. Voluntarii sunt recunoscuți în special pentru contribuțiile lor.
Informatia autorului
Afilieri
Laboratorul de metabolizare a energiei și izotopi stabili, Institutul de nutriție și tehnologie alimentară (INTA), Universitatea din Chile, Chile
José Galgani, Carolina Aguirre și Erik Díaz
Puteți căuta acest autor și în PubMed Google Scholar
Puteți căuta acest autor și în PubMed Google Scholar
Puteți căuta acest autor și în PubMed Google Scholar
autorul corespunzator
Informatii suplimentare
Interese concurente
Autorii declară că nu au interese concurente.
Contribuțiile autorilor
JG a conceput studiul, a participat la proiectarea și coordonarea acestuia și a contribuit la elaborarea manuscrisului. CA a efectuat studiul și a ajutat la elaborarea manuscrisului. ED a conceput studiul, a participat la proiectarea acestuia și a ajutat la elaborarea manuscrisului. Toți autorii au citit și au aprobat manuscrisul final.
Fișierele originale trimise de autori pentru imagini
Mai jos sunt linkurile către fișierele originale trimise de autori pentru imagini.
- Un control mai bun al glicemiei găsit în dietele bogate în proteine din plante, surse animale
- Dispozitive de monitorizare a glicemiei din sânge FDA
- Un studiu controlat randomizat al efectului sfaturilor dietetice cu conținut scăzut de grăsimi asupra răspunsului alimentar la insulină
- Există diferite tipuri de calorii Alegeți un indice glicemic scăzut
- O sarcină sănătoasă - Fundația indicelui glicemic