Parcul Hye Soon
Departamentul de Medicină de Familie, Asan Medical Center, Universitatea din Ulsan College of Medicine, Seul, Coreea.
Su Jung Sim
Departamentul de Medicină de Familie, Asan Medical Center, Universitatea din Ulsan College of Medicine, Seul, Coreea.
Parcul Jung Yul
* Departamentul de Neurochirurgie, Centrul Medical al Universității Coreea, Seul, Coreea.
Abstract
INTRODUCERE
Cel de-al treilea raport al Programului național de educație pentru colesterol Panelul pentru tratamentul adulților III (NCEP ATP III) a propus importanța sindromului metabolic în evaluarea și gestionarea bolilor cardiovasculare (1). Persoanele cu sindrom metabolic prezintă un risc crescut de morbiditate și de mortalitate prin boli cardiovasculare (2, 3). Obezitatea abdominală, în special obezitatea viscerală, promovează rezistența la insulină (4-6) și provoacă, de asemenea, gruparea factorilor de risc cardiovascular la un nivel dat al indicelui de masă corporală (IMC) (7, 8). O circumferință a taliei înalte, un bun predictor al bolilor cardiovasculare (9), este unul dintre punctele de vedere diagnostice importante ale sindromului metabolic. Un studiu prospectiv recent a arătat că obezitatea pare a fi componenta centrală a sindromului metabolic (10) și, prin urmare, identificarea acestor indivizi cu risc ridicat ar fi crucială pentru a oferi o terapie adecvată cu tratamente de modificare a bolii disponibile în prezent, împreună cu recomandarea reducerii greutății ca tratament de primă linie (1).
Coreea, ca și alte țări asiatice, a cunoscut o creștere socio-economică rapidă, cu o transformare proeminentă a stilului de viață în ultimele decenii. Bolile cardiovasculare sunt considerate una dintre cele mai frecvente cauze de deces în Coreea (11). Asiaticii tind să prezinte o prevalență ridicată a factorilor de risc cardiovascular la un IMC chiar mai mic comparativ cu caucazienii, probabil din cauza unei obezități centrale mai mari (8). Prevalența sindromului metabolic a fost raportată a fi mai mare de 20% în rândul coreenilor, în ciuda unei prevalențe mai mici a obezității (12). Cu toate acestea, creșterea IMC a fost identificată ca unul dintre factorii de risc independenți modificabili ai sindromului metabolic în rândul coreenilor (12).
Se știe că modificarea factorilor asociați este esențială pentru prevenirea și gestionarea sindromului metabolic. Cu toate acestea, sunt disponibile puține informații cu privire la efectul reducerii greutății sau modificării distribuției grăsimilor asupra componentelor metabolice la pacienții obezi în rândul coreenilor. Obiectivele acestui studiu au fost de a examina modificarea indicilor antropometrici, a distribuției grăsimilor și a componentelor metabolice cu o reducere modestă a greutății (5-10%), de a compara eficacitatea reducerii greutății la pacienții cu sau fără sindrom metabolic și de a investiga variabilele previzibile pentru îmbunătățirea componentelor metabolice și rezistența la insulină în timpul reducerii greutății la pacienții obezi coreeni.
MATERIALE ȘI METODE
Recrutarea subiecților
Studiul nostru a inclus 78 de pacienți obezi (IMC ≥25 kg/m 2) cu vârste cuprinse între 15 și 60 de ani (19 bărbați și 59 femei) care au vizitat Clinica de obezitate din Centrul Medical Asan. Acest studiu a fost aprobat de Revizuirea instituțională a Consiliului de administrație al Asan Medical Center. Subiecții excluși din acest studiu au fost femeile însărcinate sau care alăptează și cei cu cauze secundare de obezitate și dovezi ale bolilor hepatice sau renale severe. De asemenea, au fost excluși subiecții care luau medicamente care ar fi putut afecta componentele metabolice ale sindromului metabolic (de exemplu, medicamente antihipertensive, agenți hipoglicemici orali, insulină, agenți hipolipidemici și inhibitori de lipază). Toți indivizii au fost supuși unei evaluări medicale de către medici responsabili de efectuarea istoricului medical complet și a examinării fizice.
Măsurători antropometrice
Măsurătorile antropometrice au fost luate cu subiecții în haine ușoare și fără încălțăminte. Înălțimea și greutatea au fost măsurate printr-o scală automată înălțime-greutate, la cel mai apropiat de 0,1 cm și 0,1 kg. Indicele de masă corporală (IMC) a fost calculat prin împărțirea greutății (kg) la pătratul înălțimii (m 2). Procentul de grăsime corporală și totalul de grăsime corporală au fost apoi măsurate prin analiza bioimpedanței (Inbody 3.0, Biospace, Seoul, Coreea) (13). Circumferința taliei a fost măsurată la punctul mediu dintre marginea inferioară a cutiei toracice și creasta iliacă și circumferința șoldului în cea mai lată parte a regiunii șoldului. Doar un tehnician bine instruit a verificat măsurătorile antropometrice pe parcursul întregului proces al acestui studiu pentru a reduce variațiile interumane. Raportul talie-șold (WHR) a fost calculat prin împărțirea circumferinței taliei la circumferința șoldului.
Tomografie computerizata
Secțiunile transversale ale țesutului adipos visceral și subcutanat abdominal au fost măsurate prin tomografie computerizată (CT) pe un scanner Siemens Somaton (Erlangen, Germania) utilizând un protocol stabilit (14, 15). O scanare în secțiune transversală cu grosimea de 10 mm centrată pe spațiul discului vertebral L4-L5 cu subiectul în poziție culcat a fost obținută utilizând o radiografie a scheletului ca referință pentru a stabili poziția scanărilor la cel mai apropiat milimetru. Limitele țesutului adipos subcutanat și visceral (SAT și TVA) au fost definite folosind un cursor manual prin delimitarea acestor zone cu un stilou grafic, iar suprafețele țesutului adipos au fost calculate calculând suprafețele țesutului adipos cu un interval de atenuare de la -190 la -30 Hounsfield unități. Zona TVA abdominală a fost măsurată trasând o linie în peretele muscular care înconjoară cavitatea abdominală. Suprafața SAT a fost calculată prin scăderea suprafeței TVA din suprafața totală a țesutului adipos (TAT) și raportul TVA la SAT (VSR) a fost apoi calculat.
Variabile metabolice
Componentele metabolice ale sindromului metabolic (de exemplu, tensiunea arterială, glucoza din sânge, trigliceridele și HDL-colesterolul), precum și alte variabile metabolice (colesterolul total, LDL-colesterolul, acidul uric, insulina de post și scorul HOMA) au fost măsurate în subiecții studiați înainte și după reducerea greutății.
Tensiunea arterială a fost măsurată cu un tensiometru cu mercur după 10 minute de repaus în poziția șezând. Toți subiecții studiați s-au abținut de la fumat sau de la ingerarea cofeinei timp de 30 de minute înainte de măsurători. Mărimea manșetei a fost selectată în funcție de circumferința brațului participanților. Prima apariție a sunetului (sunetul Korotkoff de faza 1) a fost utilizată pentru a defini tensiunea arterială sistolică, iar dispariția sunetului (sunetul Korotkoff de faza 5) a fost utilizată pentru a defini tensiunea arterială diastolică (16). Au fost înregistrate două citiri pentru fiecare tensiune arterială sistolică și diastolică și s-a utilizat media fiecărei măsurători. Dacă primele două măsurători diferă cu mai mult de 5 mmHg, s-au obținut citiri suplimentare.
Probele de sânge au fost obținute dimineața după un post de 12 ore peste noapte dintr-o venă antecubitală în tuburi vacutainere care conțin EDTA și ulterior analizate la un laborator central certificat. Glucoza plasmatică a fost măsurată printr-o metodă de glucoză oxidază și nivelurile totale de colesterol și trigliceride prin proceduri enzimatice folosind un autoanalizator (Hitachi-747, Tokyo, Japonia). Fracția HDL-colesterol a fost măsurată prin metoda enzimatică după precipitarea lipoproteinelor care conțin apo-B cu MnCl2. Colesterolul LDL a fost calculat prin ecuația Friedewald dacă trigliceridele au fost sub 400 mg/dL (17). Concentrațiile de acid uric au fost măsurate prin metoda uricazei folosind autoanalizatorul. Insulina de post a fost măsurată prin radioimunotest (Dianabott, Tokyo, Japonia). Estimarea rezistenței la insulină prin scorul HOMA a fost calculată cu formula: insulină serică de post (µU/mL) × glucoză plasmatică de post (mmol/L)/22,5 (18).
Participanții care au 3 sau mai multe dintre următoarele criterii au fost definiți ca având sindromul metabolic; tensiunea arterială: ≥130/≥85 mmHg; glucoză de post: ≥110 mg/dL; hipertrigliceridemie: ≥150 mg/dL; și colesterol HDL scăzut: 102 cm la bărbați și> 88 cm la femei, după cum este detaliat în raportul NCEP ATP III (1).
Program de reducere a greutății
Programul de reducere a greutății a constat în modificarea stilului de viață și farmacoterapie adjuvantă utilizând supresoare ale apetitului. Aportul dietetic de rutină nerestricționat al subiecților a fost evaluat prin rechemare dietetică de 24 de ore. Pentru aceasta, intervievatorii cu experiență și bine instruiți i-au instruit pe respondenți să-și amintească și să descrie toate alimentele și băuturile pe care le-au consumat în ultimele 24 de ore. Înregistrarea fiecărui subiect a fost codificată și tabelele de referință standardizate au fost utilizate pentru a converti porțiunile de uz casnic în greutăți gram. Analiza nutrienților a înregistrărilor a fost cuantificată utilizând un program de analiză nutrițională asistată de computer (CAN, Societatea Nutrițională Coreeană, Seul, Coreea) (19). Deficiențele energetice individuale s-au bazat pe necesitățile de energie estimate calculate dintr-o rată metabolică bazală înmulțită cu un nivel de activitate fizică (20). Rata metabolică bazală a fost evaluată prin ecuația Benedict-Harris. Un dietetician bine instruit a instruit prescripțiile zilnice de energie pentru reducerea greutății.
Regimul alimentar utilizat în acest studiu a fost o dietă echilibrată nu mai puțin de 1.000 kcal/zi compusă din carbohidrați 60% din aportul total de energie, cu un nivel de grăsime sub 30% din calorii. Restricționarea consumului de alcool, fie prin reducerea frecvenței, fie a cantității de băuturi alcoolice, a fost puternic recomandată tuturor subiecților. Cu toate acestea, subiecții au fost liberi să aleagă tipul de alimente și băuturi și să păstreze jurnalele cu alimente înregistrate de trei ori pe săptămână în timpul perioadei de studiu de 12 săptămâni. Dieteticienii au intervievat subiecții în mod regulat, o dată pe lună, și și-au reevaluat aportul total de energie și substanțe nutritive din jurnalele alimentare. Ei au monitorizat pentru a se asigura că fiecare pacient urmează obiceiurile de dietă în funcție de nutriția adecvată recomandată pentru un astfel de subiect.
Nivelul de activitate fizică a tuturor subiecților a fost evaluat folosind un chestionar clasificat în unul dintre următoarele grupuri de nivel de activitate fizică: viață zilnică inactivă, ușor activă (fără exerciții externe), viață zilnică moderată activă (exercițiu formal de mai puțin de 3 ori/săptămână), și viața de zi cu zi foarte activă (exercițiu formal de peste 3 ori/săptămână). Majoritatea subiecților au fost clasificați ca inactivi sau ușor activi. Pe baza nivelului inițial de activitate fizică, subiecții au fost, de asemenea, încurajați să crească niveluri de exerciții zilnice și să reducă timpul petrecut într-un stil de viață sedentar.
Durata inițială a exercițiului a fost de aproximativ 30 de minute, dar a fost progresată la maximum 60 de minute în funcție de capacitățile individuale. Intensitatea exercițiului a fost crescută de la 50% la 85% din ritmul cardiac maxim. Modul de exercițiu a fost determinat de subiecți și a variat de la mers pe jos, mersul cu bicicleta, înotul, mersul pe bicicletă staționară sau mersul pe o bandă de alergare motorizată în condiții de trai nerestricționate. Pe tot parcursul studiului, intervievatorul a monitorizat conformitatea pentru exerciții fizice folosind un jurnal și a reevaluat nivelul de activitate fizică.
Subiecților li s-a prescris un adjuvant care suprimă pofta de mâncare pentru reducerea greutății, deoarece de obicei nu au reușit să controleze greutatea doar cu modificarea stilului de viață. Inhibatorul selectiv al recaptării serotoninei (fluoxetină 40 mg) a fost prescris în timpul programului de reducere a greutății de 12 săptămâni. Subiecții au terminat programul de scădere în greutate de 12 săptămâni și au fost luate reevaluări de urmărire, inclusiv măsurători antropometrice, scanare CT a grăsimii abdominale și variabile metabolice.
Analize statistice
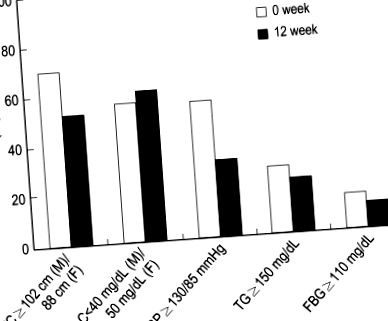
Frecvența fiecărei componente a sindromului metabolic între 0 și 12 săptămâni după programul de reducere a greutății la subiecții studiați. WC, circumferința taliei; HDL-C, HDL-colesterol; TA, tensiune arterială; TG, trigliceride; FBG, glicemie la jeun.
Frecvența fiecărei componente a sindromului metabolic de la momentul inițial până la 12 săptămâni de reducere a greutății a fost modificată după cum urmează; obezitate abdominală (70,5% până la 52,6%), colesterol HDL scăzut (56,4% până la 60,3%), hipertensiune arterială (55,1% până la 30,8%), hipertrigliceridemie (26,9% până la 21,8%) și glicemie cu jeun ridicat (14,1%) ) la 10,3%).
Frecvența grupării componentei metabolice a sindromului metabolic între 0 și 12 săptămâni după programul de reducere a greutății la subiecții studiați. RF, factor de risc.
Frecvența grupării componentei metabolice a sindromului metabolic de la momentul inițial la 12 săptămâni de reducere a greutății a fost modificată după cum urmează; unul sau mai mulți (89,5% până la 82,1%), doi sau mai mulți (79,5% până la 65,4%), trei sau mai mulți (42,3% până la 25,6%) și patru sau mai mulți (11,5% până la 2,6%).
DISCUŢIE
NCEP ATP III a identificat sindromul metabolic ca o țintă secundară a terapiei, dincolo de scăderea colesterolului (1). O analiză prospectivă recentă a componentelor principale a arătat că IMC a fost caracteristica centrală a sindromului metabolic în timp (10). Creșterea IMC a fost, de asemenea, identificată ca un factor de risc independent modificabil al sindromului metabolic la coreeni, în ciuda unei prevalențe mai mici a obezității (12). Reducerea greutății poate juca un rol esențial în prevenirea și gestionarea unui astfel de sindrom metabolic. Recentul studiu finlandez de prevenire a diabetului (21) și Programul de prevenire a diabetului (DPP) (22) au demonstrat eficacitatea chiar și unei reduceri modeste a greutății, produsă de modificări modeste ale dietei și ale activității fizice, în prevenirea diabetului la pacienții supraponderali cu toleranță la glucoză afectată.
Rezultatele studiului nostru indică faptul că o reducere medie a greutății cu 8,1 kg a indus o pierdere de 18,0% din masa totală a grăsimii corporale și 5,4% pierderea masei lipsite de grăsime, cu o reducere de 6,6 cm a circumferinței taliei însoțită de 22,9% din pierderea de grăsime viscerală și 14,3% din pierderea de grăsime subcutanată. Aceste constatări sunt comparabile cu alte rapoarte privind reducerea greutății din diferite țări (23, 24). Descoperirile de mai sus indică, de asemenea, că grăsimea viscerală răspunde mai rapid la reducerea greutății decât grăsimea subcutanată. Acest lucru este în concordanță cu alte rezultate ale studiului că țesutul adipos visceral a fost mai activ din punct de vedere metabolic și lipolitic decât țesutul adipos subcutanat (25). Mai mult, acest studiu arată că reducerea moderată a greutății (9,3% din greutatea corporală inițială) ar duce la reduceri substanțiale ale factorilor de risc metabolici legați de sindromul metabolic sau rezistența la insulină. Dintre diferitele variabile metabolice studiate, insulina de post și scorul HOMA care servesc drept markeri surogat ai rezistenței la insulină, au răspuns mai sensibil la reducerea greutății decât orice alte variabile metabolice.
Se observă în acest studiu că pacienții obezi cu sindrom metabolic pierd, la grade similare, greutatea totală (greutate și IMC) și distribuția grăsimilor (TAT, SAT, TVA, VSR și circumferința taliei) ca indivizi fără sindrom metabolic. Astfel, indică faptul că prognosticul pacienților obezi chiar și cu sindrom metabolic ar putea să nu fie atât de slab dacă acești pacienți încearcă din greu să slăbească. Dacă aplicăm criteriile pentru obezitatea abdominală ca circumferință a taliei peste 90 cm la bărbați și 80 cm la femei, sugerate de orientările Asia-Pacific (26), s-au obținut aceleași rezultate.
În timp ce diferențele dintre modificările variabilelor metabolice dintre participanții cu sau fără sindrom metabolic au fost comparate, tensiunea arterială sistolică și diastolică, glucoza de post, trigliceridele, insulina de post și scorul HOMA au fost semnificativ reduse mai mult la persoanele cu sindrom metabolic, comparativ cu cei fără ea. Acest rezultat indică faptul că există beneficii metabolice mai mari în rândul persoanelor cu sindrom metabolic, în ciuda unui grad similar de reducere a greutății. Această constatare este în concordanță cu studiile anterioare în care eficacitatea reducerii greutății ca strategie terapeutică a fost deosebit de utilă pentru persoanele cu niveluri anormale de factori de risc metabolici (27, 28). Alte studii au arătat, de asemenea, că reducerea greutății îmbunătățește rezistența la insulină (29, 30) și persoanele cu rezistență la insulină pot pierde în greutate la fel de eficient ca și persoanele sensibile la insulină (31).
În ceea ce privește variabilele predictive pentru îmbunătățirea componentelor metabolice, reducerea raportului de grăsime visceral-subcutanată (VSR) s-a dovedit a fi variabila predictibilă independentă pentru îmbunătățirea glicemiei și a trigliceridelor în repaus, iar schimbarea circumferinței taliei a fost semnificativă. legate de îmbunătățirea insulinei în repaus alimentar și a scorului HOMA. Acest lucru ar însemna că reducerea distribuției grăsimii abdominale joacă un rol important în îmbunătățirea componentei metabolice și a rezistenței la insulină, independent de modificarea greutății sau a IMC.
După reducerea greutății la pacienții obezi, frecvența fiecăruia sau gruparea factorilor de risc metabolici a fost semnificativ redusă. Comparativ cu începutul intervenției acestui program, frecvența sindromului metabolic a fost redusă de la 42,3% la 25,6% (reducere de 40%) după reducerea greutății. Astfel de descoperiri atrag atenția că, în ciuda persistenței obezității chiar și după reducerea greutății, chiar și o reducere modestă a greutății poate duce la îmbunătățirea semnificativă din punct de vedere clinic și statistic a sindromului metabolic. Dacă aplicăm criteriile sindromului metabolic stabilite de OMS (32), frecvența sindromului metabolic ar fi mai mică decât cea care ar fi fost evaluată de NCEP ATP III.
Limitările acestui studiu nu se generalizează la populația normală în greutate și nu au putut observa efectul reducerii greutății asupra sindromului metabolic la participanți în conformitate cu respectarea programului de reducere a greutății.
În concluzie, o reducere moderată a greutății a fost asociată cu o reducere substanțială a factorilor de risc metabolici ai sindromului metabolic sau rezistenței la insulină la pacienții obezi care păreau parțial mediată de reducerile corespunzătoare ale distribuției grăsimii abdominale. Beneficiul reducerii greutății s-a dovedit a fi mai mare la persoanele cu sindrom metabolic decât la cei fără sindrom metabolic. Sunt necesare viitoare studii clinice pentru a dezvolta metode ideale pentru a menține aceste beneficii ale reducerii greutății la pacienții cu sindrom metabolic.
- Efectul reducerii greutății asupra parametrilor de vâscozitate a sângelui la femeile obeze - IOS Press
- Efectul orlistatului asupra controlului glicemic la pacienții supraponderali și obezi cu diabet de tip 2
- Efectul milnacipranului asupra greutății corporale la pacienții cu fibromialgie
- Eficacitatea programelor comerciale de slăbire în sindromul metabolic - Coletta - 2016 - The FASEB
- Efectul pierderii în greutate asupra incontinenței urinare la femeile supraponderale și obeze Rezultate la 12 și 18 ani