Karin Spiller, DVM
Spitalul de Referință Veterinară din Massachusetts, Woburn, MA
Postat pe 06.06.2017 în Urgență și îngrijire critică
Marijuana este drogul ilicit cel mai frecvent utilizat în Statele Unite și, având în vedere numărul crescut de state care permit utilizarea acestuia din punct de vedere medical și recreativ, este obligatoriu să existe un impact asupra medicinei veterinare. Există dovezi din ce în ce mai mari că marijuana are valoare medicinală, dar, la fel ca toate drogurile, are și efecte dăunătoare. Marijuana poate fi găsită în multe forme diferite, iar acest lucru are implicații pentru prezentarea și severitatea intoxicațiilor observate la animale. În ultimii ani, utilizarea și prevalența produselor care conțin canabinoizi au crescut.
Cunoscută în mod obișnuit ca familia cânepei, Cannabacea este alcătuită din două genuri de importanță economică. Humulusul este sursa de hamei folosită la fabricarea berii. Canabisul, dintre care Cannabis sativa este principala specie, este una dintre cele mai vechi plante cultivate din lume. C. sativa conține mai mult de 400 de compuși, dintre care mai mult de 60 sunt canabinoizi. Cel mai abundent și activ din punct de vedere farmacologic dintre canabinoizi este Δ-9-tetrahidrocanabinol (THC sau Δ-9-THC). Δ-9-THC este un ulei volatil cu solubilitate ridicată a lipidelor și se leagă ușor de sticlă și plastic. Alte cannabinoide găsite în C. sativa sunt Δ-8-THC, cannabigerol (CBG) și cannabidiol (CBD), care, spre deosebire de THC, sunt minim psihoactive.
Termeni
- Marijuana: se referă la orice parte a plantei de canabis, dar, în general, utilizată cu referire la frunzele, tulpinile și mugurii săi uscați
- Haşiş: o rășină extrasă din mugurii înfloriți ai plantei C. sativa, are de obicei o concentrație foarte mare de THC
- Ulei de haș: obținut din planta de canabis prin extracția solventului, iar solvenții sunt evaporați pentru a lăsa un ulei foarte concentrat care poate fi afumat, ingerat sau aplicat local
- Endocannabinoizi: derivați ai acidului arahidonic precum anandamida care sunt produși în organism
- Fitocanabinoizi: compușii găsiți în planta C. sativa, inclusiv cei mai relevanți din punct de vedere medical, THC și canabidiolul
- Canabinoizi sintetici: analogi de THC și canabidiol produși în laborator
Tendințe
Studiile au descoperit rate crescute de expuneri pediatrice neintenționate în state care au adoptat legislația privind marijuana. În ultimii cinci ani, Linia de asistență pentru otrăvurile pentru animale de companie a înregistrat o creștere cu 330% a numărului de cazuri de ingerări de marijuana la animalele de companie.
Deși disponibilitatea mai mare și posibilitatea de expunere pot fi unul dintre factorii principali în creșterea cazurilor, modificările produsului în sine pot fi responsabile pentru severitatea crescută a semnelor clinice și, prin urmare, necesitatea tratamentului medical. Majoritatea expunerilor neintenționate la marijuana la copii mici provin din marijuana medicală, adesea sub forma unui comestibil. Având în vedere gustul lor și concentrațiile mai mari de THC, alimentele pot crește probabilitatea de ingestie și pot provoca semne clinice mai severe.
Produse
Conținutul de THC în marijuana variază considerabil, în funcție atât de tehnicile de cultivare (cantitatea de lumină, umiditate, tipul solului, pH-ul solului, nutrienți și îngrășăminte), cât și de modul în care este luat. Hashish poate avea aproximativ 6-10% THC, iar uleiul de hash în jur de 20-60% THC. O țigară tipică de marijuana conține, în general, 15-30 mg de THC. Produsele comestibile pot conține cantități foarte mari de THC (100-500mg). Aceste produse pot fi realizate cu unt de THC, produs prin fierberea plantei pentru a extrage THC. Se adaugă unt pentru a absorbi THC și materialul vegetal este apoi strecurat.
Mecanismul de toxicitate și efecte
Există doi receptori principali, receptorii canabinoizi 1 și 2 (CB1 și CB2). CB1 este receptorul la care acționează THC și este responsabil pentru efectele sale psihoactive. Acest receptor cuplat cu proteina G se găsește atât în SNC, cât și în mai multe locații din corp. Activarea receptorilor în anumite zone, cum ar fi cerebelul și ganglionii bazali, are ca rezultat semne clinice de incoordonare. Acțiunea THC în hipotalamus se manifestă la oameni ca „munchies”, cauzată de stimularea regiunii care controlează consumul de alimente. Receptorii CB1 au fost, de asemenea, descoperiți în splină, piele, suprarenale, pancreas, inimă, plămâni și părți ale tractului urogenital și GI. Receptorii CB2 se găsesc în principal în splină și celulele imune și se crede că au un rol în suprimarea imunității.
Deși o cale de expunere mai puțin frecventă, pacienții veterinari pot fi expuși fumului de canabis la mâna a doua. Se raportează că THC inhalat are un efect bronhodilatator, dar acest efect este efemer și foarte ușor. Fumul de canabis poate fi iritant pentru țesuturile conjunctivale, nazofaringiene și bronșice, ducând la injecție conjunctivală și sinuzită.
În mod acut, dozele de THC mici până la moderate determină o creștere a ritmului cardiac (care poate ajunge până la 50%). S-a raportat că dozele mari provoacă bradicardie.
Farmacocinetica
Absorbția canabinoizilor depinde de calea de expunere. Inhalarea are ca rezultat absorbția rapidă prin plămâni, iar Δ-9-THC poate fi detectat în câteva secunde în plasmă. Concentrațiile plasmatice maxime apar în câteva minute și semnele persistă rar după câteva ore.
Ingerarea are ca rezultat o absorbție mai întârziată și mai neregulată. În sânge, aproape 90% din THC se găsește în plasmă și se leagă de proteinele plasmatice. Metabolismul hepatic se realizează în principal prin izoenzime ale citocromului P-450. Mai mult de jumătate din canabis este excretat prin fecale și aproximativ 20% prin urină.
Deoarece THC intră rapid în țesuturi foarte vascularizate, cum ar fi ficatul, inima, plămânii, splina, mușchii și grăsimea, se observă o scădere dramatică a concentrației plasmatice. După ingestie, efectele psihotrope sunt observate în 30-90 de minute, iar efectele de vârf sunt observate în 2-4 ore. Natura extrem de lipofilă a THC îi permite să se acumuleze în țesutul adipos și este redistribuită încet din depozitele de grăsime înapoi în sânge. La câini, durează aproximativ 5 zile pentru ca 80-90% din THC să fie excretat din corp.
Doze de expunere
În ciuda dezvoltării semnelor clinice moderate la doze mici, toxicitatea generală a canabinoizilor este scăzută. Au fost raportate semne cu expuneri de până la 85 mg/kg. Experimental, moartea a fost observată la șobolani la 1 g/kg pe cale orală, dar letalitatea nu a fost observată la beagles sau maimuțele rhesus la 3-9 g/kg. O sursă menționează LD50 oral la câini ca 3 g/kg și pisici 200 mg/kg. Utilitatea determinării dozei de expunere are o valoare clinică discutabilă, deoarece dozele toxice și letale nu sunt bine stabilite.
Semne clinice
Prezentarea clasică a unui câine care a fost expus la marijuana implică de obicei o combinație de ataxie, incontinență urinară și dezorientare. Într-un studiu pe 213 de câini cu expunere presupusă sau confirmată la THC, 99% au prezentat semne neurologice. Acestea includ depresie, ataxie, tremurături, convulsii, midriază, ochi sticloși, dezorientare, hiperestezie, hiperactivitate, mișcarea capului, culcare și stupoare. S-a raportat smulgerea muștelor la pisici. Efectele SNC pot fi explicate atât de activitatea la receptorii CB, cât și de faptul că THC afectează o varietate de neurotransmițători. THC crește activitatea GABA, ceea ce duce la o inhibare crescută a creierului care duce la depresia SNC. Semnele SNC sunt de obicei de scurtă durată și durează de obicei 4-6 ore. Timpii de recuperare în general pot fi de până la 5 zile, în funcție de doza de expunere.
Deși THC are proprietăți antiemetice, poate provoca vărsături. Acest lucru se poate datora efectelor iritante ale materialului vegetal asupra mucoasei gastrice sau dacă a fost consumată și o altă substanță despre care se știe că provoacă vărsături (de exemplu, ciocolată). Toxicitatea combinată a marijuanei și a ciocolatei a apărut la 21% dintre câinii expuși la marijuana într-un studiu realizat de Meola și colab. Acest studiu a constatat, de asemenea, că 47% dintre câinii au prezentat incontinență urinară, care este mult mai mare decât cea raportată anterior și nu este un efect observat la oameni. Acest lucru se poate datora unui metabolit THC urinar suplimentar produs în mod unic la câini. Alte semne clinice care au fost raportate la câini: hipersalivație, tahie sau bradicardie și hipo- sau hipertermie.
Diagnostic
Există o multitudine de alte toxine cunoscute pentru a provoca depresia SNC, iar acestea trebuie considerate ca fiind diagnostice diferențiale. Acestea includ: etanol, etilen glicol, ivermectină, opioide, barbiturice, benzodiazepine, fenotiazine, amfetamine, antihistaminice și antidepresive triciclice.
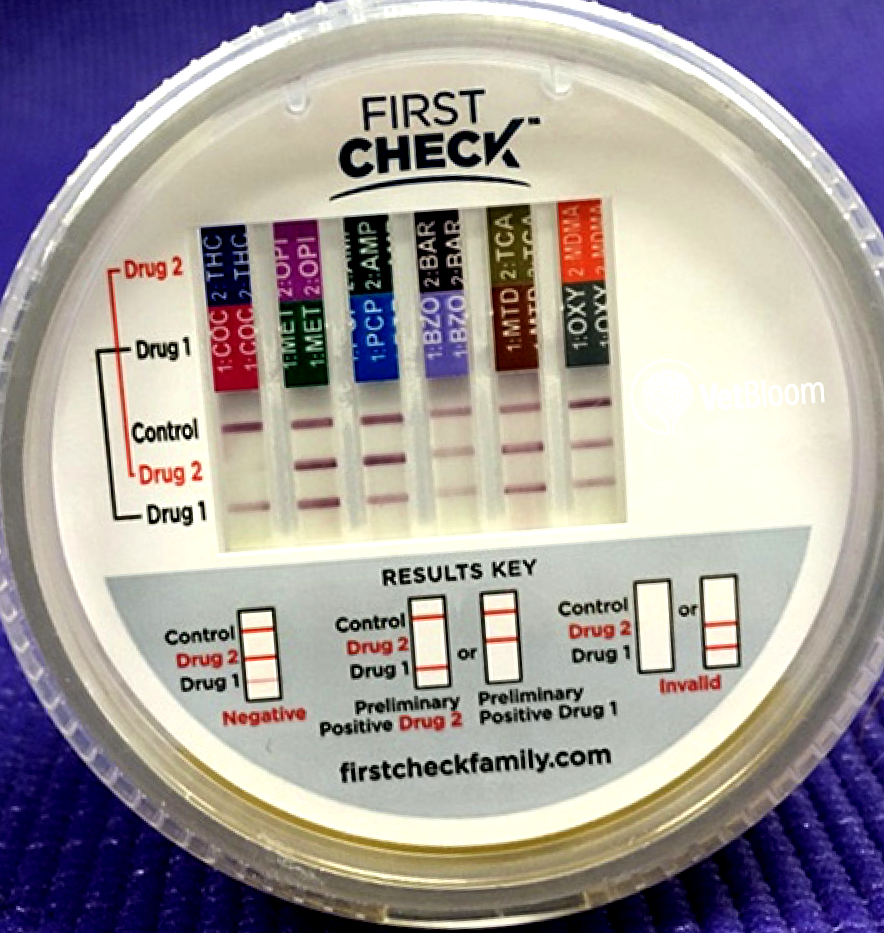
Test de droguri în urină la un câine cu toxicoză de marijuana. THC este medicamentul 2 pe banda 1 - lipsa unei linii indică un rezultat pozitiv al testului. Imagine oferită de Dr. Mark Troxel, neuropetvet.com.
Diagnosticul definitiv poate fi dificil și se bazează de obicei aproape în întregime pe prezentarea clinică. Marijuana nu provoacă tulburări clinicopatologice specifice. Canabinoizii sunt detectabili în conținutul stomacului, urină, păr, salivă și plasmă. Urina este proba preferată la om din cauza concentrației mai mari și a timpului mai mare de detectare a metaboliților. În acest moment, nu există niciun test științific care să detecteze în mod fiabil THC în urina pacienților canini. (Cu toate acestea, un rezultat pozitiv pentru THC poate fi util, deoarece există puțini falsi pozitivi cu acest test.) Analiza urinei canine a arătat metaboliți diferiți produși în concentrații diferite de cei găsiți în urina umană. Multe teste de depistare a medicamentelor pentru urină disponibile în comerț detectează cel mai frecvent metabolit găsit în urina umană, 11-OH-Δ-9-THC. Acest lucru poate explica rata ridicată a falselor negative la canini, precum și testarea prea recentă după expunere și manipularea necorespunzătoare a probelor (THC se leagă de cauciuc și sticlă).
Tratament
Majoritatea cazurilor sunt ușor până la moderat afectate și pot fi tratate în ambulatoriu cu lichide SQ, +/- un antiemetic și în timp. Prognosticul este favorabil excelent pentru pacienții simptomatici. Spitalizarea trebuie luată în considerare la pacienții grav afectați (de exemplu vărsături intratabile, hipotensive, obținute) sau pentru tratamentul co-intoxicațiilor. Cu îngrijire de susținere, recuperarea este de obicei în termen de 72 de ore.
Decontaminare
- Inducerea emezei
- Apomorfină 0,03-0,04mg/kg IV
- Dacă expunerea recentă și calea de expunere au fost orale
- Spălare orogastrică sub anestezie generală
- Luați în considerare dacă expunerea este mare
- Cărbune activat
- Prima doză cu cathartic
- 1-2g/kg q8h x24h (recirculare enterohepatică)
Îngrijire de susținere
- Fluide IV
- Îngrijire culcată
- Flip laterale q4h
- +/ -Catheter urinar intern?
- Luați în considerare dacă comatoză sau co-intoxicație (ciocolată)
- Anti-emetic
- Cerenia 1mg/kg IV sau SQ q24h
- Ondansetron 0,2 mg/kg IV q12-24h
- Dolasetron 0,6mg/kg IV q24h
- Sedare (anxietate, stimulare severă a SNC)
- Butorfanol 0,1-0,4mg/kg IV
- Midazolam 0,2 mg/kg IV
- Acepromazină 0,01-0,05mg/kg IV
- Cutremure, convulsii
- Diazepam 0,25-0,5mg/kg IV
- Bradicardie severă
- Atropină 0,02-0,04mg/kg IV, IM sau SQ
- Hiperestezie
- Mediu întunecat și liniștit, cu stimulare minimă
- Bile de bumbac în urechi
- Suport de căldură
- Monitorizați elementele vitale
- Mentare, TPR, TA 2-4h
- Lipide (emulsie intravenoasă de lipide/ILE)
- Compuși lipofili (anestezice locale, permetrine, ivermectină)
- Bolus inițial (1,5 ml/kg timp de 2-3 minute) urmat de un CRI (0,25 ml/kg/min x 30-60 minute)
Produse umane
- Dronabinol (Marinol)
- Agonistul receptorului CB1, conține THC derivat sintetic
- Substanța controlată din anexa III
- FDA a aprobat tratamentul greaței și vărsăturilor induse de chimioterapie (CINV) și anorexiei legate de SIDA și scăderii în greutate
- Nabilone (Cesamet)
- CB1 agonist, un analog sintetic al THC
- FDA a aprobat tratamentul CINV
- Programul II
- Nabiximoli (Sativex)
- Extract din plante întregi de marijuana
- Studii clinice în SUA pentru tratamentul durerii. (Aprobat în Europa, Canada pentru tratamentul spasticității asociate cu scleroza multiplă și durerea neuropatică)
Canabinoizi sintetici („marijuana sintetică”; K2, condiment)
Conține ierburi pe lângă compuși sintetici canabinoizi și interacționează cu receptorii CB. Pacienții umani prezintă anxietate, paranoia, agitație și iluzii; semnele clinice includ tahicardie, gură uscată și injecție conjunctivală. Există date limitate privind expunerile la animale, dar semnele frecvente raportate la linia de asistență pentru otrăvurile pentru animale de companie includ ataxia, vărsăturile, hipersalivarea, incontinența urinară, zvâcniri, hiperestezie și midriază; nu au fost raportate decese. Decontaminarea trebuie efectuată, dacă este cazul. Agitația sau stimularea SNC pot fi tratate cu benzodiazepine sau fenotiazine. Recuperarea este așteptată în 24-48 de ore.
Lectură suplimentară
- Fitzgerald K, Bronstein A, Newquist K. Marijuana Poisoning. Top Companion Anim Med 2013; 28: 8-12.
- Gwaltney-Brant S, Meadows I. Utilizarea emulsiilor lipidice intravenoase pentru tratarea anumitor cazuri de otrăvire la animale mici. Vet Clin Small Anim 2012; 42: 251-262.
- Janczyk P, Donaldson C, Gwaltney S. Două sute și treisprezece cazuri de toxicoze de marijuana la câini. Vet Toxicol uman 2004; 46 (1): 19-21.
- Meola S, Tearney C, Haas S și colab. Evaluarea tendințelor în toxicoza marijuanei la câinii care trăiesc într-un stat cu marijuana medicală legalizată: 125 câini (2005-2010). J Vet Emerg Crit Care 2012; 22 (6): 690-96.
- Teitler J. Evaluarea unui test de urină la fața locului cu medicamente multidrog pentru utilizare de urgență la câini. J Am Anim Hosp Assoc 2009; 45: 59-66.
Despre autor
Dr. Karin Spiller este originară din California de Nord și a primit diploma de licență de la UC Berkeley. A urmat o școală veterinară la Universitatea de Stat din Washington și a finalizat un stagiu rotativ pentru animale mici la Clinica de specialitate veterinară și urgență din Pittsburgh, în vestul Pennsylvania. Dr. Spiller s-a alăturat echipei de urgență și îngrijire critică la Mass Vet în iulie 2016.
- Marijuana Pro-Tips Cum am pierdut 50 de kilograme folosind canabis
- Jefferson a pierdut 170 de kilograme în ani Blogul Beachbody
- Am pierdut 20 de lire sterline în 60 de zile, aflu cum este blogul Beachbody
- Cum am slăbit 20 kg după naștere Sănătatea sarcinii; Fitness, Pierdere în Greutate Blog Postat de Maahi Sareen
- Pierderea greutății bebelușului De ce contează cel mai mult primul an după naștere; Sarcina Blogului Baby2Body;