Li-Long Pan
1 Școală de Medicină, Universitatea Jiangnan, Wuxi, China
Jiahong Li
2 Laborator cheie de stat de știință și tehnologie alimentară, Universitatea Jiangnan, Wuxi, China
3 Laborator de nutriție și imunologie, Școala de știință și tehnologie a alimentelor, Universitatea Jiangnan, Wuxi, China
Muhammad Shamoon
2 Laborator cheie de stat de știință și tehnologie alimentară, Universitatea Jiangnan, Wuxi, China
3 Laborator de nutriție și imunologie, Școala de știință și tehnologie a alimentelor, Universitatea Jiangnan, Wuxi, China
Madhav Bhatia
4 Grupul de cercetare a inflamației, Departamentul de patologie, Universitatea din Otago, Christchurch, Noua Zeelandă
Jia Sun
2 Laborator cheie de stat de știință și tehnologie alimentară, Universitatea Jiangnan, Wuxi, China
3 Laborator de nutriție și imunologie, Școala de știință și tehnologie a alimentelor, Universitatea Jiangnan, Wuxi, China
Abstract
Pancreatita acută (AP) este o tulburare inflamatorie acută abdominală frecventă și principala cauză a internării în spital pentru tulburări gastro-intestinale în multe țări. Manifestările clinice ale AP variază de la inflamația locală autolimitată la stări patologice sistemice devastatoare care determină morbiditate și mortalitate semnificative. Până în prezent, în ciuda eforturilor extinse în traducerea unor ținte terapeutice experimentale promițătoare în studiile clinice, remedierea eficientă specifică bolii rămâne obscură, iar îngrijirea de susținere a fost în continuare tratamentul primar pentru această boală. Dovezile emergente, în lumina stării actuale a fiziopatologiei AP, au evidențiat faptul că inițierea strategică a nutriției cu suplimente nutriționale adecvate sunt cheia pentru a limita inflamația locală și pentru a preveni sau gestiona complicațiile asociate AP. Revizuirea actuală se concentrează pe progresele recente privind intervențiile nutriționale, inclusiv strategiile de nutriție enterală versus parenterală, și suplimentele nutriționale, cum ar fi probioticele, glutamina, acizii grași omega-3 și vitaminele din AP clinică, în speranța de a avansa cunoștințele și practicile actuale legate de nutriție și nutriție. suplimente în managementul clinic al AP.
Introducere
tabelul 1
| Atlanta 2012 a | Blând | × | × | × | × | (10, 11) |
| Moderat | √ | √ | × | √ | ||
| Nord | √ | × | √ | √/× | ||
| Bazat pe determinant b | Blând | × | × | × | n/A | |
| Moderat | Steril | √ | × | n/A | ||
| Nord | Infectat | √ | √ | n/A | ||
| Critic | Infectat | × | √ | n/A |
AP, pancreatită acută; EPC, exacerbarea comorbidității preexistente; N/A, nu se aplică; POF, insuficiență persistentă a organelor; TOF, insuficiență tranzitorie a organelor; √, da; ×, nu.
a În Atlanta 2012, complicațiile locale sunt subcategorizate (edematoasă interstițială, pancreatită necrotizantă, pancreatită necrotizantă infectată, alte complicații locale etc.), în timp ce complicațiile sistemice sunt definite ca TOF sau POF sau un EPC (insuficiență de organ care persistă> 48 h; trei sisteme de organe = renal, respirator, cardiovascular; scor mareșal ≥2).
b Sistemul de evaluare a insuficienței organice legate de sepsis este utilizat pentru a defini insuficiența organelor, iar pentru pancreatita severă, fie POF, fie necroza infectată este obligatorie.
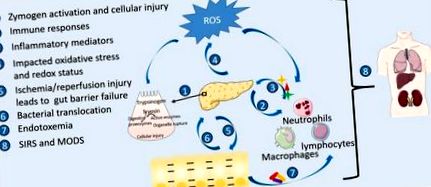
Fiziopatologia pancreatitei acute care evidențiază locurile de acțiune prin nutriție. Stresul etiologic declanșează activarea prematură a zimogenilor digestivi și a leziunilor celulare intraacinare cu stresul oxidativ însoțitor. Implicarea celulelor imune cu mediatori inflamatori eliberați și stresul oxidativ amplificat exacerbează cascada inflamatorie. Inflamația intestinală și eșecul barierei apar în urma răspunsurilor inflamatorii sistemice, tulburări vasculare și leziuni de ischemie/reperfuzie secundare inflamației pancreatice. Funcția de barieră întreruptă duce în continuare la translocație bacteriană, infecție pancreatică și necroză și endotoxemie, responsabilă în cele din urmă de sindromul disfuncției organelor multiple (MODS) și de deces.
O mai bună înțelegere a fiziopatologiei AP a atras eforturi de cercetare pentru restabilirea homeostaziei imune și a organelor/țesuturilor în PA clinică și spre dezvoltarea de noi strategii de intervenție (20). Cu terapii farmacologice farmacologice încă obscure, dezvoltarea strategiilor de gestionare din studiile clinice randomizate este esențială în prevenirea complicațiilor sistemice în timpul PA severe. Sprijinul și intervenția nutrițională sunt o parte importantă a managementului clinic al pacienților cu AP (21, 22).
Intervenție nutrițională în AP clinică
Intervenții nutriționale vizate pe parcursul întregului episod de pancreatită acută. Intervenții nutriționale vizate: nutriție enterală sau parentală și suplimente nutritive, inclusiv imunonutrienți antiinflamatori, antioxidanți și probiotice sunt prezentate în etapa de administrare.
Abordările strategice de includere a suplimentelor nutritive au fost, de asemenea, încercate să ofere efecte imunitare suplimentare de reglare și antioxidante. S-a demonstrat că probioticele și prebioticele stabilizează homeostazia barierei intestinale perturbate și sunt benefice în reducerea ratei de infecție în studiile clinice primare (28-31). Datorită naturii imunosupresoare și inflamatorii a bolii, imunonutrienții precum glutamina și acizii grași omega-3 (ω-3 FAs) au fost adăugați la formulele parenterale sau enterale pentru a modula funcțiile imune, pentru a suprima răspunsurile hiperinflamatorii și pentru a restabili țesutul și organul. homeostazia în practica clinică (21, 32, 33). Suplimentele cu proprietăți antioxidante precum glutamina și vitamina C au fost, de asemenea, sugerate pentru a oferi efecte benefice suplimentare (34).
Revizuirea își propune să ofere o analiză cronologică cuprinzătoare a ultimelor studii clinice privind strategiile EN versus PN și suplimentele nutriționale, inclusiv probiotice (prebiotice și sinbiotice), glutamină,-3 FA și vitamine, sperând să ofere baza pentru dezvoltarea viitoare a nutriției strategii în AP clinică.
EN versus PN
Suplimente nutritive
Probiotice, Prebiotice și Sinbiotice
Modificările motilității intestinale și ale microbiomului, ale răspunsului imun și ale funcției de barieră mucoasă în timpul AP duc la translocația bacteriană și la infecția ulterioară a necrozei pancreatice, care este una dintre principalele cauze de complicații și deces la pacienții cu AP severă (45). Rolurile potențiale ale probioticelor au fost propuse pentru beneficii imunomodulatoare și de promovare a sănătății pentru restabilirea integrității intestinului, modularea răspunsurilor imune împotriva agenților patogeni invadatori și prevenirea proliferării bacteriilor dăunătoare dincolo de cele ale nutriției de bază, care au fost evaluate în mai multe studii clinice ( Tabel (Tabel2 2).
masa 2
Caracteristicile studiilor clinice privind tratamentul probiotic în AP.
| Olah și colab. (46) | Lactobacillus plantarum 299 plus fibră de ovăz (10 9 × 2/doză zilnică) | Fibre + simbiotice + EN + versus fibre + simbiotice inactivate la căldură + EN | - | - | Nicio diferenta | Nicio diferenta | Nicio diferenta | Infection infecție pancreatică care necesită operație în brațul probiotic | Nicio diferenta |
| Kecskes și colab. (47) | L. plantarum 299 plus fibră de ovăz | + Fibre + simbiotice + versus + fibre + simbiotice inactivate la căldură + EN | - | - | ↓ în braț simbiotic | - | - | - | |
| Olah și colab. (48) | Multistrain (40 × 10 9/doză zilnică) și multifibre | EN + fibre versus EN + fibre + simbiotic | - | - | ↓ în braț simbiotic | ↓ SIRS + MODS în braț simbiotic | ↓ intervenții chirurgicale în brațul probiotic | Nicio diferenta | |
| Qin și colab. (49) | L. plantarum (tulpină nespecificată) (10 10/doză zilnică) | TPN versus PN + EN + probiotice parțiale | Excreție urinară de lactoză/ramnoză | ↓ în brațul probiotic | - | ↓ SIRI în brațul probiotic | ↓ MODS în brațul probiotic | ↓ Complicații infecțioase la brațul probiotic | Nicio diferenta |
| Karakan și colab. (50) | Multifibre | EN + multifibre versus EN | - | - | - | Nicio diferenta | Nicio diferenta | - | Nicio diferenta |
| Besselink și colab. (51) | Produs multistrat (10 10/doză zilnică) plus maltodextrine și amidon de porumb | EN + placebo versus EN + probiotice | - | - | Nicio diferenta | - | ↑ MODS în brațul probiotic | Nicio diferenta | ↑ în brațul probiotic din cauza NOMI |
| Besselink și colab. (52) | Produs multistrain (10 10/doză zilnică) | EN + placebo versus EN + probiotice | PEG excreție urinară | Nicio diferenta | - | - | - | - | - |
| Sharma și colab. (53) | Produs multistrain (10 10/doză zilnică) | Placebo versus probiotice (prin modul actual de hrănire) | Excreție urinară de lactoză/ramnoză | Nicio diferenta | - | - | Nicio diferenta | ↓ anticorp endotoxinic IgG, IgM în brațul probiotic | Nicio diferenta |
| Cui și colab. (54) | Produs multistrain 1 × 10 11/12 h | PN versus EN versus EN + probiotice (PN) | - | - | ↓ în brațul EN și brațul EN + cu probiotice | - | - | - | Nicio diferenta |
AP, pancreatită acută; EN, nutriție enterală; MODS, sindromul disfuncției organelor multiple; PN, nutriție parenterală; SIRS, sindrom de răspuns inflamator sistemic; TPN, nutriție parenterală totală.
Glutamina
Glutamina este un component important al grupului de aminoacizi intra și extracelular, cu efecte imunomodulatoare și antioxidante, iar epuizarea sa a fost demonstrată în bolile critice (58). Glutamina îmbunătățește funcțiile celulelor imune și contribuie la apărarea antioxidantă. De asemenea, poate susține integritatea intestinală și poate reduce translocația bacteriană; prin urmare, reduceți răspunsurile inflamatorii sistemice și sepsisul, care sunt importante în bolile critice, cum ar fi AP (33).
Tabelul 3
Caracteristicile studiilor clinice pe glutamină ca supliment nutritiv în AP.
- Revizuirea sistematică și meta-analiza formulărilor de nutriție enterală în pancreatita acută - PubMed
- Tulburări legate de nutriție și anxietate; Centrul de tratament TOC
- Pancreatită acută recurentă în anorexie și bulimie Insight Medical Publishing
- Specialist în pancreas în Grapevine, TX Doctor în nutriție pentru pancreatită
- Tratament nutrițional și ibogaină; Tratamentul cu ibogaină pentru dependență