Și Harrison
1 Facultatea de Științe Medicale și Umane, Universitatea din Manchester, Manchester, Marea Britanie
S Hayes
1 Facultatea de Științe Medicale și Umane, Universitatea din Manchester, Manchester, Marea Britanie
L Howell
2 Departamentul de histopatologie, Salford Royal NHS Foundation Trust, Salford, Marea Britanie
S Lal
1 Facultatea de Științe Medicale și Umane, Universitatea din Manchester, Manchester, Marea Britanie
Abstract
Biopsiile din a doua parte a duodenului sunt efectuate în mod obișnuit la pacienții cu scădere în greutate neintenționată. Când se detectează atrofia vilozitară și o limfocitoză intraepitelială crescută, cea mai frecventă cauză a acesteia este boala celiacă. Atrofia viloasă severă cu limfocitoză intraepitelială crescută (Marsh IIIc) este foarte specifică pentru boala celiacă. Cu toate acestea, boala celiacă cu această prezentare este foarte rară. Anomalii mai ușoare, cum ar fi Marsh I-II (enterită microscopică) și Marsh IIIa, nu sunt specifice bolii celiace și ar putea apărea în alte condiții, cum ar fi cele enumerate în discuție. Prezentăm cazul unei femei în vârstă de 74 de ani care, după ce a fost diagnosticată cu boală celiacă seronegativă, nu a reușit să se îmbunătățească cu o dietă fără gluten. Discutăm diagnosticul diferențial al bolii celiace și posibilele cauze alternative ale tocirii viloase, acordând o atenție deosebită diagnosticului de creștere excesivă a bacteriilor intestinale subțiri.
fundal
Pierderea în greutate neintenționată, cu sau fără simptome gastrointestinale (GI) asociate, este o indicație obișnuită pentru trimiterea la un specialist. Biopsiile intestinului subțire sunt efectuate în mod obișnuit ca parte a procesului de diagnosticare. Când se detectează atrofia viloasă, cea mai frecventă cauză este boala celiacă. 1 Cu toate acestea, trebuie luate în considerare și diagnosticele alternative, deoarece eșecul în acest sens poate duce la un diagnostic ratat și la o malabsorbție continuă, ceea ce duce la morbiditate suplimentară. Acest caz evidențiază importanța corelației clinicopatologice detaliate; este necesară luarea în considerare a unor diagnostice alternative atunci când un pacient, considerat inițial că are boală celiacă pe baza constatărilor histologice, nu reușește să se îmbunătățească după adoptarea unei diete fără gluten.
Prezentarea cazului
O femeie în vârstă de 74 de ani, nefumătoare, a fost trimisă pentru a doua opinie gastroenterologică pentru a stabili cauza pierderii în greutate și a simptomelor gastrointestinale.
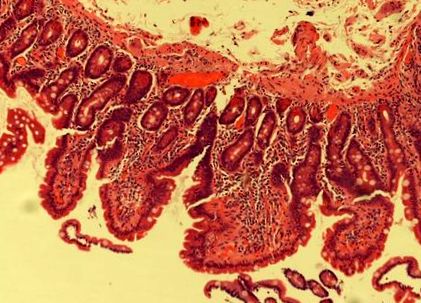
Cu zece luni înainte de această recomandare, ea se prezentase unui alt gastroenterolog cu antecedente de 11 luni de pierdere în greutate neintenționată (6 kg), apetit redus și greață în creștere. Nu avea alte simptome gastrointestinale sau alte antecedente medicale semnificative. La acel moment, anticorpii antiendomiziali (EMA) erau negativi. O scanare CT a toracelui, abdomenului și bazinului a fost normală. Gastroscopia nu a fost remarcabilă, deși biopsiile duodenale au prezentat dovezi de atrofie viloză cu o limfocitoză intraepitelială crescută (figura 1). Pe baza acestor investigații, a fost diagnosticată boala celiacă seronegativă. A început o dietă fără gluten. O lună mai târziu, pacientul a raportat scaune compatibile cu steatoreea. Tatăl ei murise de cancer pancreatic, la vârsta de 53 de ani. Un RMN al pancreasului era normal, dar elastaza fecală era scăzută (200). Culturile de scaune pentru ovule, chisturi și paraziți au fost negative.
Revizuirea de specialitate a scanării CT anterioare a exclus boala vasculară mezenterică și orice altă patologie semnificativă. O urmă de bariu a arătat o ușoară proeminență a pliurilor intestinului subțire, dar acest lucru nu a fost considerat patologic. O absorptiometrie cu raze X cu energie dublă a arătat osteoporoză. Colonoscopia a arătat o boală diverticulară; biopsiile colonice aleatorii au exclus colita microscopică.
Biopsiile duodenale repetate au arătat din nou o arhitectură viloză tocită cu o limfocitoză intraepitelială asociată. Analiza de specialitate nu a găsit dovezi histologice ale limfomului.
A fost efectuat un test de respirație glucoză/hidrogen. Nivelul de hidrogen a crescut peste nivelul maxim detectabil (> 150 ppm). Partea glicocolat a testului a fost negativă (0,5% la 6 ore (figura normală 2). Atât un test combinat de glucoză hidrogen/metan, cât și un test de respirație glicocolat au fost negative. Următorul pas în managementul ei va fi restabilirea normală a glutenului dieta și rebiopsia în viitor.
Imagine cu microscopie luminoasă a biopsiei duodenale repetate (colorare H&E) realizată după rezolvarea simptomelor.
Discuţie
Acest pacient a prezentat o pierdere semnificativă în greutate însoțită de simptome GI nespecifice. Deoarece biopsiile duodenale au arătat dovezi de atrofie viloasă și limfocitoză intraepitelială, diagnosticul inițial dat a fost boala celiacă. Aceasta este o boală autoimună obișnuită care afectează aproximativ 1% din populația Regatului Unit. 2 3 Prezentarea sa poate include simptome de scădere în greutate, anorexie, dureri abdominale, alterarea obiceiurilor intestinale (diaree, steatoree sau constipație); alternativ, poate fi asimptomatic. 4 5 La diagnostic, pot fi prezente deficiențe nutriționale biochimice, cum ar fi folatul și zincul. 5 6
Diagnosticul bolii celiace depinde de prezența constatărilor histologice cheie, susținute de simptome compatibile și serologie (de exemplu, EMA și anti-tTG). Diferite metode de testare disponibile în comerț au sensibilități și specificități diferite. O meta-analiză din 16 studii a raportat că sensibilitatea EMA este> 90% și specificitatea este 98%, în timp ce sensibilitatea și specificitatea anti-tTG sunt ambele> 90%. 7 Atât EMA cât și anti-tTG sunt anticorpi IgA și, prin urmare, ambii pot prezenta fals negativitate în deficiența selectivă de IgA. Prevalența deficitului de IgA în populația europeană generală este de 0,24-0,61%. 8 9 În boala celiacă, prevalența deficitului de IgA este de 2%. 10 Deși serologia pozitivă susține un diagnostic de boală celiacă, absența acesteia nu o exclude. Boala celiacă seronegativă se caracterizează prin caracteristici clinice și histologie de susținere și serologie negativă.
Intestinul subțire este adesea biopsiat atunci când investigăm simptomele gastrointestinale și pierderea în greutate. Caracteristicile patologice observate în boala celiacă, atunci când sunt expuse la gluten, includ atrofia viloasă, creșterea limfocitelor T intraepiteliale, scăderea înălțimii enterocitelor și hiperplazia criptelor. Deși aceste modificări susțin diagnosticul bolii celiace, ele nu sunt patognomonice pentru aceasta, ci sunt în schimb caracteristici nespecifice. Ghidurile actuale recomandă administrarea de biopsii duodenale multiple (una sau două din bulb și cel puțin patru din duodenul distal) pentru a diagnostica sau exclude boala celiacă. 11 Includerea biopsiilor din bulb crește detectarea anomaliilor histologice, deoarece mai mult de 8% dintre pacienții cu boală celiacă au doar anomalii histologice în bulb, care altfel ar fi ratate. 12-14 Probele histologice pot fi descrise folosind schema de clasificare Marsh. 15 Severitatea implicării histologice se poate corela cu nivelurile serice ale anticorpilor bolii celiace. În prezența atrofiei parțiale, spre deosebire de totală, a vilozității, sensibilitatea EMA serică este redusă. 16 17
Într-un studiu, 95% dintre pacienții cu atrofie viloză duodenală au fost diagnosticați cu boală celiacă, ceea ce înseamnă că 5% au avut un diagnostic alternativ. 1 Astfel, pentru a diagnostica cu încredere boala celiacă, descoperirile histologice trebuie luate în considerare împreună cu alte caracteristici de susținere, cum ar fi simptomele și testarea anticorpilor. După începerea unei diete fără gluten, îmbunătățirea histologică poate dura câteva luni și rezoluția completă poate dura câțiva ani. 18
În acest caz, pacientul a avut simptome și histologie de susținere, dar EMA negative și anti-tTG, cu o concentrație normală de IgA serică. Astfel, se credea că are boală celiacă seronegativă. Cu toate acestea, când nu a reușit să se îmbunătățească în ciuda aderării la o dietă fără gluten, diagnosticele alternative, inclusiv boala celiacă seronegativă refractară, limfomul cu celule T intestinale de tip enteropatie și SIBO au fost luate în considerare de către al doilea gastroenterolog.
Boala celiacă are o predispoziție genetică subiacentă. Este legat de anumite complexe majore de histocompatibilitate de clasa II, și anume HLA-DQ2 și HLA-DQ8. Acestea nu sunt diagnostice, deoarece nu sunt limitate la boala celiacă. Au o valoare predictivă pozitivă scăzută, dar o valoare predictivă negativă ridicată (98-100%). 19 20 Aceasta înseamnă că nu sunt potrivite pentru screening, dar sunt utile pentru a exclude boala celiacă. Într-un studiu european, doar 6% dintre pacienții cu boală celiacă nu aveau nici heterodimerul HLA-DQ2, nici HLA-DQ8. 21 Cu toate acestea, aproape toți acești pacienți negativi cu HLA-DQ2 și HLA-DQ8 cu boală celiacă au purtat una dintre alelele haplotipului HLA-DQ2. Astfel, în cazul nostru, absența oricărui complex HLA a făcut ca boala celiacă să fie puțin probabilă.
Deoarece boala celiacă a fost un diagnostic unificator puțin probabil, au fost luate în considerare alternative viabile. Cu toate acestea, în timp ce făcea acest lucru, pacientul a continuat o dietă fără gluten din cauza gravității stării sale de prezentare. O serie de 30 de pacienți, cu atrofie viloasă, dar la care boala celiacă fusese exclusă, au raportat 10 etiologii diferite, deși există mai multe. 22 Acestea au inclus duodenită peptică (n = 3), duodenită peptică cu infecție Helicobacter pylori (n = 2), colagenous sprue (n = 3), gastroenterită eozinofilă (n = 2), gastroenterită acută virală (n = 2), SIBO n = 3), boala Crohn (n = 2), sprue tropical (n = 1), alergie alimentară (n = 1), sindrom de imunodeficiență variabilă comună (n = 1) și enteropatie mediată imun nedefinită (n = 10). Alte cauze raportate de atrofie viloasă, cu sau fără limfocitoză intraepitelială crescută, includ boala grefă contra gazdă, ischemia cronică intestinală, chimioradierea, anumite medicamente și deficiențe nutriționale. 23 24
Într-un studiu, SIBO a afectat 11% dintre pacienții cu boală celiacă dovedită cu biopsie, care nu răspund. 25 Colonizarea proximală a intestinului subțire de către bacteriile colonice provoacă malabsorbție prin degradarea alterată a sării biliare. SIBO devine mai frecvent odată cu înaintarea în vârstă și este adesea predispus la o anomalie subiacentă care afectează intestinul subțire sau mecanisme defensive. Într-un studiu, un factor de risc a fost găsit în 66% din cazuri. 26 Anomaliile intestinului subțire includ cele care afectează structura intestinului subțire (de exemplu, buclele orbului chirurgical, aderențe, fistule și rezecții ileocaecale) sau motilitatea (de exemplu, diabetul zaharat și scleroza sistemică). 26 Alți factori predispozanți includ utilizarea prelungită a medicamentelor care scad acidul, cum ar fi inhibitorii pompei de protoni și insuficiența renală cronică. 26 27 Niciuna dintre aceste condiții predispozante nu a fost prezentă în cazul prezentat. În special, înainte de apariția simptomelor, pacienta nu lua medicamente obișnuite, iar singurul său istoric medical a fost de boală diverticulară. Testul standardului de aur este cultura aspiratului jejunal. Cu toate acestea, la fel ca în cazul nostru, pacienții sunt de obicei diagnosticați prin testul de respirație radiomarcat mai convenabil, care măsoară produsele de fermentare bacteriană expirate.
SIBO poate provoca modificări microscopice ale mucoasei duodenale, ca în acest caz. Cu toate acestea, modificările histologice nu sunt prezente la majoritatea pacienților cu SIBO. Un studiu, care a implicat cazuri dovedite de aspirat de SIBO, a constatat apariția vilor în 24% și a crescut limfocitoza intraepitelială în 26%. 26 Cu toate acestea, 52% dintre pacienții studiați nu au avut nicio anomalie histologică. Modificările patologice se rezolvă după eradicarea bacteriilor luminale. 28 Astfel, în cazul nostru, ameliorarea mucoasei ar putea fi rezultatul eradicării bacteriene. Acest lucru a fost susținut de testul normal de respirație ulterior. Dieta parțială fără gluten a pacientului era puțin probabil să fie cauza îmbunătățirii, deoarece, chiar și atunci când ea fusese pe deplin conformă, aceasta nu reușise să-și rezolve anomaliile histologice duodenale, darămite simptomele ei.
Alte rezultate potențial confuze în acest caz includ elastaza fecală scăzută, care a fost corectată ulterior și calprotectina crescută. Elastaza fecală are o sensibilitate scăzută pentru insuficiența pancreatică ușoară. 29 Elastaza fecală este scăzută în stări diareice nespecifice, inclusiv boala celiacă netratată și infecțiile acute, probabil din cauza deteriorării mucoasei, deoarece se corectează la vindecarea mucoasei. 30 31 Acest lucru poate explica elastaza fecală scăzută în cazul nostru.
Calprotectina fecală este un marker al inflamației intestinale subclinice. Bolile intestinale accidentale, inclusiv SIBO și celiacul, s-au dovedit a fi asociate cu calprotectina fecală crescută. 32 Cu toate acestea, studiile comparative nu au demonstrat o diferență între participanții cu și fără SIBO sau boală celiacă. 33–35
Pe scurt, acest caz evidențiază necesitatea de a investiga pe deplin pacienții care nu răspund așa cum era anticipat. Nerespectarea acestui lucru poate duce la simptome continue și la scăderea nutrițională.
Puncte de învățare
Blunting vilos duodenal și limfocitoză intraepitelială sunt descoperiri nespecifice și diagnosticul diferențial include boala celiacă.
Dacă un pacient despre care se crede că are boală celiacă nu reușește să se amelioreze, respectarea unei diete fără gluten ar trebui verificată de un specialist dietetician.
Dacă un pacient despre care se crede că are boală celiacă nu reușește să se îmbunătățească așa cum s-a prevăzut atunci când aderă la o dietă fără gluten, ar trebui luate în considerare diagnostice alternative, inclusiv creșterea excesivă a bacteriilor.
În cazurile de boală celiacă suspectată cu histologie discordantă - constatări serologice, trebuie efectuată determinarea antigenului leucocitelor umane.
Note de subsol
Colaboratori: EH a scris articolul. SH, LH și SL au examinat și editat articolul.
Interese concurente: Nici unul.
Consimțământul pacientului: Obținut.
Proveniență și evaluare inter pares: Nu este comandat; extern evaluat de colegi.
- Raport de caz Vărsături severe recurente din cauza hipertiroidismului
- Always Dailies Slim Panty Liners 26 (Caz de 8)
- 10 beneficii ale consumului de lapte de ciocolată pentru recuperarea nutriției - Fundația Gold Crown
- Un studiu de caz MOGXP privind nutriția optimă a publicului nou
- California Gold Nutrition Lăptișor de matcă concentrat; Liofilizat