Publicat: 26 februarie 2020 (vezi istoricul)
DOI: 10.7759/cureus.7110
Citați acest articol ca: Sugiyama S, Jinnouchi H, Hieshima K și colab. (26 februarie 2020) Remisiunea diabetului de tip 2 și reducerea substanțială a greutății corporale realizate cu metformină și un inhibitor de cotransportor 2 de glucoză de sodiu. Cureus 12 (2): e7110. doi: 10.7759/cureus.7110
Abstract
Scopul general în tratamentul diabetului zaharat de tip 2 (T2DM) este remisiunea. Cu toate acestea, efectele unui inhibitor al cotransportorului de sodiu-glucoză 2 (SGLT2i) asupra remisiei T2DM sunt necunoscute. Raportăm aici un caz care implică un bărbat în vârstă de 43 de ani, supraponderal, care și-a revenit complet din T2DM după terapia SGLT2i (dapagliflozin la 5 mg/zi). În perioada de pretratare, el a avut un indice de masă corporală (IMC) de 26,0 kg/m2, concentrație de hemoglobină A1c (HbA1c) de 10,3%, rezistență avansată la insulină, disfuncție pancreatică a celulelor β și ficat gras. La 18 luni de la terapia cuprinzătoare, inclusiv administrarea unui SGLT2i și a metforminei, IMC-ul său scăzuse la 21,3 kg/m2 și controlul glicemic a fost aproape normal (HbA1c de 5,3%), în ciuda întreruperii tuturor medicamentelor hipoglicemiante. Acest raport este primul care propune utilitatea terapiei combinate a SGLT2i și metforminei pentru realizarea greutății corporale normale și a remisiei T2DM nou diagnosticate într-o situație clinică reală.
Introducere
Diabetul zaharat de tip 2 (T2DM) este larg recunoscut ca o boală cronică progresivă care necesită tratament hipoglicemiant pe tot parcursul vieții [1]. Cu toate acestea, unii pacienți pot menține un control glicemic bun doar prin dietă și terapie de efort după ce au primit un diagnostic definitiv de T2DM [2]. T2DM are diverse cauze patogene și este asociat cu mai multe afecțiuni clinice, iar boala urmează cursuri clinice diverse în rândul pacienților afectați [3].
Debutul T2DM este puternic asociat cu creșterea în greutate corporală și excesul de acumulare de grăsime ectopică în ficat și pancreas [4-5]. În faza incipientă a T2DM, se recomandă modificarea stilului de viață prin dietă și terapie cu exerciții fizice pentru a atinge greutatea corporală și aportul caloric adecvat. Dacă nu se realizează un control glicemic adecvat, se ia în considerare adăugarea farmacoterapiei care scade glucoza [2]. Cu toate acestea, furnizarea de direcții și instrucțiuni specifice și personale pentru îmbunătățirea stilului de viață tinde să fie insuficientă în practica clinică zilnică. Aplicarea și continuarea unei diete stricte și a terapiei de efort sunt adesea dificile în situația de viață de zi cu zi alimentată de mulți pacienți cu T2DM [6].
Inhibitorii cotransportorului de sodiu-glucoză 2 (SGLT2is), care sunt medicamente eficiente pentru scăderea glucozei, reduc concentrația de glucoză din sânge prin creșterea excreției urinare de glucoză într-un mod independent de insulină. Acest lucru are ca rezultat metabolismul grăsimilor acumulate și o reducere a greutății corporale prin pierderea de calorii în urină [7]. Această pierdere în greutate indusă de SGLT2i ar putea fi benefică pentru o gamă largă de pacienți cu T2DM [8-9].
În prezenta descriem un pacient cu T2DM la care concentrația de hemoglobină A1c (HbA1c) a scăzut cu succes la aproape un nivel normal, cu o pierdere substanțială în greutate după terapia cuprinzătoare, inclusiv administrarea de metformină și SGLT2i (dapagliflozin la 5 mg/zi). Pacientul nostru a întrerupt complet toate medicamentele hipoglicemiante, ducând la remisia T2DM [10].
Prezentarea cazului
La începutul lunii aprilie 2018, un bărbat în vârstă de 43 de ani a prezentat Centrul de îngrijire a diabetului de la spitalul Jinnouchi din Kumamoto, Japonia, din cauza controlului inadecvat al T2DM. La 33 de ani, fusese diagnosticat cu obezitate (indice de masă corporală (IMC) de 28,7 kg/m2), sindrom de apnee în somn și hipertensiune. La acel moment, el a fost tratat cu presiune continuă pozitivă a căilor respiratorii, un blocant al receptorilor angiotensinei II, un antagonist al canalelor de calciu și un diuretic tiazidic de către medicul său de îngrijire primară. Cu două luni înainte de vizita sa inițială la spitalul nostru, a dezvoltat oboseală generală, scădere în greutate (de la 86 la 81 kg) și crampe la nivelul membrelor inferioare în timpul activității sale de vânzător. Nu avea obiceiul de a consuma excesiv de băuturi răcoritoare. Simptomele sale nu s-au ameliorat, iar o concentrație crescută de glucoză în ser de post de 252 mg/dl a fost detectată pentru prima dată la un control anual de sănătate în martie 2018. De asemenea, avea un istoric familial puternic de T2DM (bunica, tatăl și fratele). El a devenit serios îngrijorat de starea sa clinică și a decis să viziteze Centrul nostru de îngrijire a diabetului.
La prima sa vizită la serviciul nostru ambulatoriu, examenul clinic a arătat o înălțime corporală de 174 cm, greutatea corporală de 80,8 kg, IMC de 26,0 kg/m 2, tensiunea arterială de 118/65 mmHg și o frecvență regulată a pulsului de 94 bătăi/min. . Examenul fizic nu a evidențiat nicio anomalie. Examenul de laborator a arătat hiperglicemie (concentrația glicemiei în jeun, 157 mg/dL); concentrații crescute de HbA1c (10,3%), aspartat transaminază (38 UI/L) și alanină transaminază (46 UI/L); și o rată de filtrare glomerulară estimată redusă (68,1 mL/min/1,73 m 2). Mai mult, pacientul avea proteinurie (±), hematurie (+) și corpuri cetonice urinare pozitive (+) (Tabelul 1).
| Biochimie | Metabolismul glucozei | ||
| Proteine totale (g/dL) | 7.2 | Glicemia din jeun (mg/dL) | 157 |
| Albumină (g/dL) | 4.6 | Hemoglobina A1c (%) | 10.3 |
| Bilirubină totală (mg/dL) | 0,9 | ||
| AST (IU/L) | 38 | [Numărul de celule sanguine] | |
| ALT (IU/L) | 46 | Celule albe din sânge (/ ml) | 4670 |
| g-GTP (IU/L) | 30 | Celule roșii din sânge (/ ml) | 493 x 10 4 |
| LDH (UI/L) | 158 | Hemoglobina (g/dL) | 15.2 |
| ALP (IU/L) | 184 | Hematocrit (%) | 44,7 |
| CPC (IU/L) | 246 | MCV (fL) | 90,7 |
| Amilază (UI/L) | 52 | MCH (pag.) | 30,8 |
| Colesterol total (mg/dL) | 192 | MCHC (%) | 34,0 |
| HDL-colesterol (mg/dL) | 41 | Trombocite (/ ml) | 25,7 x 10 4 |
| Trigliceridă (mg/dl) | 78 | ||
| LDL-colesterol (mg/dL) | 135 | [Date urinare] | |
| BUN (mg/dL) | 11.2 | pH | 6.0 |
| Creatinină (mg/dL) | 0,89 | Gravitație specifică | 1.025 e cel mai frecvent |
| Acid uric (mg/dL) | 6.8 | Proteină | +/- |
| Sodiu (Na; mEq/L) | 137 | Glucoză | - |
| Potasiu (K; mEq/L) | 4.2 | Sange ocult | + |
| Clorură (Cl; mEq/L) | 98 | Cetonă | + |
| Calciu (Ca; mg/dL) | 9.3 | Urobilinogen | +/- |
Tabelul 1: Date de laborator la prima vizită la spitalul Jinnouchi
AST: aspartat aminotransferază, ALT: alanină aminotransferază, γGTP: γ glutamil transpeptidază, LDH: lactat dehidrogenază, ALP: fosfatază alcalină, CPK: creatinin fosfokinază, BUN: azot uree din sânge, HDL: lipoteină cu densitate mare, MCV: corpusc mediu MCH: hemoglobină corpusculară medie, MCHC: concentrație medie de hemoglobină corpusculară
Nu a avut retinopatie diabetică, neuropatie, disfuncție tiroidiană, anomalie suprarenală sau antecedente de boli cardiovasculare.
Tabelul 2: Evaluarea inițială a stării diabetice și a complicațiilor asociate diabetului
CPR: imunoreactivitate peptidă C, GAD: decarboxilază a acidului glutamic, valoare M: viteza de perfuzie a glucozei, M/I: (valoare M)/(insulină în stare de echilibru), eGFR: rata estimată de filtrare glomerulară, CT: tomografie computerizată, PAT: tonometrie arterială periferică (indicele funcției endoteliale microvasculare)
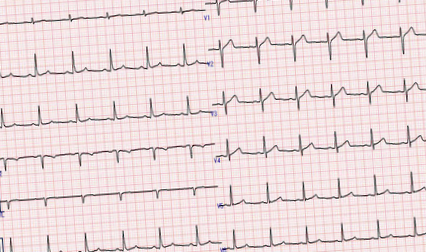
O electrocardiogramă (Figura 1) și o radiografie toracică (Figura 2) nu au evidențiat anomalii.
Figura 1: Electrocardiogramă
Figura 2: Radiografie toracică
O examinare cu ultrasunete abdominală a evidențiat ficat gras (Figura 3A-3B), calcificare renală dreaptă (Figura 3B, o săgeată albă), un polip al vezicii biliare (Figura 3C, săgeți galbene) și nicio anomalie în pancreas (Figura 3D).
Figura 3: Imagini cu ultrasunete abdominale înainte de terapie
A: Imagini de ficat; B: Imagine a ficatului și a rinichiului drept, săgeata albă indică calcificarea rinichilor; C: imaginea vezicii biliare, săgețile galbene indicau un polip al vezicii biliare; D: imagini de pancreas
Tomografia computerizată abdominală a arătat depunerea excesivă de grăsime subcutanată (Figura 4, săgeți albe) și creșterea acumulării de grăsime hepatică (Figura 4, săgeți galbene), evaluată prin raportul de atenuare a ficatului la splină (Tabelul 3) [12].
Figura 4: Modificări ale acumulării de grăsime abdominală și hepatică după remisiunea diabetului
Imagini de scanare a grăsimilor și imagini de tomografie computerizată abdominală înainte de terapie și după remisiunea diabetului. Zonele albastre au indicat grăsimea subcutanată și zonele roșii au indicat grăsimea viscerală evaluată prin scanare a grăsimii; VFA: zona de grăsime viscerală (cm 2), SFA: zona de grăsime subcutanată (cm 2). Săgețile albe indică acumularea de grăsime subcutanată abdominală, iar săgețile galbene indică ficatul gras.
A: Imagine de scanare a grăsimilor înainte de terapie; B: Imagine de scanare a grăsimilor după remisie; C: Imagine a ficatului și a splinei înainte de terapie; D: Imagine a ficatului și splinei după remisie
| Pre-tratament | Post-tratament și remisie | |
| Hemoglobina A1c (%) | 10.3 | 5.3 |
| Glucoza plasmatică în post (mg/dL) | 157 | 93 |
| Insulina de post (mU/ml) | 8.7 | 2.5 |
| HOMA-IR | 3.37 | 0,57 |
| HOMA-b | 33.3 | 30.0 |
| QUICKI | 0,121 | 0,41 |
| Indicele insulinogen | 0,03 | 0,75 |
| Indicele Matsuda și DeFronzo | 3.25 | 10,84 |
| Indicele de dispunere | 0,03 | 8.18 |
| Valoarea M (mg/kg/minut) | 6.35 | - |
| Greutate corporală (kg) | 80,8 | 66,5 |
| Indicele de masă corporală (kg/m 2) | 26.0 | 21.3 |
| Circumstanța taliei (cm) | 90,8 | 80.0 |
| Masa de grăsime corporală (kg) | 22.2 | 8.8 |
| Procentul de grăsime corporală (%) | 27,8 | 13.3 |
| Masa musculară scheletică (kg) | 32,8 | 32.0 |
| Apa corporală totală (L) | 42,5 | 42,5 |
| Zona de grăsime viscerală abdominală (cm 2) | 81,90 | 15,96 |
| Suprafață grasă subcutanată abdominală (cm 2) | 233,49 | 113,97 |
| Suprafața totală de grăsime abdominală (cm 2) | 315.39 | 129,93 |
| Raport de atenuare a ficatului/splinei | 0,40 | 1.12 |
Tabelul 3: Modificări ale parametrilor metabolici și antropometrici ai glucozei
HOMA-IR: Evaluarea modelului de homeostazie pentru rezistența la insulină; HOMA-b: Evaluarea modelului homeostatic pentru funcția celulelor beta; QUICKI: Indicele cantitativ de verificare a sensibilității la insulină; Valoare M: Viteza de perfuzie a glucozei
Starea sa clinică a sugerat posibilitatea unor factori ereditari pentru T2DM, disfuncție pancreatică a celulelor β, ficat gras și rezistență la insulină cu exces de greutate corporală și acumulare de grăsime ectopică.
Datorită rezistenței la insulină existente și a capacității păstrate de secreție de insulină intrinsecă, pacientul a primit terapie de modificare a stilului de viață în timpul spitalizării. I s-au dat informații tipărite cu privire la utilizarea dietei și a exercițiilor fizice pentru tratarea T2DM. El a primit, de asemenea, o explicație a stării sale actuale de supraponderalitate și a greutății corporale țintă din Figura 5: evoluția în timp a modificărilor greutății corporale și a HbA1c în timpul îngrijirii ambulatorii post-externare
IMC: indicele de masă corporală; BW: greutatea corporală; HbA1c: hemoglobina A1c; SGLT2: cotransportor de sodiu-glucoză-2
Săgeata neagră indică atingerea unei greutăți corporale de 70 kg, săgețile gri indică un control bun susținut al diabetului, linia punctată albastră indică nivelul greutății corporale ideale, iar linia punctată verde indică punctul de timp (noiembrie 2018) al normalizării atât a HbA1c, cât și a corpului greutate
În decembrie 2018, am început să tratăm pacientul cu administrarea alternativă a SGLT2i pe zi, iar în februarie 2019, am adăugat o jumătate de doză de metformină (500 mg/zi) deoarece HbA1c a crescut de la 5,2 la 5,3%. În aprilie 2019, am oprit SGLT2i și am tratat pacientul doar cu doză mică de metformină. În cele din urmă, în iunie 2019, am întrerupt toate medicamentele care scad glucoza și am reexaminat pacientul la ambulatoriu la fiecare două luni. Controlul glicemiei și greutatea corporală au fost bine gestionate și au rămas în limitele normale (Figura 5, săgețile gri). Tabelele 3 și Figura 6 prezintă modificările parametrilor metabolici și antropometrici ai glucozei pacientului înainte de tratament și după remisia T2DM timp de șase luni.
Figura 6: Modificări ale concentrațiilor de glucoză și insulină în testul oral de toleranță la glucoză de 75 g înainte și după remisiunea diabetului
A: Concentrațiile de glucoză înainte de terapie; B: Concentrațiile de glucoză după remisie; C: Concentrațiile de insulină înainte de terapie; D: Concentrațiile de insulină după remisie
Parametrii săi metabolici ai glucozei s-au normalizat, iar faza incipientă a secreției de insulină s-a recuperat cu succes după o încărcătură orală de glucoză (Figura 6). Interesant este faptul că tomografia computerizată abdominală după remisia T2DM a arătat că volumul pancreasului a crescut de la 52,5 cm 3 la 61,4 cm 3. Analiza impedanței bioelectrice utilizând un analizor de compoziție corporală (InBody 770; InBody SUA, Cerritos, CA) nu a indicat aproape nicio modificare a masei sale musculare scheletice și a cantității de apă din corp în timpul terapiei [13]. Cu toate acestea, masa sa de grăsime corporală scăzuse dramatic. Mai mult, zonele sale de grăsime abdominală viscerală și subcutanată scăzuseră semnificativ și acumularea sa de grăsime ectopică în ficat se normalizase (Figura 4B-4D) [12]. Nu au apărut evenimente adverse grave în timpul tratamentului.
Discuţie
Scopul general în tratamentul clinic al T2DM este remisiunea [10,14]. Am experimentat un caz care implică un japonez în vârstă de 43 de ani, care a obținut cu succes o reducere cu aproximativ 20% a greutății corporale. De asemenea, a obținut remisiunea completă a T2DM-ului recent diagnosticat după o terapie cuprinzătoare, inclusiv administrarea unui SGLT2i.
În faza incipientă a T2DM, oferim inițial pacienților instrucțiuni cu privire la modificarea stilului de viață prin dietă și terapie de efort pentru a ajunge la o greutate corporală adecvată și a corecta aportul excesiv de calorii [2]. Apoi adăugăm farmacoterapie care scade glicemia dacă nu s-a realizat un control glicemic adecvat [2]. Recunoaștem că continuarea cu succes a terapiei dietetice și a exercițiilor fizice este importantă pentru a obține remisiunea T2DM. Unii pacienți cu T2DM pot menține un control glicemic bun doar prin dietă și terapie de efort, iar unii pacienți întrerup complet toate medicamentele hipoglicemiante, rezultând remisiunea T2DM [3,10]. În practica clinică zilnică reală, furnizarea de direcții și instrucțiuni specifice și personale pentru îmbunătățirea stilului de viață tinde să fie insuficientă, deoarece membrii personalului clinic nu au timp pentru îngrijirea adecvată a pacienților. În plus, asigurarea medicală nu acoperă terapia exercițiilor fizice pentru T2DM în Japonia. Remisia T2DM poate regresa cu ușurință la T2DM evident, necesitând medicamente hipoglicemiante.
În contextul clinic, terapia SGLT2i poate duce la pierderea în greutate corporală (în principal prin reducerea grăsimilor fără un control alimentar intensiv, cum ar fi o dietă cu conținut scăzut de calorii) la scurt timp după începerea administrării medicamentului [7,13]. Terapia SGLT2i poate servi astfel ca o strategie eficientă și mai puțin stresantă de reducere a greutății la pacienții supraponderali sau obezi cu T2DM. Posibilitatea de a obține o greutate corporală dorită prin terapia de reducere a greutății poate ajuta la menținerea motivației pacientului, ducând la o reducere durabilă a greutății în epoca actuală a terapiei SGLT2i. Scăderea și normalizarea greutății induse de SGLT2i ar putea promova în mod spontan schimbarea comportamentului unui pacient pentru a menține cu succes dieta zilnică și terapia cu efort. Noi, clinicienii, ar trebui să ținem cont de importanța unei astfel de strategii de tratament cuprinzătoare, inclusiv SGLT2i.
În populația japoneză, riscul de a dezvolta T2DM și rezistența la insulină crește la un IMC ≥ 23 kg/m 2 [19]. Prin urmare, o scădere a grăsimii corporale indusă de terapia de reducere a greutății ar putea ajuta la îmbunătățirea rezistenței la insulină la pacienții japonezi cu T2DM ușor sau moderat supraponderali. Rezistența la insulină este o afecțiune patogenă fundamentală a T2DM nu numai la pacienții cu obezitate severă care sunt candidați clinici la chirurgie bariatrică, ci și la pacienții supraponderali cu T2MD din Japonia [5,20]. Terapia cuprinzătoare antidiabetică și de reducere a greutății, inclusiv administrarea SGLT2i, ar putea elimina grăsimile excesiv acumulate [7,9]. Acest lucru ar putea duce la o îmbunătățire a rezistenței la insulină, a ficatului gras și a metabolismului glucozei [12]. Constatările din acest caz sugerează că se poate dezvolta o strategie integrată anti-diabetică și de reducere a greutății cu o dietă adecvată și o terapie de efort, inclusiv administrarea unui SGLT2i, la pacienții supraponderali, în stadiul incipient al T2DM. În viitor, va fi interesant să se ia în considerare contribuția terapiei de modificare a stilului de viață și a SGLT2i la îmbunătățirea și remisiunea T2DM.
Concluzii
Scopul general în tratamentul T2DM este remisiunea. Raportăm aici un caz care implică un bărbat în vârstă de 43 de ani, supraponderal, care și-a revenit complet din T2DM după o terapie cuprinzătoare, inclusiv administrarea unui SGLT2i și a metforminei. Recomandăm clinicienilor să încerce o strategie de reducere a greutății pentru a obține remisiunea T2DM la pacienții supraponderali. Propunem utilitatea unui SGLT2i pentru obținerea unei greutăți corporale normale și a remisiei T2DM nou diagnosticate într-o situație clinică reală.
- Ar putea această intervenție chirurgicală de scădere în greutate un remediu pentru diabetici de tip 2 asociați laparoscopici avansați
- Guma de guar pentru meta-analiza de reducere a greutății corporale a studiilor randomizate - ScienceDirect
- EFECTELE GUMULUI DE GUAR ASUPRA REDUCERII GREUTĂȚII, SCULPTURILOR ȘI DIABETULUI ÎN GLOBESITY BOOTCAMP PENTRU OBESE
- Modificări ale IMC și ale greutății înainte și după dezvoltarea diabetului de tip 2 Îngrijirea diabetului
- CoolSculpting Sculptarea corpului, conturarea corpului, reducerea neinvazivă a grăsimilor