Instrumente
Urmăriți jurnalul
Secția de imunologie, Instituția pentru științe medicale experimentale, Universitatea Lund, Lund, Suedia
Secția de imunologie, Instituția pentru științe medicale experimentale, Universitatea Lund, Lund, Suedia
Departamentul de Oncologie Pediatrică/Hematologie, Spitalul Universitar Skåne, Lund, Suedia
Secția de imunologie, Instituția pentru științe medicale experimentale, Universitatea Lund, Lund, Suedia
Corespondență: David Bryder, Ph.D., Secția de imunologie, Institution for Experimental Medical Science, Universitatea Lund, BMC D14, Klinikgatan 32, 221 84 Lund, Suedia. Căutați mai multe lucrări ale acestui autor
Secția de imunologie, Instituția pentru științe medicale experimentale, Universitatea Lund, Lund, Suedia
Secția de imunologie, Instituția pentru științe medicale experimentale, Universitatea Lund, Lund, Suedia
Departamentul de Oncologie Pediatrică/Hematologie, Spitalul Universitar Skåne, Lund, Suedia
Secția de imunologie, Instituția pentru științe medicale experimentale, Universitatea Lund, Lund, Suedia
Corespondență: David Bryder, Ph.D., Secția de imunologie, Institution for Experimental Medical Science, Lund University, BMC D14, Klinikgatan 32, 221 84 Lund, Suedia. Căutați mai multe lucrări ale acestui autor
Abstract
Introducere
Procesul fiziologic al îmbătrânirii este însoțit de o pierdere generală a condiției fizice și o prevalență crescută dramatic a multora dintre cele mai devastatoare boli ale noastre, inclusiv demență, autoimunitate și cancer. Deoarece durata de viață a populației umane se extinde continuu, este foarte necesară o înțelegere sporită a mecanismelor care stau la baza procesului de îmbătrânire. Acest lucru este important nu numai pentru a înțelege dezvoltarea bolii în contextul vârstei, ci și pentru obiectivul pe termen lung de a atinge în cele din urmă o stare generală mai sănătoasă în etapele ulterioare ale vieții [1], obiectiv care poate fi anticipat a fi atins. prin inversarea sau cel puțin inhibarea decăderii determinate de vârstă a performanței organismului.
Deși au fost propuse mai multe încercări de formulare a unor teorii mai universale asupra cauzelor îmbătrânirii, îmbătrânirea organismelor multicelulare este, fără îndoială, un proces multiparameter progresiv [2] care se caracterizează prin fenotipuri asincrone/segmentare ale diferitelor organe [3]. În ciuda acestui fapt, un consens în creștere susține o asociere a creșterii vârstei și a eșecului de a menține în mod adecvat homeostazia organelor și a țesuturilor sau de a reveni la condițiile homeostatice după stres sau leziuni [4]. Celulele stem rezidente de țesuturi, care până acum au fost identificate în majoritatea organelor și țesuturilor adulte [5], s-au sugerat că sunt legate cauzal de procesul de îmbătrânire [4]. Din punctul de vedere că funcția principală a celulelor stem este menținerea homeostaziei țesuturilor prin completarea celulelor pierdute prin diferite insulte, o contribuție a celulelor stem la procesul de îmbătrânire pare intuitivă [5]. Acest lucru, nu în ultimul rând, deoarece evenimentele mutaționale asociate vârstei sau alte forme de leziuni macromoleculare câștigate la nivelul celulelor stem somatice prezintă riscul propagării către descendenții săi diferențiați. În cele din urmă, acest lucru poate fi imaginat pentru a compromite fie generarea, fie funcția produselor finale diferențiate.
Manifestarea îmbătrânirii HSC și relevanța sa pentru sistemul imunitar de îmbătrânire
Un organ care depinde în mod critic de funcția celulelor stem adulte este sistemul sanguin sau hematopoietic [5]. În acest sistem, toate celulele sanguine provin din celule stem hematopoietice (HSC) care rezidă în măduva osoasă rare (BM), care se auto-reînnoiesc și sunt capabile să inițieze o cascadă de diferențiere treptată și ierarhică. Aceasta implică generarea diferitelor tipuri de celule progenitoare intermediare cu potențial de diferențiere îngustat progresiv, în care rezultatul final este generarea de celule sanguine efectoare mature aparținând uneia din mai multe linii distincte [5].
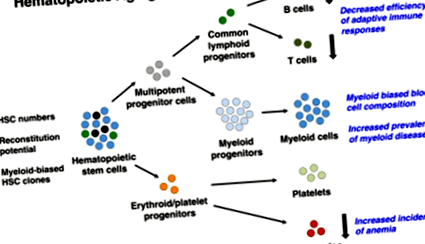
Luând în considerare nu numai că prevalența diferitelor boli hematologice crește dramatic odată cu vârsta [35], ci și că acestea apar în mod predominant din descendențele mieloide [9], este tentant să speculăm că o înclinare mieloidă asociată vârstei ar putea sta la baza mai multor fenotipuri relevante clinic, cum ar fi competența imunitară adaptivă redusă și creșterea prevalenței mai multor boli mielogene (Fig. 1). Sprijinirea directă a acestei interpretări este constatările pe care BCR/ABL fuziunea oncogenă, care este adesea cauzală atât pentru leucemia limfoidă cronică, cât și pentru leucemia mieloidă, a fost capabilă să dea naștere leucemiei mieloide numai atunci când a fost evaluată într-un context de îmbătrânire [9]. Pe aceeași linie, MLL‐Leucemia rearanjată asociată cu sugarii s-a arătat că implică progenitori limfoizi cu diferite tipuri de imunoglobulină/receptor de celule T - modele de rearanjare în comparație cu cele care apar mai târziu în viață [36] și, de fapt, în ambele MLL‐Rearanjat și BCR-ABL‐Leucemie pozitivă, vârsta este un factor de prognostic important pentru supraviețuire [37].
Modificări asociate vârstei în sistemul hematopoietic. O serie de neajunsuri imunologice apar ca o consecință a înaintării în vârstă și se crede că depind de modificările intrinseci celulare care apar la HSC în vârstă pentru întreținerea și propagarea lor. Acestea, la rândul lor, modifică compoziția ierarhiei hematopoietice și producția globală de celule sanguine. HSC cresc, de asemenea, în număr, ceea ce reflectă posibil un răspuns compensatoriu cauzat de capacitatea globală redusă de formare a sângelui. Pe măsură ce grupul HSC devine dominat de clone HSC cu potențial de diferențiere mieloidă (reprezentat ca HSC albastru deschis), abundența HSC echilibrate (descrise ca HSC negre) și HSC cu tendințe limfoide (descrise ca HSC verzi) scad odată cu vârsta. Acest lucru are ca rezultat o compoziție de celule sanguine înclinate, în care celulele mieloide periferice devin mai dominante, în timp ce atât progenitorii limfoizi, cât și limfocitele naive B și T scad din abundență. Abreviere: HSC, celulă stem hematopoietică.
Modelele au propus să explice capacitatea redusă de formare a sângelui din grupul HSC în vârstă. (A): Modelul de schimbare a populației sugerează că toate HSC sunt omogene la începutul vieții (cercuri gri deschis) și că majoritatea clonelor HSC treptat (cercuri gri închise) devin funcțional modificate odată cu înaintarea în vârstă. Acest lucru duce în cele din urmă la manifestarea unei stări de îmbătrânire în care majoritatea, dacă nu toate, clonele HSC sunt grav compromise funcțional (cercuri gri închise). (B): Modelul de selecție clonală propune în schimb că grupul HSC este eterogen și că creșterea vârstei are ca rezultat o extindere progresivă a clonelor selective HSC (descrise ca o expansiune a cercurilor negre). Odată cu vârsta înaintată, aceste clone HSC ajung să domine grupul HSC și rămân câteva clone HSC „tinere”, cum ar fi. (C): În modelul compozit, îmbătrânirea are ca rezultat extinderea selectivă a anumitor clone HSC (cercuri negre), care este însoțită de alte clone HSC care devin compromise funcțional odată cu creșterea vârstei (cercuri gri închise). La îmbătrânirea avansată, grupul HSC constă dintr-o proporție ridicată de HSC cu tendință mieloidă și un potențial global de formare a sângelui drastic redus pentru majoritatea clonelor HSC. Abreviere: HSC, celulă stem hematopoietică.
Declanșatorii îmbătrânirii
Dintr-o perspectivă evolutivă, îmbătrânirea ar putea fi în general considerată a fi rezultatul presiunilor selective. Dacă da, îmbătrânirea ar trebui să aibă una sau mai multe componente genetice subiacente care să păstreze resursele necesare pentru populația mai mare, prin îndepărtarea indivizilor care au trecut de prima lor reproducere [42]. Cu toate acestea, s-a sugerat că îmbătrânirea ar rezulta și din acumularea de mutații ADN [43] și gene pleiotropice: gene care sunt avantajoase la începutul vieții, dar dezavantajoase odată cu creșterea vârstei [44]. Deși devine din ce în ce mai clar că factorii de mediu au impact asupra capacității organismului, durata de viață foarte diferită a multor specii din natură susține noțiunea că îmbătrânirea poate fi guvernată intrinsec [45]. Trebuie menționat, totuși, că majoritatea animalelor din natură cedează la moarte prematură, de exemplu din cauza bolii sau a prădării și, în general, nu prezintă caracteristici asociată îmbătrânirii asemănătoare omului [46]. În acest sens, îmbătrânirea umană, inclusiv răspunsurile imune diminuate odată cu înaintarea în vârstă, poate fi văzută ca o „problemă” evolutivă tânără, care este rezultatul unei speranțe de viață prelungite cauzată de o calitate generală a vieții crescută și de o stare de sănătate îmbunătățită.
Cele mai multe investigații privind îmbătrânirea HSC au fost studiate folosind modele de șoarece, mai precis tulpina de șoarece C57Bl/6. Bineînțeles, aceasta este o preocupare pentru aplicabilitatea generală a descoperirilor făcute și traducerea lor la oameni. Încurajator, totuși, a devenit din ce în ce mai clar că mai multe fenotipuri de îmbătrânire sunt conservate nu numai între tulpini de șoareci alternative [7 - 9], ci și mai important cu îmbătrânirea hematopoietică umană (Fig. 1) [10]. De exemplu, oamenilor vârstnici li s-a propus recent să se asocieze cu o frecvență crescută a HSC-urilor care adăpostește un potențial de diferențiere cu tendințe mieloide [10]. Alte similitudini cu sistemul șoarecilor includ scăderi distincte ale celor mai primitivi progenitori limfoizi angajați și apariția frecventă a anemiei ușoare [11]. Astfel, mai multe aspecte cheie ale îmbătrânirii hematopoietice par a fi evolutive și conservate intrinsec și, cel mai important, pot fi studiate folosind organisme model cu durate de viață mai scurte - o problemă critică pentru a stabili experimental cauzalitatea.
Modificări intracelulare care însoțesc îmbătrânirea HSC
Deteriorarea ADN-ului
Mediatori moleculari ai îmbătrânirii celulelor stem hematopoietice (HSC) și consecințele lor asupra inversării. (A): Datorită longevității lor extinse, HSC-urile s-au propus a fi deosebit de predispuse la dobândirea daunelor ADN asociate vârstei sub formă de deleții, mutații și/sau eroziune telomerică. Dacă deteriorarea ADN-ului ar fi fost factorul principal al îmbătrânirii HSC, strategiile de inversare ar fi complicate de natura ireversibilă a modificărilor. (B): HSC în vârstă adăpostesc modificări epigenomice sub formă de distribuții modificate ale metilării ADN și modificări ale histonelor, care stau la baza transcriptomului modificat al HSC în vârstă. Inversarea acestor modificări ar trebui să dețină potențialul de întinerire funcțională a funcției HSC în vârstă.
Semnături transcripționale și epigenetice ale îmbătrânirii HSC
Progresele în izolarea celulelor au permis izolarea populațiilor de celule hematopoietice imature distincte la puritate ridicată. Profitând de acest lucru, mai mulți studii au realizat în ultimii ani o profilare extinsă a genelor direct pe HSC tineri și vârstnici [8, 13, 15, 23, 25, 61, 70, 71]. În mod colectiv, aceste lucrări au dezvăluit că modelele de expresie genică ale HSC-urilor tinere se modifică în mod distinct odată cu vârsta. Interesant este faptul că mai multe gene care devin reglate cu vârsta sunt importante pentru diferențierea celulelor mieloide, în timp ce multe gene reglate în jos se asociază cu limfopoieza [8]. Aceste descoperiri oferă sprijin molecular pentru distorsiunea mieloidă asociată vârstei a sistemului sanguin și sugerează că cel puțin unele dintre fenotipurile care apar în timpul îmbătrânirii HSC au baze transcripționale.
Colectiv, datele actuale susțin astfel că îmbătrânirea HSC se asociază puternic cu o „derivă” transcripțională și epigenetică (Fig. 3B), pe lângă rolul potențial al dobândirii ADN-ului cu vârsta. Cu toate acestea, deși contribuția epigeneticii la procesul de îmbătrânire începe să fie bine stabilită, trebuie să recunoaștem întrebarea restantă dacă aceste schimbări sunt factorii determinanți sau mai degrabă consecințele progresului în vârstă.
Este starea de îmbătrânire HSC reversibilă?
Deși în multe cazuri indirecte, descoperirile descrise susțin în comun că mediul de îmbătrânire și potențialii factori produși în cadrul acestuia pot avea, de asemenea, un impact asupra manifestării stării de îmbătrânire a HSC. Cu toate acestea, pe măsură ce transplantul de HSC în vârstă într-un mediu tânăr reconstituie un sistem hematopoietic în vârstă, modificările intrinseci ale celulelor în HSC în vârstă trebuie să fie suficiente, cel puțin pentru menținerea stării de îmbătrânire HSC fiziologică.
Perspective de viitor, terapie și provocări
Concluzie
- Diversitatea microbiană intestinală înainte de transplantul de celule stem poate avea un impact asupra supraviețuirii
- Oboseala cronică este foarte răspândită la supraviețuitorii transplantului de celule stem autolog și
- EDiets Review 2020 - Rip-Off sau merită încercat Iată de ce
- Editor’s Pick Impactul psihosocial al alergiei alimentare la adolescenți O recenzie a literaturii -
- Daily Harvest Recenzie boluri pentru micul dejun Au gust bun În valoare de 7 dolari fiecare Business Insider