Graziani A, Cappa FM, Fiorini E, Casalini P, Albertini F (2019) Sepsis pneumococic ca cauză a infarctului splenic masiv la pacientul cu boală celiacă necunoscută. Int J Crit Care Emerg Med 5: 079. doi.org/10.23937/2474-3674/1510079
RAPORT DE CAZ DOI ACCES DESCHIS: 10.23937/2474-3674/1510079
Alessandro Graziani 1 *, Federica Mirici Cappa 2, Erica Fiorini 2, Pierpaolo Casalini 3 și Francesco Albertini 4
1 Departamentul de Medicină Internă, Spitalul Ravenna, Italia
2 Departamentul de Medicină Internă, Spitalul Faenza, Italia
3 Departamentul de Medicină Terapie Intensivă, Spitalul Faenza, Italia
4 Secția de infectare, Spitalul Ravenna, Italia
Infarctul splenic (SI) este un eveniment rar care apare atunci când artera splenică (SA) sau ramurile sale devin ocluse de embol sau de tromboză in situ [1]. Majoritatea evenimentelor SI sunt rezultatul unor surse embolice, fie cardiace, fie aortice. Cu toate acestea, tulburările hematologice maligne și bolile autoimune sunt cauzele predominante ale trombozei splenice [2]. Infarctul splenic masiv (MSI) rezultă din fluxul sanguin compromis la mai mult de jumătate din splină [3]. În această lucrare descriem un caz al unui pacient anterior sănătos care a prezentat sepsis pneumococic care, la investigație, a dezvăluit o boală celiacă necunoscută și un MSI.
O femeie în vârstă de 57 de ani a intrat în secția de urgență (ED) cu 48 de ore de durere la nivelul piciorului drept agravată, letargie și febră. Istoricul ei medical trecut a inclus un prolaps al valvei mitrale (MVP). În DE a fost febrilă, letargică, elevii au fost egali și reactivi, fără anomalii la examenul neurologic. Semnele ei vitale au fost după cum urmează: tensiunea arterială (TA) 60/40 mmHg, ritmul cardiac (HR) 103 bătăi/min, temperatura 38,6 ℃, frecvența respiratorie (RR) de 18/min și oximetria pulsului de 96% pe aerul din cameră . Examenul fizic a arătat sunete pulmonare clare până la auscultare, ritm cardiac tahicardic cu ritm regulat, fără murmur, abdomenul a fost distins și difuz, fără protecție sau revenire.
Evaluarea inițială de laborator a demonstrat: celule albe din sânge (globule albe) 37210 × 10 9/litru; hemoglobină (Hb) 11,5 g/dL; trombocite (PLT) 12 × 10 9/litru; creatinină, 1,53 mg/dL; bilirubină totală 1,3 mg/dL; bilirubină directă, 0,9 mg/dL; ALT 75 U/L; 1,39 INR; fibrinogen 232 mg/dl, tromboplastină parțială activată (aPTT) 37 sec (raport 1,39); Proteină C reactivă (CRP) 272 mg/L (normal 9/litru cu hematurie. Din acest motiv, pacientul a primit o transfuzie de concentrate de trombocite (PC) și plasmă proaspătă congelată (FFP).
Din ziua internării, ea a prezentat o erupție maculară eritematoasă inițial asemănătoare cu petechii, care apoi a evoluat la o erupție purpurică cu vezicule cutanate și a progresat rapid către purpura fulminană. Leziunile au fost extinse la membrele superioare și inferioare, nas, obraji și regiunea abdominală. Hemoculturile au fost pozitive pentru pneumonia cu streptococ și antibiograma a relevat că această bacterie era sensibilă la terapia pe care pacientul o primea cu amoxicilină/clavulanat. După douăsprezece zile în terapie intensivă, a devenit stabilă clinic și a fost transferată la Departamentul de Medicină Internă. Aici a fost supusă unei ecografii abdominale, urmată de un ecou Doppler cu agent de contrast. Acest test a relevat o pierdere completă a perfuziei splenice care a sugerat un infarct masiv (Figura 1) confirmat și de CT abdominală cu material de contrast (Figura 2). A fost tratată cu enoxaparină subcutanată anticoagulantă în doza de 100 U/kg/zi. În zilele următoare, pacientul a fost febril și a necesitat o consultație cu boli chirurgicale și infecțioase. S-a decis apoi efectuarea unor investigații suplimentare și continuarea tratamentului cu antibiotice.
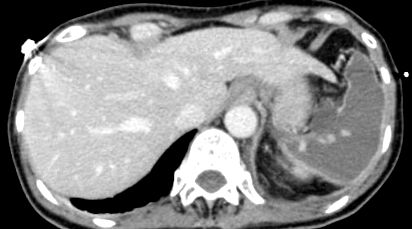
Figura 2: CT 2. Vizualizați figura 2
Ecocardiograma transtoracică (TTE) a demonstrat o vegetație pe valva mitrală, neprezentată de o fostă examinare ICU, confirmată de o ecocardiogramă trans-esofagiană (TEE). Un nou specimen de hemocultură a fost negativ pentru creșterea bacteriană, așa că am presupus că o propagare pneumococică anterioară în timpul fazei acute a sepsisului a cauzat colonizarea endocardică a valvei mitrale. Pacientul a suferit, de asemenea, tomografie cu emisie de pozitroni (PET) cu analogul glucozei 2- [18F] fluoro-2-deoxi-D-glucoză (18F-FDG) care nu a detectat nicio inflamație sau infecție. Am investigat posibilele cauze ale septicemiei pneumococice și am găsit în special un marker serologic pozitiv pentru anticorpii anti-gliadină și anti-endomiziali. Endoscopia GI superioară a arătat pierderea pliurilor Kerckring în duodenul descendent, iar histopatologia a relevat o atrofie viloasă completă. Pe baza constatărilor de mai sus, am suspectat o boală celiacă și pacientul a început să urmeze o dietă fără gluten și să primească vitamine. Tratamentul cu antibiotice a fost continuat timp de 15 zile după ultima hemocultură negativă.
În zilele următoare, examenele de laborator au arătat o reducere progresivă a parametrilor inflamatori ca WBC și RCP. Splina, evaluată periodic prin ultrasunete abdominale cu agent de contrast, a rămas neperfuzată și și-a redus progresiv volumul, așa cum a fost demonstrat și de un TC abdominal cu material de contrast (Figura 3a și Figura 3b). Pacientul a fost externat și i s-a recomandat vaccinarea pentru organismele capsulate. După patru luni de urmărire, ea a fost stabilă clinic. Nivelurile de proteină C, proteină S și antitrombină III, anticorpi anti-cardiolipină imunoglobulină (Ig) G și IgM, anticoagulant lupus, homocisteină, Leiden, mutația genei JAK 2 v617f și mutația genei protrombinei au fost normale. Ecografia abdominală a arătat o reducere suplimentară a volumului splinei fără complicații.
Figura 3A: CT 3. Vedeți Figura 3A
Figura 3B: Un TC abdominal cu material de contrast. Vedeți Figura 3B
SI este rezultatul ischemiei parenchimatoase și al necrozei țesuturilor datorate ocluziei uneia sau mai multor ramuri ale arterei splenice [4,5]. Splina, care are un aport vascular bogat (5% din debitul cardiac), este vulnerabilă la infarct din cauza lipsei circulației colaterale între ramurile arterei. SI se poate dezvolta secundar afecțiunilor cardiovasculare ca fibrilație atrială, anevrism ventricular și boli ale valvei cardiace. Alte tulburări etiologice non-cardiovasculare sunt boli hematologice, boli trombotice, boli ale țesuturilor colagenice, traume, intervenții chirurgicale abdominale sau infecții [6]. Simptomul predominant este durerea abdominală, uneori acută și severă, localizată în cadranul superior stâng asociată cu febră și vărsături. Examenele de laborator pot arăta un nivel crescut al serului de lactat dehidrogenază (LDH) și WBC.
În acest raport de caz, descriem un pacient internat la UCI din cauza șocului septic pneumococic care a dezvoltat MSI. Investigațiile efectuate la internare nu au identificat locul sursei primare a infecției [7]. În timpul spitalizării, au fost examinate acele boli care predispun la sepsis pneumococic și am găsit o boală celiacă (CD) necunoscută. În CD există o afectare a funcției imune a splinei, numită hiposplenism funcțional (FH). Acest lucru determină un număr redus de limfocite B cu memorie IgM și o activitate defectuoasă a moleculelor opsonizante (tuftsin, properdin) care participă la răspunsul imunității împotriva microorganismelor încapsulate [8-10]. Manifestările clinice ale sindromului septic la pacienții cu FH sunt: O bacteremie masivă cauzată de microorganisme încapsulate, fără sursă primară evidentă de infecție, debut rapid al simptomelor, șoc septic însoțit de coagulopatie intravasculară diseminată și rate de mortalitate de 50-70% [ 11].
Studiul splinei prin Doppler ecologic color abdominal cu agent de contrast și apoi prin CT abdominal, a relevat o pierdere completă a semnalului vascular așa cum este descris în MSI [12,13]. După cum sa menționat anterior, printre cauzele SI, evenimentele cardiovasculare sunt cele mai frecvente. Din acest motiv, pacientul a suferit o ecocardiogramă trans-esofagiană care a relevat o endocardită a valvei mitrale. În cadrul endocarditei infecțioase din partea stângă (IE), SI apare la aproximativ 40% dintre pacienți și se estimează că doar 5% din cazuri vor dezvolta un abces splenic [14]. Diferențierea abcesului de infarct este dificilă. Sepsisul continuu și hemoculturile recurente pozitive, care răspund slab doar la terapia cu antibiotice, sunt mai tipice pentru abces [15]. În timpul spitalizării, pacientul a fost febril pentru o lungă perioadă de timp, dar după începerea tratamentului cu antibiotice, hemoculturile au fost în mod repetat negative. Splina a fost investigată periodic cu Doppler ecologic color abdominal cu agent de contrast care a relevat lipsa absolută a semnalului vascular și reducerea progresivă a volumului.
PET-ul cu analogul glucozei 2- [18F] fluoro-2-deoxi-D-glucoză (18F-FDG) nu a detectat niciun fel de mation sau infecție. Pe baza acestor rezultate nu am efectuat splenectomie. SI singur nu este o indicație pentru intervenția chirurgicală, dar complicațiile precum infecția, ruptura sau durerea cronică sunt indicații pentru intervenția chirurgicală [16]. MSI la acest pacient se poate datora unui mecanism concomitent care acționează într-o manieră sinergică. Coagularea intravasculară diseminată apărută în timpul sepsisului ar putea determina o activare sistemică a coagulării sângelui, rezultând o tromboză a vasului mic [17,18]. Această afecțiune ar putea crește efectul ischemic creat prin ocluzia arterei splenice de către vegetația embolizată din valva mitrală. Pacienta a fost tratată cu anticoagulare parenterală pe tot parcursul șederii sale în spital. În cele din urmă a fost externată după două luni de spitalizare într-o stare clinică stabilă și i s-a recomandat urmărirea atentă. Un Doppler ecologic cu agent de contrast efectuat trei luni mai târziu, a arătat o reducere suplimentară a volumului splenic fără semne de abcese sau rupturi.
În concluzie, am dori să subliniem că la pacienții cu o bacteremie masivă cauzată de microorganisme încapsulate și fără sursă primară evidentă de infecție, poate fi util să investigăm și să testăm o boală potențială care să provoace un hiposplenism funcțional, uneori descoperit la vârsta adultă pacient pe care l-am descris în acest raport [19,20]. În plus, Doppler Echo-color cu agent de contrast este un instrument util pentru diagnosticarea și urmărirea pacienților cu SI. Acest test poate fi efectuat pe paturile pacienților și este deosebit de util pentru pacienții care nu sunt transportabili cu terapie intensivă [21].
- Infarctul splenic spontan ca cauză mai puțin frecventă a febrei la un pacient cu cirotă - ScienceDirect
- Obezitatea ca etiologie a bolii, tratament și considerații de management pentru pacientul obez -
- Biopsii duodenale de rutină pentru diagnosticarea bolii celiace
- Non; Glutenul celiac Sensibilitatea la grâu Fundația pentru boala celiacă
- Infarct splenic
