Luis Vitetta
1 unitate de integrare a sănătății, Școala de Medicină, Universitatea din Queensland, Australia;
Bill Anton
2 Path Lab, Melbourne, Australia
Abstract
Introducere
Înțelegerea diferenței dintre speranța de viață și durata de viață este cadrul pe care trebuie să provină orice revizuire selectivă a intervențiilor anti-îmbătrânire. Speranța de viață a omului este determinată din tabelele de date privind mortalitatea. Speranța de viață este o proiecție statistică a lungimii pe care se așteaptă să o trăiască ființa umană pe baza probabilităților și presupunerilor de predispoziții genetice, condiții de viață, descoperiri și progrese medicale, dezastre naturale și alți factori de mediu. Statisticile privind morbiditatea urmăresc cauzele presupuse ale decesului în timp, producând date privind tendințele care pot fi luate în considerare în tabelele speranței de viață (Mathers și Loncar 2005). Cu toate acestea, durata de viață este definită ca vârsta caracteristică a morții observată pentru cei mai în vârstă.
De-a lungul majorității istoriei umane înregistrate, s-a recunoscut că starea socio-economică și nutrițională slabă a fost puternic asociată cu scăderea speranței de viață, o tendință care este, de asemenea, foarte evidentă astăzi (US Gov. Report, 2005). Estimările actuale ale datelor arată că, în medie, speranța de viață a omului în țările occidentale este de aproximativ 82 de ani pentru femei și 80 de ani pentru bărbați (US Gov. Report, 2005).
În această scurtă analiză selectivă prezentăm dovezi științifice cu privire la ce practici anti-îmbătrânire pot servi mai bine pentru a crește speranța medie de viață și, prin urmare, durata de viață a omului.
Mod de viata
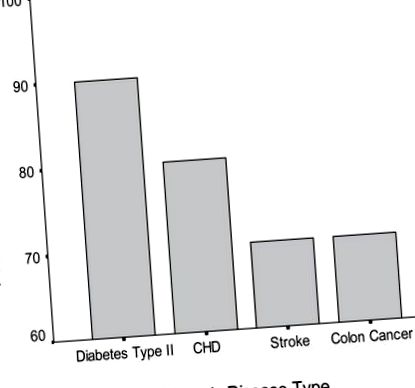
Willet (2002) a subliniat recent că factorii genetici și de mediu, inclusiv dieta și stilul de viață, contribuie atât la boli cardiovasculare, cancere și la alte cauze majore ale mortalității și că numeroase linii de dovezi indică faptul că factorii de mediu sunt cei mai importanți în determinarea prevenirii bolilor. Prin urmare, factorii de mediu pot avea cu siguranță cea mai puternică influență asupra speranței de viață și, prin urmare, a duratei de viață (Figura 1) (Willett 2002; Vitetta și colab. 2005). Împletit cu practicile nutriționale și stilul de viață este modificarea stresului vieții (Vitetta și colab. 2005).
Boli cronice prevenibile. Adaptat și modificat din Willett 2002.
Continuă să se adune dovezi care sugerează cu tărie că starea minții unei ființe umane - care asociază factorii psihosociali cu stările emoționale precum depresia și cu dispozițiile comportamentale care includ ostilitatea și stresul psihosocial al stilului de viață - pot influența direct și semnificativ funcția fiziologică umană și, la rândul ei, rezultatele sănătății.
Stresorii și reacțiile negative legate de stres au fost documentate și recunoscute ca având multiple sechele legate de starea de sănătate, iar expunerea la stres social cronic a fost asociată cu multe tulburări sistemice și mentale. Acestea au rezultate dăunătoare semnificative care scad semnificativ speranța de viață (Ader 2003; Vitetta și colab. 2005).
Diferite grupuri de cercetare susțin ideea că consecințele asupra sănătății sunt mai susceptibile să apară atunci când factorii de stres imprevizibili de natură socială induc cronic ajustări fiziologice și comportamentale care pot crea uzura funcțiilor fiziologice subiacente. Atunci când factorii stresanți contestă integritatea unui organism, se declanșează un set de reacții fiziologice pentru a contracara posibila amenințare și a ajusta setarea fiziologică a organismului la noua situație. Acest lucru a devenit cunoscut sub numele de răspuns la stres (Ader 2003). Stresorii și alegerile stilului de viață pot fi un factor semnificativ de declanșare a bolii prin imunomodularea sistemului imunitar care îmbunătățește susceptibilitatea bolii, care poate afecta apoi speranța de viață (Ader 2003). Modulația funcției imune influențată și exprimată de experiențele de viață stresante are o corelație semnificativă cu punctul de vedere al declanșatorului de mediu al lui Willett (2002) asupra inițierii bolii.
Nutriție
S-a demonstrat că factorii declanșatori pentru practici nutriționale adverse și inadecvate în copilărie au corelații psihosociale în viața adultă cu o creștere a riscului de boală (Jackson 2005). Obezitatea la om, influențată de alegeri dietetice slabe și inactivitate, este asociată în mod semnificativ cu un risc crescut de boli cronice, cum ar fi diabetul, hipertensiunea arterială, colesterolul ridicat, bolile cardiovasculare, astmul, artrita, unele tipuri de cancer și starea generală de sănătate slabă, care poate scade semnificativ speranța de viață a unui individ.
CR este legat de alegerile nutriționale. CR cu alimente slabe din punct de vedere nutrițional (de exemplu, consumul a jumătate din cantitatea unui fast-food) este încă o alegere nutrițională dezechilibrată, deși în porțiuni mai mici și încă nu oferă niciun avantaj pentru sănătate.
Recent a fost raportat și confirmat în continuare că o mai mare aderență la o dietă tradițională mediteraneană a fost asociată cu o reducere semnificativă a mortalității totale din toate cauzele (Trichopoulou et al 2003). Meyer și colegii (2006) au demonstrat că asocierea unei diete CR cu aderarea la o dietă de tip mediteranean care consta din cereale integrale, fasole, pește, fructe, ulei de măsline și multe tipuri diferite de legume a fost benefică pentru sănătatea inimii. Prin urmare, atunci când alegerile nutriționale optime sunt cuplate cu CR, este posibilă o creștere a speranței de viață. Astfel de practici nutriționale pot servi la extinderea în continuare a duratei de viață a omului.
Restricție calorică (CR)
Efectul CR și al exercițiului asupra supraviețuirii la șobolani. Adaptat și modificat din Holloszy 1995.
Au fost identificați numeroși biomarkeri ai RC la rozătoare, cum ar fi temperatura și DHEAS, nivelurile de insulină și glucoză (Roth și colab. 2002). Roth și colegii (2002) au observat recent că temperatura corpului și nivelurile de insulină și DHEAS au fost modificate și la primatele care au fost supuse CR, validând astfel utilitatea acestor biomarkeri la speciile cu viață mai lungă. Mai important, au arătat, de asemenea, că acești parametri au fost modificați la bărbații cu viață mai lungă. Împreună, aceste descoperiri susțin rolul acestor factori ca biomarkeri ai longevității la om.
Recent, a fost finalizat un studiu privind efectul unei diete CR de 6 luni asupra biomarkerilor metabolici, cum ar fi consumul de energie și stresul oxidativ la om (Heilbronn și colab. 2006). Raportul a arătat că CR prelungit a redus semnificativ doi biomarkeri de longevitate, și anume, nivelul insulinei la post și temperatura corpului. Acesta este primul studiu uman care arată că CR, pe lângă reducerile semnificative ale biomarkerilor bine-cunoscuți ai îmbătrânirii, a provocat și o adaptare metabolică la indivizii CR și o reducere a fragmentării ADN-ului care reflecta mai puține daune ADN (Heilbronn și colab. 2006) .
Legături genetice importante și regulatori ai duratei de viață a organismului au fost descoperite sub forma sirtuinelor (Sauve și colab. 2006) Sirtuinele sunt o familie de deacetilaze proteice dependente de NAD + larg distribuite în toate filele vieții. În organismele multicelulare, sirtuinele deacetilează histonele și factorii de transcripție care reglează stresul, metabolismul și căile de supraviețuire. Sir2 este membru fondator al unei familii numeroase și variate a acestor enzime sirtuin modificatoare de proteine, care reglează căile cheie de-a lungul biologiei, în eubacterii, arhee, eucariote și chiar viruși (Sauve și colab. 2006).
Legătura dintre CR și Sir2 și îmbătrânire a fost revizuită în altă parte (cf. pentru recenzii: consultați Sinclair și Guarente 1997; Guarente și Picard 2005; Suave și colab. 2006). Mai subliniem că există un corp extins de dovezi care sugerează că sirtuinele sunt implicate în promovarea longevității, în special a longevității asociate cu regimurile CR, în mai multe organisme. Relația sirtuin - CR rămâne totuși complexă. Recent, Suave și colegii săi (Sauve și colab. 2006) au emis ipoteza că SIRT1 la mamifere poate media schimbări semnificative în țesuturi și sisteme endocrine prin detectarea dietelor cu nivel scăzut de CR și declanșarea modificărilor fiziologice care beneficiază mamiferele cu sănătate și, prin urmare, longevitate.
S-a dovedit că factorii vegetali precum resveratrolul sporesc longevitatea în mai multe organisme prin reglarea Sir2/SIRT1 (cf. pentru revizuire: Baur și Sinclair 2006). La mamifere, există dovezi din ce în ce mai mari că resveratrolul poate preveni sau întârzia apariția cancerului, a bolilor de inimă, a leziunilor ischemice și induse chimic, a diabetului, a inflamației patologice și a infecțiilor virale. Aceste efecte sunt observate în ciuda biodisponibilității extrem de scăzute și a eliminării rapide a resveratrolului din circulație (Baur și Sinclair 2006). S-a sugerat că resveratrolul este asociat cu prevenirea bolilor legate de vârstă, cum ar fi cancerul, datorită reglării factorilor de transcripție care controlează supraviețuirea celulelor tumorale (Guarente și Kenyon 2000; Howitz și colab. 2003; Nemoto și colab. 2005; Storz 2005 ).
Mitocondriile și radicalii liberi
Faptul că mitocondriile au un rol esențial în furnizarea eficientă de energie către celulele eucariote este un fapt științific incontestabil. Mecanismele celulare care reglementează utilizarea energiei trebuie să funcționeze corespunzător pentru a susține viața. Adenozina 5 ′ - trifosfat (ATP) este molecula omniprezentă de stocare a energiei produsă în mai multe procese celulare. Metabolismul energiei aerobe necesită o investiție celulară, și anume oxigen molecular. Oamenii se bazează pe mitocondrii pentru a sintetiza și exporta ATP. Procesul este inițiat prin transferul de electroni derivați din surse de hrană de-a lungul unei serii de purtători ai lanțului respirator mitocondrial până când sunt consumați odată cu producția de apă din utilizarea oxigenului. O singură celulă eucariotă poate conține între câteva sute până la mii din aceste organite energetice. Odată cu îmbătrânirea crescută, există o scădere a producției de energie mitocondrială (Singh 2006). Prin urmare, la animalele aerobe, sănătatea mitocondrială pentru furnizarea eficientă de energie este esențială vieții.
Teoria radicalilor liberi a îmbătrânirii, așa cum a fost formulată de Denham Harman (1956), este susținută de observații că durata de viață a majorității organismelor este aproximativ proporțională cu rata metabolică a acestora și, prin urmare, cu viteza la care organismul generează specii de oxigen reactiv derivate din mitocondrii. (ROS). Cu toate acestea, acest punct de vedere este prea simplist și poate necesita modificări în limitele îmbătrânirii. ROS generat celular care contribuie la producția generală de ROS este aparent urmărit înapoi la mitocondrii (Lenaz și colab. 2002). ROS au fost privite ca fiind în mare parte dăunătoare sănătății și, prin urmare, îmbătrânirii. Rapoartele care arată că într-un spectru larg de specii de animale, antioxidanții dietetici sau restricția calorică, precum și antioxidanții chimici sau expresia crescută a proteinelor antioxidante, pot reduce producția de mitocondrii ROS, ceea ce se traduce printr-o prelungire a duratei de viață a acestor specii care au a servit pentru a susține teoria radicalilor liberi a îmbătrânirii (Orr și Sohal 1994; Sohal și Weindruck 1996; Parkes et al 1998; Sun and Tower 1999; Taub et al 1999; Schon 2000; Finkel și Holbrook 2000; Xu și Finkel 2002) se știe că ROS sunt generate în mai multe compartimente celulare și de mai multe sisteme enzimatice din interiorul celulei și au funcții de semnalizare celulară care sunt critice pentru funcția fiziologică normală a celulei (Rhee și colab. 2003; Linnane și colab. 2007a, 2007b, 2007c).
Contribuții importante la producerea ROS în celule, includ proteine din membrana plasmatică, cum ar fi familia în creștere a NADPH oxidazelor; metabolismul lipidic în peroxizomi; sinteza proteinelor în reticulul endoplasmatic; precum și activitatea diferitelor enzime citosolice, cum ar fi ciclooxigenazele (Linnane și Eastwood 2004; Moldovan și Moldovan 2004; Balaban et al 2005). Generarea ROS mitocondrială este o consecință a fosforilării oxidative, un proces care folosește oxidarea controlată și reglată a NADH sau FADH pentru a genera o energie potențială pentru protoni de-a lungul membranei interioare mitocondriale (ROS produs de mitocondrii s-a demonstrat că are importanță și specificitate roluri în semnalizarea celulară (Linnane și Eastwood 2004) Noțiunea că mitocondriile sunt singurul cel mai abundent loc de formare a ROS este în prezent o zonă de multă discuție și dezbatere (Rhee și colab. 2003; Balaban și colab. 2005; Linnane și colab. 2007b ).
Întreruperea funcțiilor mitocondriale a fost implicată în peste 40 de boli cunoscute, inclusiv ateroscleroza, bolile cardiace ischemice, cancerul, diabetul și bolile neurodegenerative, cum ar fi boala Alzheimer, boala Parkinson, boala Huntington și scleroza laterală amiotrofică (cf. pentru recenzii: McKenie 2004; Wallace 2005). Împreună, aceste date indică faptul că sănătatea mitocondrială este un factor important pentru sănătate și îmbătrânire. Cercetările actuale și viitoare ar avea ca scop îmbunătățirea și conservarea funcției mitocondriale. Deși sunt necesare cercetări suplimentare, rapoartele recente arată că suplimentarea cu coenzima Q10 arată promițătoare în menținerea sănătății mitocondriilor (Kagan și colab. 1999; Crestanello și colab. 2002; McKenzie și colab. 2004; Somayagulu și colab. 2005; Linnane și colab. . 2007b).
Mai mult, mimeticele antioxidanților celulari specifici, cum ar fi SOD/catalaza mimetică EUK-134, pot fi utilizate pentru a ajuta la reducerea radicalilor de oxigen și sunt deja în studii clinice (Melov și colab. 2000).
Hormoni
La om există o scădere progresivă a sintezei hormonale, precum și o pierdere a receptorilor hormonali cu vârsta. Vârstnicii au demonstrat niveluri semnificativ mai mici de producție a majorității hormonilor în comparație cu adulții tineri (Hertogue 2005). Există un volumos volum de literatură științifică care se ocupă cu deficitele hormonale ale îmbătrânirii. Adică, nivelurile de hormon de creștere (GH) și insulină precum factorul de creștere-1 (IGF-1), melatonină (nocturnă), TSH, hormoni tiroidieni (T3), calcitonină, DHEA (formă sulfatată și 17-ceto-urinară) metaboliți), aldosteron, estrogeni, testosteron la bărbați și femei s-a demonstrat că scad progresiv odată cu vârsta la adulți (pentru o analiză extinsă și referințe individuale, consultați Hertogue 2005).
Deficitul hormonal nu se limitează doar la menopauză, andropauză (menopauză masculină), somatopauză (deficit de hormon de creștere pentru adulți) și alte boli legate de hormoni sexuali, ele sunt acum implicate în condiții precum obezitatea (Cranny și colab. 2006; Pasquali și Gambineri 2006 ), osteoporoză (Bennett 2005), fibromialgie (Cleare 2004) sindrom de oboseală cronică (Cleare 2004) cancer (Simonenko și colab. 2006) probleme de deficit de atenție (Cheng 2005) și, probabil, altele care încă rămân de elucidat.
Tratamentele de medicină convențională s-au întrerupt doar pentru a aborda epuizarea hormonală, ignorând deficiențele ușoare și moderate; întrucât modelul de medicamente anti-îmbătrânire se concentrează pe deficiențe ușoare, moderate și severe. Simptomele și severitatea simptomelor vor fi proporționale cu nivelul de deficiență pentru fiecare hormon (Anton și colab. 2005). Abia recent, știința endocrinologiei a început să se concentreze pe metode avansate de testare, luând în considerare intervalele de referință bazate pe vârstă, precum și pe sex, nivelurile hormonilor liberi sau biodisponibili față de nivelurile hormonilor legați și raporturile dintre hormonii antagonici majori pentru a titra pacienții și a obține un nivel optim echilibru. Titrarea și echilibrul optim au fost utilizate cu hormoni tiroidieni și insulină și nu au fost aplicate universal la toți ceilalți hormoni, până în ultima perioadă. Cercetările continue în domeniul longevității ar trebui să includă utilizarea precursorilor nutrienți și hormonali pentru a spori capacitatea organismului de a produce mai mulți compuși hormonali proprii, limitând astfel daunele structurale și ADN din ultimele decenii de viață.
Concluzii finale
Cea mai pură utilizare a termenului „îmbătrânire biologică” îl limitează exclusiv la modificările moleculare. Hayflick (2003) definește îmbătrânirea în sistemele biologice ca un proces stocastic care are loc sistemic după maturitatea reproducerii la animale care ating o dimensiune fixă la vârsta adultă și că este apoi cauzat de pierderea crescândă a fidelității moleculare care depășește în cele din urmă capacitatea de reparare. Acest lucru crește apoi vulnerabilitatea la patologie sau la bolile asociate vârstei. În plus, există o finitudine asociată cu îmbătrânirea care duce în cele din urmă la moarte (Hayflick 2003). Grimley Evans (2000) a definit modificările senescente ca modificări structurale și funcționale de novo care nu fac parte din programul de dezvoltare. În această scurtă revizuire selectivă și sintetică, am rezumat dovezile științifice care pot preveni bolile și menține integritatea moleculară a organismului, extinzând astfel speranța medie de viață în timp ce operează în cadrul funcției și reparării fiziologice normale. Constatăm că, deși îmbătrânirea nu este ireversibilă și inevitabilă, anumiți factori cheie pot adăuga beneficii semnificative speranței de viață medii umane.
Există o gamă largă de literatură științifică care concluzionează că factorii de modificare a stilului de viață care optimizează nutriția, activitatea fizică și sănătatea mintală au corelații semnificative cu reducerea riscurilor de boală în viața ulterioară, care se traduce printr-o speranță de viață medie crescută. Mai mult, deși corectarea tuturor deficitelor hormonale printr-o terapie adecvată de substituție hormonală multiplă nu este posibilă în prezent, terapia hormonală constituie o soluție viabilă pentru prevenirea și tratarea majorității deficitelor hormonale datorate îmbătrânirii patologice. Hertogue (2005) a raportat recent că, deși în prezent nu suntem capabili să abrogăm senescența prin tratamente hormonale din cauza indisponibilității ca medicamente pentru toți hormonii care scad odată cu vârsta, viitorul pare promițător.
Ca notă finală; odată cu debutul secolului 21, este evident că ne aflăm la orizontul unei revoluții în terapiile și tehnologiile anti îmbătrânire. O modalitate terapeutică promițătoare, conceptul de tratamente cu celule stem, va permite, în următorul deceniu, o calitate semnificativ extinsă a sănătății și, de asemenea, poate crește și mai mult speranța medie de viață a omului. Progresele recente ale marilor corporații, atât private, cât și publice, au documentat că suntem deja capabili să luăm celule stem de la un individ și să copiem selectiv aceste celule împreună cu componentele ADN-ului lor. Astfel, este posibilă restaurarea și întinerirea proprietăților pe care corpurile umane le pierd pe măsură ce îmbătrânesc. Prin urmare, perspectivele utilizării derivaților celulelor stem embrionare umane în medicina regenerativă sunt semnificative (Trouson 2006). Dacă se pot realiza contribuțiile potențiale la medicina regenerativă umană, vor fi posibile modificări semnificative și îmbunătățirea speranței medii de viață la om.
- Dietele keto sunt efectele lor metabolice numai datorită restricției calorice
- Cum să îmbrățișați stilul de viață mediteranean și să vă bucurați de sănătatea stelară Revista Fox
- Cum Cindy a lovit zahărul de la bordură și și-a redat sănătatea - prosperă nutriția și yoga
- Sănătate și jargon alimentar decodificat pentru nutriția dvs. în Thousand Oaks
- Beneficiile pentru sănătate ale kefirului, date nutriționale, prepararea kefirului acasă