Subiecte
Abstract
Răspândirea rezistenței paraziților la artemisinină amenință terapiile antimalarice actuale, evidențiind nevoia de noi medicamente cu moduri de acțiune alternative. Deoarece doar 0,2-1% dintre paraziții asexuali se diferențiază în forme sexuale, competente în materie de transmisie, vizarea acestui blocaj natural oferă o cale tangibilă de a întrerupe transmiterea bolii și de a atenua selecția rezistenței. Aici vă prezentăm un ecran de mare capacitate de gametogeneză împotriva unui
70.000 bibliotecă de diversitate de compuși, identificând șaptesprezece molecule asemănătoare medicamentelor care vizează transmisia. Moleculele lovite au profiluri variate de activitate, inclusiv masculin specific, masculin cu acțiune dublă - feminin și dual-asexual-sexual, cu unul promițător N-((4-hidroxicroman-4-il) metil) -sulfonamidă eșafodaj care sa dovedit a avea activitate sub-micromolară in vitro și in vivo eficacitate. Dezvoltarea de potențiale cu moduri de acțiune axate pe stadiile sexuale ale dezvoltării parazitului malariei oferă o bază neexplorată anterior din care pot fi dezvoltate viitoare terapii, capabile să prevină transmiterea paraziților prin populație.
Introducere
Succesul în reducerea poverii bolii malariei de la începutul mileniului a cunoscut schimbarea paradigmei de la control la unul de eliminare regională și eventuală eradicare globală 1,2. Implementarea coordonată a măsurilor stabilite a condus la reduceri substanțiale ale mortalității și morbidității și a contribuit la eliminarea malariei în 10 țări 3. Cu toate acestea, pentru a se asigura că aceste câștiguri sunt menținute și accelerate, și având în vedere îngrijorarea apariției malariei multirezistente în Asia de Sud-Est 4, sunt necesare terapii noi și inovatoare pentru a preveni o inversare potențială a numărului în următorii ani.
2-5 oochiste (comparativ cu 10 11 paraziți asexuali la o gazdă infectată) 10 .
Conceptul de vizare specifică a etapelor sexuale, ca strategie de reducere a incidenței malariei, a primit un interes crescut recent 11. Acest lucru urmează (re) aprecierii emergente că vizarea parazitului malariei la blocajul acut al populației de transmitere are beneficii potențiale asupra terapiei vizate asexual, atât ca mijloc de a întrerupe ciclul infecției, dar, în mod critic, și ca o barieră în calea răspândirii alelelor rezistente la medicamente. 11.12. Conceptual, evoluția rezistenței la medicamente care vizează în mod specific etapele de transmitere va dura mult mai mult decât pentru antimalarile convenționale, deoarece presiunea selectivă se aplică doar populației relativ mici (care nu replică) de gametocite în comparație cu medicamentele care vizează
Aici am întreprins HTS pentru o mare bibliotecă de diversitate chimică imparțială, unde filtrul principal pentru identificarea loviturilor este în mod specific capacitatea de a viza transmisia însăși, utilizând Pf DGFA. Profilarea rezultatelor selectate a relevat o gamă variată de activități, atât dependente, cât și independente de activitatea asexuată, iar unele care prezintă activitate specifică sexului gametocitului. Arătăm că moleculele exemplare din fiecare clasă de activitate par să inhibe transmiterea prin diferite mecanisme și că acest lucru se traduce direct într-o blocadă a transmiterii țânțarilor. În special, identificăm un roman N-((4-hidroxicroman-4-il) metil) sulfonamidă (N-4HCS) schelă care inhibă rapid procesul de formare a gametilor masculini in vitro și blochează transmiterea in vivo într-un model de malarie la șoareci. Schela N-4HCS prezintă o tractabilitate chimică excelentă, proprietăți fizico-chimice favorabile și promite o dezvoltare ulterioară ca terapie specifică transmisiei, care ar putea fi utilizată în noile terapii combinate antimalarice.
Rezultate
Gametocite și compuși vizați asexuat în cadrul GHCDL
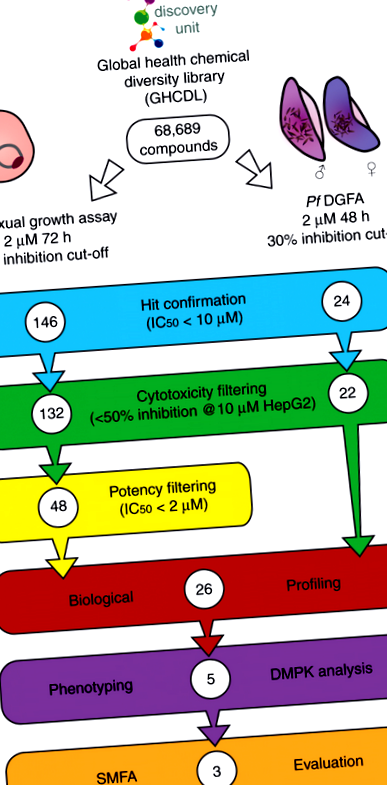
Global Health Chemical Diversity Library (GHCDL) cuprinde 68.689 de compuși diferiți de moleculele deja cunoscute ca având proprietăți antimalarice. Toate moleculele posedă proprietăți fizico-chimice asemănătoare plumbului și sunt aranjate în grupuri similare din punct de vedere structural, cuprinse între 3 și 14 compuși. DGP Pf măsoară viabilitatea funcțională a gametocitelor masculine și feminine din stadiul V, după cum este raportat prin capacitatea lor de a forma gamete masculine și feminine 23. GHCDL a fost selectat în Pf DGFA la 2 µM cu o incubație de 48 de ore înainte de declanșarea formării gametilor, producând 24 de lovituri cu un IC50 Fig. 1
Proiectarea cascadei de progresie. Global Health Chemical Diversity Library (GHCDL) a fost analizat în paralel împotriva Plasmodium falciparum stadiu asexual și gametocit masculin și feminin. Activele au fost reconfirmate și compușii citotoxici au fost eliminați. Loviturile asexuale au fost filtrate în continuare în funcție de potență și 26 de compuși selectați pentru o profilare suplimentară pe baza potenței și disponibilității comerciale. Cinci compuși cu proprietăți diferite de blocare a transmisiei au fost investigați în continuare pentru activitatea fenotipului împotriva gametogenezei masculine și a proprietăților lor fiziochimice (DMPK) investigate. Activitatea a trei molecule a fost confirmată prin testul standard de alimentare cu membrană (SMFA)
În paralel, GHCDL a fost testat împotriva stadiilor de sânge asexuate la 2 µM pe o incubare de 72 de ore utilizând activitatea lactatului dehidrogenază ca citire surogat pentru creșterea paraziților. Screeningul a produs 146 de accesări cu un IC50 Fig. 2
Am investigat dacă compușii afectați ar putea inhiba invazia și creșterea stadiului hepatic într-un mediu stabilit P. berghei testul invaziei HepG2 a sporozoitului luciferazei 24. Doar un compus, DDD01243506, a prezentat activitate submicromolară împotriva P. berghei invazie în stadiu hepatic la un nivel similar cu activitatea sa împotriva asexuaților (Pb ficat IC50 = 0,52 µM; HepG2 TOX50 ≥ 50 (M; Luciferază recombinantă IC50 ≥ 50 (M; Pf asexual IC50 = 0,66 (M, date suplimentare 3). Într-adevăr, niciun compus activ PFA DGFA nu a prezentat activitate specifică împotriva stadiilor hepatice, probabil fie din cauza diferențelor fundamentale în biologia celulară între diferitele etape ale parazitului, fie a diferențelor specifice speciilor dintre P. falciparum și P. berghei.
Pentru a evalua pe deplin puterea conductei de screening și pentru a înțelege modul în care categoriile de profilare s-ar putea traduce prin terapie de blocare a transmisiei, au fost selectați cinci compuși pentru studii suplimentare bazate pe potență și profil (Fig. 3): DDD01027599 (DDD599/BPCA) și DDD01245291 (DDD291) reprezentând activele asexuale și Pf DGFA în două etape, respectiv; DDD01249504 (DDD504) și DDD01255968 (DDD968) reprezentând activi specifici masculin și, respectiv, specific gametocitului; și în cele din urmă, DDD01035881 (DDD881), unul dintre clusterele N-4HCS reprezentând activi specifici gametilor masculini. În rezumat, eforturile noastre de screening au identificat 17 blocaje de transmisie confirmate și 9 conducte de vizare asexuată pentru dezvoltare ulterioară.
Structura chimică a compușilor GHCDL selectați pentru studii ulterioare. Cinci compuși care prezintă o serie de activități de blocare a transmisiei în etapa de profilare au fost selectați pentru un studiu detaliat. DDD01027599 (care se găsește de fapt BPCA - vezi Fig. 1-2 suplimentară) și DDD01245291 sunt active împotriva gametocitelor și asexuatelor; DDD01255968 și DDD01249504 sunt active în mod specific împotriva gametocitelor masculine; și DDD01035881 vizează în mod specific formarea gametilor masculini
Impactul fenotipic al compușilor asupra gametogenezei masculine
Evoluția in vitro urmată de analiza întregului genom este abordarea principală utilizată în prezent pentru a înțelege cum acționează compușii în paraziții malariei 25. Deoarece în prezent nu este fezabil să se genereze mutanți rezistenți la compuși care sunt activi doar în stadiul gametocitelor (generarea rezistenței necesită runde extinse de replicare în prezența compusului), s-au efectuat teste fenotipice de imunofluorescență pentru a evalua activitatea compusului la formarea gametilor masculini. Gametocitele tratate cu 10 uM din fiecare compus au fost prelevate la 0, 2, 3, 4, 6, 8, 10 și 20 de minute după inducerea formării gametilor înainte de imagistică (Fig. 4). Celulele masculine individuale au fost apoi extrase din imagini și analizate pentru a determina forma și numărul de cromozomi haploizi/conținutul ADN pentru a măsura cantitativ progresia replicării ADN-ului (n = 198-668 celule) (Fig. 5a).
Profilare chimică preliminară, analiză SAR și DMPK
- Evaporator imprimat 3D, All-in-One pentru generarea de abur solar cu eficiență ridicată sub 1 Soare
- Un studiu al rezultatelor pe termen lung pentru a evalua reducerea riscului rezidual STatin cu EpaNova în HiGh
- 32 de perechi de tocuri de înălțime pentru înlocuirea capacelor de reparații, seturi de instrumente de reparare pentru tocuri pentru femei, dibluri
- Britney Spears Pierdere în Greutate Antrenament Repetări ridicate, mișcări izolate
- Construirea unui gândac Cum mediul larval duce la performanța adulților într-un gândac cu coarne