ARTICOL ORIGINAL
Aportul alimentar la pacienții cu boli inflamatorii intestinale
Alice Freitas da Silva; Maria Eliana Madalozzo Schieferdecker; Heda Maria Barska dos Santos Amarante
RAŢIONAL: Pacienții cu boli inflamatorii intestinale pot prezenta deficiențe nutriționale.
OBIECTIV: Verificați adecvarea aportului de pacienți cu boala Crohn și retocolită ulcerativă nespecifică.
METODE: Pentru a evalua ingestia a 55 de pacienți, 28 cu boala Crohn și 27 cu ulcerativă retocolită asistată în ambulatoriu de gastroenterologie, se utilizează înregistrarea alimentară a 24 de ore și o întrebare de frecvență alimentară. Activitatea inflamatorie a bebelușului a fost afectată de nivelurile de proteine C reactive și de Institutul Harvey și Bradshaw. Pentru compararea mediilor utilizate pentru teste și nerecomandate, pentru mediile non-parametrice, pentru testul Mann-Whitney, luând în considerare nivelul de semnificație al valorii p
Descriptori: Copilă coroană. Proctolit. Aportul alimentar.
Boala inflamatorie intestinală (DII) este o denumire generală dată unui grup de cauze inflamatorii de deshidratare, care implică tractul gastro-intestinal, care poate fi împărțit în două grupe de principii, colita ulcerativă (DCCI). Cauza DII a fost descoperită și există o interacțiune între factorii genetici, de mediu și imuni 33 .
Starea nutrițională a DII noastre poate fi afectată de reducerea ingestiei de alimente cauzată de simptomele gastrice, dar de absorbția și tratamentul medicamentelor, cu modificări ale fazei majore a alăptării. Pe lângă reducerea ingestiei de alimente, a simptomelor simptomelor gastrointestinale, cum ar fi anorexia, incontinența, greața și vărsăturile, pacienții pot crește, de asemenea, nevoia de nevoi nutriționale ca o consecință a activității inflamatorii și a complicațiilor de 25 .
Ainda não está claro se a manipulação dietetica combinada com o o tratamento medicamentoso poderia melhorar os sintomas ou induzir a remissão da doença. Intoleranțele alimentare observate variază și trebuie tratate individual 26. Deficiențe nutriționale variabile pentru DII, cum ar fi fierul, cianocobalamina, folatul, calciul și zincul 18. Deficitul de folat poate provoca anemie și are, de asemenea, un risc major de cancer de colon și de retină 24. Vitamina D reglează funcția sistemului imunitar și proliferarea și diferențierea testiculului 20, dar este important să se mărească metabolismul organismului, numai cu calciu 28. Alți nutrienți importanți în metabolismul vitaminei K, prezenți în formarea și reabsorbția acidului 7 .
Luând în considerare modificările care provoacă deficiența nutrienților și influența asupra ingestiei alimentare, este dificil să se evalueze adecvarea ingestiei alimentare a pacienților cu DII în diferite stări de activitate inflamatorie.
Studiu transversal cu criterii de includere în diagnosticul bolii inflamatorii intestinale, în condiții fizice de evaluare antropometrică, cu vârsta de cel puțin 18 ani, în perioada 17 ianuarie - 14 aprilie 2008. A 55-a Universitate a Pacienților Gastronomici Federal din Paraná, în Curitiba, PR, Brazilia că particip la studiul pentru studenți cu privire la facilitățile și asimilarea Consimțământului gratuit de viață și acordeon cu aprobarea Comitetului de etică al spitalului clinic al Universității Federale din Pa o numărul 1121.160/2005-10.
Informații relative în momentul diagnosticului, operații preoperatorii, alte diagnostice asociate și utilizarea medicamentelor pentru îngrijirea prenatală. Pacienții au pus întrebări cu privire la prezența simptomelor gastro-intestinale, preferințelor și/sau intoleranțelor alimentare, modificarea aportului alimentar, luând în considerare cât timp și motiv, ingestia de lichiditate pentru copii.
Pentru a verifica activitatea inflamatorie a DC și RCUI, luăm în considerare valorile reactivei proteinei C (PCR) realizate prin nefelometrie, luând în considerare valorile normale ale valorilor inferioare de 0,50 mg/dl. Am luat în considerare examinările PCR care au fost aprobate și implementate în ultimele 15 zile. Pentru pacienții cu DC, aceștia sunt obișnuiți (indicarea activității de propus pentru Harvey și Bradshaw 17 în timpul consilierii medicale. Și 16 activitate moderată și majoră 16 activitate gravă .
Pentru a analiza consumul de alimente pentru pacienți, în urma anamnezei alimentelor, care se referă la consumul obișnuit de 24 de ore (R24H). În acest caz, pacienții au răspuns la un chestionar privind frecvența alimentelor, care a fost analizat în conformitate cu Guia Alimentar pentru populația braziliană 4. Pentru a calcula costul consumului de alimente, utilizați software-ul Dietwin Nutrition Evaluation 6 .
Rezultatele sunt prezentate luând în considerare media și dezvoltarea. Pentru compararea mediilor utilizate pentru teste și nespecificate, și pentru medii non-parametrice, testul Mann-Whitney, având în vedere nivelul de semnificație valor p
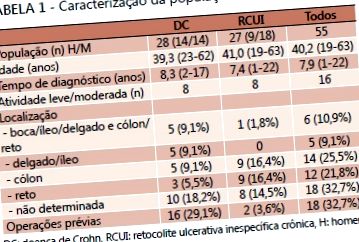
Foram avaliados 55 de pacienți cu boală inflamatorie intestinală, cu o vârstă cuprinsă între 19 și 63 de ani și un timp de diagnostic de 7,9 ani (1 la 22). Toți sunt 80% (44) din Curitiba și regiunea metropolitană, 58% (32) din sexul feminin și au 40 de ani (Tabelul 1).
Clasificarea activității coardei cu PCR a fost comparată cu activitatea persoanelor Harvey și Bradshaw cu pacienți cu DC, iar PCR cu acest indice clasifică 30,8% dintre pacienții cu un risc de 69,2%. Dintre pacienții cu RCUI, 39% sunt în repaus și 61% sunt în remisie. Zece pacienți, 17 terapii prescrise cu corticosteroizi.
Menos pe care 20% dintre pacienți îl raportează la practicarea activităților fizice, îl trimit ca fiind cei mai obișnuiți, fotbal la sfârșitul săptămânii, gimnastică și musculatură, realizat cu o frecvență media de trei săptămâni pentru săptămână.
Pacienții cu DC, în timp ce se află în activitate după remisiunea bolii, au energie inactiv mai mică decât este necesar, deoarece nu sunt semnificative. Ingerarea protetică pentru pacienții majori, după caz, cu diferență semnificativă pentru pacienții în remisie (p
Pacienții cu RCUI în activitate prezintă un aport scăzut de energie și kcal/kg per peso (p
Acordul cu frecvența alimentelor, cât de scăzută este ingestia de leguminoase, fructe, latină și fecale, ingestia adecvării amilazei și ingestia de fructe și fructe în exces (Tabelul 4). Cele mai frecvente intoleranțe sunt adesea legate de pacienții cu lactoză (50%), fructe și horticultură (33%), carne (20%), fructe/soia și doce (12%), condimente (9%) și prăjite și oleaginos ( 9%). Intoleranță la pâine/masă, cafea și agenți frigorifici pentru pacienții cu frecvență (5%) a pacienților.
Estudos com calorimetria indireta verificaram that o gasto energetático basal de patients com DII em remissão não sample sa differenceça quado comparado com cheresá Saudi 9. O chiar verificare-se em pacienții com DC em ativitate sem uz de corticosteróides 30, entretanto os patients em atividade e emissão that recebiam corticosteroids tiveram gasto energetiko em repouso maior that dos control 2 .
Subliniați studiile găsite în literatura de specialitate Tenham a folosit metodologii diferențiate pentru a evalua ingestia de deficiențe, ceea ce nu este cazul oamenilor.
Intoleranțele la alimentele relaționale, în principal lactoză, fructe, horticultură și furaje pot fi afectate de consumul redus de alimente din aceste grupuri. Porțiunile diareice incluse în recomandările Ministerului Sănătății din Brazilia 4 .
Incidența creșterii fructelor și legumelor nu este aceeași cu observarea pacienților cu DII 32. O reducere a ingestiei de fructe și legume are ca rezultat ingestia de fibre, care poate fi asociată cu orientarea pe termen lung a laptelui activ, pentru reducerea motilității intestinale și pentru fermentarea bacteriană și pentru evitarea simptomelor abdominale. Cu toate acestea, unii pacienți continuă cu restricția că activitatea este controlată 1, ceea ce contribuie la ingestia de micronutrienți și substanțe antioxidante 9. Excluderea fructelor și a horticulturii a contribuit, de asemenea, la ingestia scăzută de folat la pacienții cu studii RCUI de Jowett și colab. 19 .
Relația de intoleranță la lactoză este o problemă foarte importantă și poate afecta ingestia de calciu. Într-un test de toleranță orală la lactoză la 67 de pacienți cu DII și 25 martori, nu a fost observată nicio observație între grupurile de 22. Ingerarea de calciu la pacienții cu DII (n = 152) la pacienții majori cu controale saudite (n = 73). Deficiențele majore au fost găsite la 47% (n = 71) dintre pacienții care urmau o dietă cu restricție de lactoză și au avut teste de toleranță pentru anomalii la 25% (n = 18) dintre pacienții 31. Aceste semne indică importanța respectării toleranței individuale în alimente și derivate, identificarea aportului acestor alimente este legată de intoleranța la lactoză sau alergia la proteine 8 .
Între pacienții care au studiat, aceștia au o deficiență a ingestiei de anexe feroase la pacienții cu RCUI în remisie. Amintiți-vă că Heatley 18 a observat în studiul său că a existat un deficit de mai mult de un pacient la pacienții cu RCUI.
Intoleranța față de pacienți sau pacienții cu DII legată de unii pacienți poate fi explicată prin producerea de medicamente anticorozive Saccharomyces cerevisiae (ASCA pozitiv), în principal naqueles individ cu o boală localizată în intestin. Cât mai curând posibil, studiul intoleranței la posibilitatea cauzelor în masă cauzate de conservanți 5 .
Pe lângă ingestia de legume, fructe și lapte și ingestia majoră de proteine animale, cereale, carbohidrați simpli și mândri în rândul pacienților cu RCUI în raport cu riscul major de a dezvolta cancer de colon 29. Ingerarea alimentelor procesate și a alimentelor rafinate, caracteristică dietei moderne, aduce atingere adăugării unui factor de risc legat de consumul de sulfit în prezența alimentelor procesate 23. Beneficiile alimentelor pentru pacienți pot influența ingestia de substanțe nutritive importante 19 .
Este necesar să constatăm că nu trebuie să lucrăm la apenas de avocado un aport nutritiv al corzii cu un recorder alimentar, fără a lua în considerare utilizarea suplimentelor, folatului, calciului și vitaminei D pentru pacienți. Să știți că tratamentul DII cu sulfasalazină este redus prin absorbția acidului folic și a corticosteroizilor prin absorbția calciului 33. Am stabilit că pacienții tratați cu corticosteroizi ar trebui să primească supliment de colecalciferol de 800-1000 UI/zi și 1000 mg/zi de calciu ionic 21. Dieta trebuie să fie echilibrată și nerestrictivă, iar pacienții, în principal în remisie pe apă, ar trebui încurajați să-și îmbunătățească suplimentele alimentare 32 .
Deficiența Houve a aportului de hrană DC și RCUI atât în activitate, cât și în remisie. Aceste deficiențe se referă în principal la aportul de macronutrienți, cum ar fi energia și fibrele și micronutrienții, calciu, acid folic, colecalciferol, tocoferol, menadionă, retinol, riboflavină, piridoxină, tiamină. Deficiențele constatate pot afecta negativ cursul alăptării și pot justifica necesitatea unei intervenții nutriționale cu acești pacienți.
REFERINȚE
1. Agdassi E, Wendland BE, Stapleton M, Raman M, Allard JP. Adecvarea aportului nutrițional la o populație canadiană de pacienți cu boală Crohn. J Am Diet Conf. Univ. 2007; 107 (9): 1575-1580. [Link-uri]
2. Al-Jaouni R, Hébuterne X, Pouget I, Rampal P. Metabolismul energetic și oxidarea substratului la pacienții cu boala Crohn. Nutriție. 2000, 16: 173-178. [Link-uri]
3. Cel mai bun WR. Prezicerea Infexului asupra activității bolii Crohn din indicele Harvey-Bradshaw. Inflamm intestin Dis. 2006; 12 (4): 304-310. [Link-uri]
4. Brazilia. Ministerul Sanatatii. Ghid pentru populația braziliană. Brasilia, DF; 2005. [Link-uri]
5. Brunner B, Scheurer U, Seibold F. Diferențe în intoleranța la drojdie între pacienții cu boală Crohn și colită ulcerativă. Dis Colon Rectum. 2007; 50 (1): 83-88. [Link-uri]
6. Dietwin ® (Software de evaluare nutrițională). Versiunea 2.2.24. Brazilia, 1995-2007.
7. Duggan P, O'Brien M, Kiely M, McCarthy J, Shanahan F, Cashman KD. Starea vitaminei K la pacienții cu boala Crohn și relația cu fluctuația osoasă. Am J Gastroenterol 2004; 99 (11): 2178-2185. [Link-uri]
8. Ferguson LR, Shelling AN, Browning BL, Huebner C, Petermann I. Gene, dietă și boli inflamatorii intestinale. Mutat Res. 2007; 622: 70-83. [Link-uri]
9. Filippi J, Al Jouani R, Wiroth JB, Hébuterne X, Schneider SM. Deficiențe nutriționale la pacienții cu boală Crohn în remisie. Inflamm intestin Dis. 2006; 12 (3): 185-191. [Link-uri]
10. Consiliul pentru alimentație și nutriție. Institutul de Medicină. Aporturi dietetice de referință pentru calciu, fosfor, magneziu, vitamina D. și fluor. Washington DC: National Academy Press; 1997. [Link-uri]
11. Consiliul pentru alimentație și nutriție. Institutul de Medicină. Aporturi dietetice de referință pentru tiamină, riboflavină, niacină, vitamina B6, folat, vitamina B12, acid pantotenic, biotină și colină. Washington DC: National Academy Press; 1998. [Link-uri]
12. Consiliul pentru alimentație și nutriție. Institutul de Medicină. Aporturi dietetice de referință pentru vitamina A, vitamina K, arsenic, bor, crom, cupru, iod, fier, mangan, molibden, nichel, siliciu, vanadiu și zinc. Washington DC: National Academy Press; 2000. [Link-uri]
13. Consiliul pentru alimentație și nutriție. Institutul de Medicină. Aporturi dietetice de referință pentru vitamina C, vitamina E, seleniu și carotenoizi. Washington DC: National Academy Press; 2000. [Link-uri]
14. Consiliul pentru alimentație și nutriție. Institutul de Medicină. Consumuri dietetice de referință pentru apă, potasiu, sodiu, clorură și sulfat. Washington DC: National Academy Press; 2004. [Link-uri]
15. Consiliul pentru alimentație și nutriție. Institutul de Medicină. Aporturi dietetice de referință pentru energie, carbohidrați, fibre, grăsimi, acizi grași, colesterol, proteine și aminoacizi (macronutrienți). Washington DC: National Academy Press; 2005. [Link-uri]
16. Geerling BJ, Badart-Smook A, Stockbrügger RW, Brummer RJM. Stare nutrițională cuprinzătoare la pacienții diagnosticați recent cu boală inflamatorie intestinală comparativ cu controalele populației. Eur J Clin Nutr. 2000; 54: 514-521. [Link-uri]
17. Harvey RF, Bradshaw JM. Un index simplu al activității bolii Crohn. Lancet 1980; 1: 514. [Link-uri]
18. Heatley RV. Evaluarea stării nutriționale în bolile inflamatorii intestinale. Gut 1986; 27: 61-66. [Link-uri]
19. Jowett SL, Seal CJ, Phillips E, Gregory W, Barton JR, Welfare MR. Convingeri dietetice ale persoanelor cu colită ulcerativă și efectul lor asupra recăderii și aportului de nutrienți. Clin Nutr. 2004; 23 (2): 161-170. [Link-uri]
20. Leslie WD, Miller N, Rogala L, Bernstein CN. Starea vitaminei D și densitatea osoasă în bolile inflamatorii intestinale diagnosticate recent: Studiul de cohortă IBD din Manitoba. Am J Gastroenterol 2007; 102: 1-9. [Link-uri]
21. Lochs H, Dejong C, Hammarqvist F, Hebuterne X, Leon-Sanz M, Schütz T, van Gemert W, van Gossun A, Valentini L, Lübke H, Bischoff S, Engelmann N, Thul P . ESPEN Guidelines on Enteral Nutriție: gastroenterologie. Clin Nutr 2006; 25: 260-274. [Link-uri]
22. Madrid RB, Benarroch HS, Sánchez SM, Sánchez FG, Meroño AA, Martínez JM. Malabsorbția lactozei la pacienții cu boală inflamatorie intestinală infantilă: este justificată excluderea produselor tuturor pacienților? An Med Interna. 2004; 21 (5): 212-214. [Link-uri]
23. Magee EA, Edmond LM, Tasker SM, Kong SC, Curno R, Cummings JH. Asocieri între dieta și activitatea bolii la pacienții cu colită ulcerativă folosind o metodă nouă de analiză a datelor. Jurnal de nutriție. 2005; 4: 7. [Link-uri]
24. Mathers JC. Inversarea hipometilării ADN-ului prin suplimente de acid folic: rol posibil în prevenirea cancerului colorectal. Bun 2005; 54: 579-581. [Link-uri]
25. O'Sullivan M, O'Morain C. Nutriția în bolile inflamatorii intestinale. Best Practice Res Clin Gastroenterol. 2006; 20 (3): 561-573. [Link-uri]
26. Rajendran N, Kumar D. Rolul dietei în gestionarea bolilor inflamatorii intestinale. World J Gastroenterol. 2010; 16 (12): 1442-1448. [Link-uri]
27. Palaniappan U, Cue RI, Payette H, Gray-Donald K. Implicații ale variabilității de zi cu zi asupra măsurătorilor consumului obișnuit de alimente și nutrienți J Nutr. 2003; 133: 232.235. [Link-uri]
28. Rodriguez-Borez L, Barahona-Garrido J, Yamamoto-Furusho JK. Aspecte de bază și clinice ale osteoporozei în bolile inflamatorii intestinale. World J Gastroenterol. 2007; 13 (46): 6156-6165. [Link-uri]
29. Rosman-Urbach M, Niv Y, Birk Y, Morgestern S, Schwartz B. Relația dintre obiceiurile nutriționale adoptate de colita ulcerativă relevantă pentru pacienții cu dezvoltare a cancerului în etapele de remisie clinică și parametrii molecular-genetici. Br J Nutr. 2006; 95: 188-195. [Link-uri]
30. Schneeweiss B, Lochs H, Zauner C, Fischer M, Wyatt J, Maier-Dobersberger T, Schneider B. Metabolismul energiei și al substratului la pacienții cu boală Crohn activă. J Nutr. 1999, 129: 844-848. [Link-uri]
31. Silvennoinen J, Lamberg-Allardt C, Kärkkäinen M, Niemelä S, Lehtola J. Aportul dietetic de calciu și relația sa cu densitatea minerală osoasă la pacienții cu boală inflamatorie intestinală. J Intern Med 1996; 240: 285-292. [Link-uri]
32. Valentini L, Schaper L, Buning C, Hengstermann S, Koernicke T, Tillinger W, Greglielmi FW, Norman K, Buhner S, Ockenga J, Pirlich M, Lochs H. Malnutriție și afectarea forței musculare la pacienții cu boala Crohn și ulcerative colită în remisie. Nutriție 2008; 24: 694-702. [Link-uri]
33. Wild GE, Drozdowski L, Tartaglia C, Clandinin MT, Thomson ABR. Modularea nutrițională a răspunsului inflamator în boala inflamatorie intestinală - De la moleculară la integrativă la clinică. World J Gastroenterol. 2007; 13 (1): 1-7. [Link-uri]
Corespondenţă:
Alice Freitas da Silva,
e-mail: [email protected]
Fond de finanțare: nu aici
Conflict de interese: nu aici
Primit pentru publicare: 06/12/2010
Această publicație a fost publicată la data de: 19/04/2011
Lucrare realizată la Hospital de Clinicas da Universidade Federal do Paraná, Ambulatório de Gastroenterologia, Curitiba, PR, Brazilia.
Tot conținutul acestui jurnal, cu excepția cazului în care se menționează altfel, este licențiat sub o licență de atribuire Creative Commons
- Impactul factorilor nutriționali asupra proteomei inducerii Escherichia coli intestinale a
- Helicobacter pylori Gastrita previne colita FullText - Boli inflamatorii intestinale
- Dieta bogată în grăsimi provoacă epuizarea eozinofilelor intestinale asociate cu permeabilitatea intestinală
- IDDF2018-ABS-0203 Modularea disbiozei intestinale la pacienții cu constipație predominant
- Cum să evitați paraziții și viermii intestinali umani